308
Радиохимия, 2019, т. 61, N 4, c. 308-313
Комплексы Np(VI) с анионами циклобутанкарбоновой кислоты
и однозарядными катионами во внешней сфере: [NH4][NpO2(cbc)3],
[C(NH2)3][NpO2(cbc)3], [N(CH3)4][NpO2(cbc)3]
© И. А. Чарушникова*а, М. С. Григорьева, А. М. Федосеева
a Институт физической химии и электрохимии им. А. Н. Фрумкина РАН,
119071, Москва, Ленинский пр., д. 31, корп. 4; * e-mail: charushnikovai@ipc.rssi.ru
Получена 09.07.2018, после доработки 30.08.2018, принята к публикации 30.08.2018
УДК 539.26+546.798.21
Синтезированы и исследованы методом рентгеноструктурного анализа три новых комплекса Np(VI) с
анионами циклобутанкарбоновой кислоты и однозарядными внешнесферными катионами: аммонием -
[NH4][NpO2(cbc)3] (I), гуанидинием - [C(NH2)3][NpO2(cbc)3] (II) и тетраметиламмонием - [N(CH3)4]·
[NpO2(cbc)3] (III). Координационное окружение атомов Np в соединениях I-III - гексагональные бипи-
рамиды с тремя бидентатно-циклическими анионами C4H7COO- в экваториальном поясе. В соединени-
ях I и II внешнесферные катионы NH+ и C(NH2)+ связываются с анионными комплексами [NpO2(cbc)3]-
в трехмерный каркас через водородное взаимодействие типа N-H···O. В комплексе III крупные внешне-
сферные катионы N(CH3)+ являются причиной различия в строении анионных комплексов [NpO2(cbc)3]-.
Ключевые слова: нептуний(VI), циклобутанкарбоновая кислота, синтез, кристаллическая структура.
DOI: 10.1134/S003383111904004X
Карбоксилатные комплексы шестивалентных
сы Np(VI) с однозарядными внешнесферными ка-
актинидов с алканкарбоновыми кислотами, такие
тионами аммония NH+, гуанидиния C(NH2)+ и тетра-
как ацетаты, пропионаты, бутираты, хорошо извест-
метиламмония N(CH3)+:
[NH4][NpO2(cbc)3] (I),
ны и продолжают активно изучаться [1-3]. Высокая
[C(NH2)3][NpO2(cbc)3] (II),
[N(CH3)4][NpO2(cbc)3]
устойчивость карбоновых кислот к окислению по-
(III), cbc- = C4H7(COO)-. На примере этих соедине-
зволяет получить анионные комплексы не только
ний можно также проследить роль водородного свя-
для U(VI), но также для Np(VI), Pu(VI) и даже
зывания в формировании структуры.
Am(VI) [4]. Комплексы An(VI) с алканкарбоновыми
кислотами также характеризуются довольно высо-
Экспериментальная часть
кой устойчивостью, быстрой кристаллизацией из
В работе использовали Hcbc фирмы Aldrich (98%)
водных растворов, что делает их подходящими для
без дополнительной очистки. Перхлорат Np(VI), по-
структурных исследований, позволяющих прово-
лученный упариванием запасных азотнокислых рас-
дить корреляции состав-структура-свойства не
творов с концентрированной HClO4, растворяли в
только по ряду актинидов, но и по ряду карбоновых
воде и осаждали водным раствором аммиака с по-
кислот. Однако с увеличением гидрокарбильного
следующим промыванием полученного осадка во-
радикала вышеуказанные характеристики заметно
дой. Осадок растворяли в водном растворе 0.5 моль/л
меняются и сложно даже оценить возможность син-
Hcbc и добавляли водный раствор ~0.5 моль/л соли,
теза соответствующих соединений в виде монокри-
полученной нейтрализацией циклобутанкарбоновой
сталлов, пригодных для рентгеноструктурного ана-
кислоты аммиаком, карбонатом гуанидиния или гид-
лиза (РСА). Недавно в число объектов исследований
роксидом тетраметиламмония. При медленном испа-
были включены комплексы актинидов с анионами
рении при комнатной температуре (~18-20°C) в ре-
циклопропанкарбоновой [5-7] и циклобутанкарбо-
акционных смесях с NH+, C(NH2)+ и N(CH3)+ образо-
новой [8-10] кислот, в частности, благодаря их стой-
вались кристаллы, пригодные для РСА.
кости к окислению. В случае циклобутанкарбоновой
кислоты (Hcbc) изучены дигидраты
[AnO2(cbc)2·
Рентгенодифракционные эксперименты выполне-
(H2O)2] [An(VI) = U, Np] и моногидраты [AnO2(cbc)2·
ны на автоматическом четырехкружном дифракто-
(H2O)] (An(VI) = Np, Pu) [8], комплексы шестива-
метре с двумерным детектором Bruker Kappa Apex II
лентных U, Np и Pu состава [UO2(bipy)(cbc)2] и
(излучение MoKα, графитовый монохроматор) при
[AnO2(bipy)(cbc)2]·0.5(bipy) [An(VI) = Np, Pu, bipy =
100 К. Параметры элементарных ячеек уточнены по
2,2'-бипиридин] [9] и анионные комплексы [AnO2·
всему массиву данных. В экспериментальные интен-
(cbc)3]- [An(VI) = Np, Pu], содержащие катионы ще-
сивности введены поправки на поглощение с помо-
лочных металлов Na+, K+ и Cs+ [10]. В настоящей
щью программы SADABS [11]. Все структуры рас-
работе выделены и исследованы анионные комплек-
шифрованы прямым методом (SHELXS97
[12]),
Комплексы Np(VI) с анионами циклобутанкарбоновой кислоты
309
Таблица 1. Кристаллографические данные и характеристики рентгеноструктурного эксперимента
[NH4][NpO2(cbc)3]
[C(NH2)3][NpO2(cbc)3]
[N(CH3)4][NpO2(cbc)3]
Параметр
(I)
(II)
(III)
Формула
C15H25NO8Np
C16H27N3O8Np
C19H33NO8Np
М
584.36
626.40
640.46
Сингония
Ромбическая
Тетрагональная
Триклинная
Пространственная группа
P212121
I41/a
P¯
a, Å
11.6090(3)
16.8287(8)
13.4977(11)
b, Å
12.2676(3)
16.8287(8)
16.5702(13)
c, Å
13.0989(4)
30.4145(15)
30.739(2)
α, град
90
90
89.678(2)
β, град
90
90
88.663(2)
γ, град
90
90
84.505(2)
V, Å3; Z
1865.47(9); 4
8613.5(9); 16
6841.6(9); 12
ρвыч., г/см3
2.081
1.932
1.865
μ(MoKα), мм-1
3.634
3.154
2.976
Число измеренных/независимых отражений
16215/5694
31513/3714
78435/36068
Число независимых отражений с I > 2σ(I)
5278
2019
21906
Число уточняемых параметров
238
247
1568
R(F); wR(F2) [I > 2σ(I)]
0.0241; 0.0406
0.0756; 0.1264
0.0506; 0.0775
R(F); wR(F2) [весь массив]
0.0290; 0.0420
0.1538; 0.1570
0.1044; 0.0942
GOOF
0.971
1.186
0.944
Δρmax и Δρmin, e·Å-3
0.842; -0.943
3.710; -3.802
1.484; -1.623
структуры уточнены полноматричным методом наи-
в этих структурах. Отметим, что слишком большой
меньших квадратов (SHELXL-2014 [13]) по F2 по
разброс в некоторых длинах связей в комплексе II
всем данным в анизотропном приближении для всех
(например, Np=O, табл. 2) является следствием низ-
неводородных атомов. Мелкие кристаллы соедине-
кого качества кристалла. В соединении III присутст-
ния II оказались низкого качества, и найденную мо-
вует шесть кристаллографически независимых фор-
дель удалось уточнить только до R1 ~8%. Атомы H
мульных единиц, на рис. 3 представлен фрагмент
анионов C4H7COO- и катионов гуанидиния C(NH2)+
структуры и на примере одной из шести независи-
(II) и тетраметиламмония N(CH3)+ (III) введены на
мых структурных единиц [центральный атом Np(1)
геометрически рассчитанные позиции и уточнены с
анионного комплекса и атом N(1) внешнесферного
UН = 1.2Uэкв(N,C), а атомы H катиона NH+ (I) найде-
катиона N(CH3)+, n = 1] показана нумерация атомов
ны на разностном синтезе Фурье и уточнены с огра-
ничением расстояний N-H и UН = 1.2Uэкв(N).
C(10)
C(9)
Детали рентгеноструктурного эксперимента и
cbc2
основные кристаллографические данные приведены
O(5) C(6)
C(7) C(8)
в табл. 1. Координаты атомов депонированы в Кем-
C(4)
бриджский центр кристаллографических данных, де-
O(4)
C(3)
C(5)
поненты CCDC 1832939-1832941.
O(6)
O(1)
C(2)
Np(1)
cbc1
Результаты и обсуждение
C(1)
O(3) O(2)
O(7)
Основу структур I-III составляют анионные ком-
плексы [NpO2(cbc)3]-, окруженные однозарядными
C(11) C(13)
катионами NH+, C(NH2)+ или N(CH3)+. Анионный
O(8)
комплекс имеет обычное для подобных комплексов
N(1)
C(12)
строение с тремя бидентатно-циклическими аниона-
cbc3
ми C4H7COO- в экваториальном поясе. Координаци-
онные полиэдры (КП) атомов Np - гексагональные
C(15) C(14)
бипирамиды с атомами O катионов NpO2+ в апикаль-
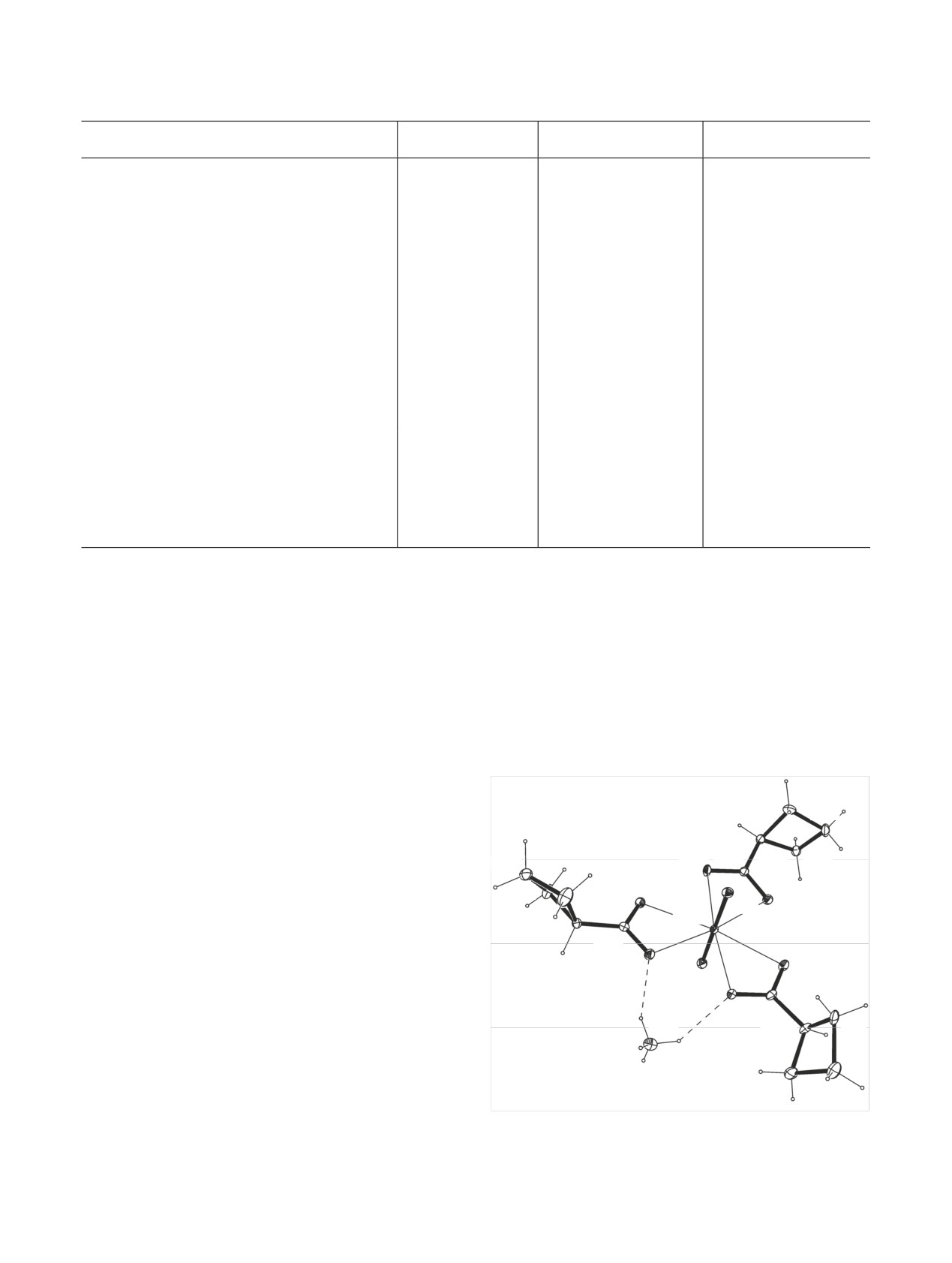
ных позициях. На рис. 1 и 2 представлены фрагмен-
Рис. 1. Фрагмент структуры [NH4][NpO2(cbc)3] (I). Темпера-
ты структур I и II, в табл. 2 - длины связей и валент-
турные эллипсоиды показаны с 30%-ной вероятностью, пунк-
ные углы в координационном окружении атомов Np
тирными линиями показаны водородные связи; то же на рис. 2.
310
И. А. Чарушникова и др.
C(9)
Таблица 2. Длины связей (d) и валентные углы (ω) в КП
C(8)
Np в структурах I и II
Параметр
I
II
cbc2
Связь
d, Å
C(7)
Np(1)=O(1)
1.757(3)
1.849(14)
Np(1)=O(2)
1.748(4)
1.709(15)
O(6)
Np(1)-O(3)
2.478(3)
2.359(12)
C(6)
O(7)
C(13)
C(14)
Np(1)-O(4)
2.475(4)
2.397(13)
O(1)
C(11)
cbc3
Np(1)-O(5)
2.460(3)
2.472(12)
O(5)
C(12)
Np(1)-O(6)
2.461(3)
2.577(14)
Np(1)
C(15)
Np(1)-O(7)
2.448(4)
2.523(12)
O(8)
O(4)
Np(1)-O(8)
2.500(3)
2.462(14)
O(2)
C(1)-O(3)
1.276(6)
1.33(2)
O(3)
C(1)-O(4)
1.267(5)
1.29(2)
C(1)
N(2)
C(1)-C(2)
1.489(6)
1.50(3)
C(5)
C(2)
Среднее (C-C)цикл
1.533(8)
1.51(3)
cbc1
C(16)
C(6)-O(5)
1.266(6)
1.28(2)
N(1)
C(6)-O(6)
1.272(6)
1.31(2)
C(3)
C(6)-C(7)
1.495(6)
1.52(3)
C(4)
N(3)
Среднее (C-C)цикл
1.540(8)
1.54(3)
C(11)-O(7)
1.285(5)
1.33(2)
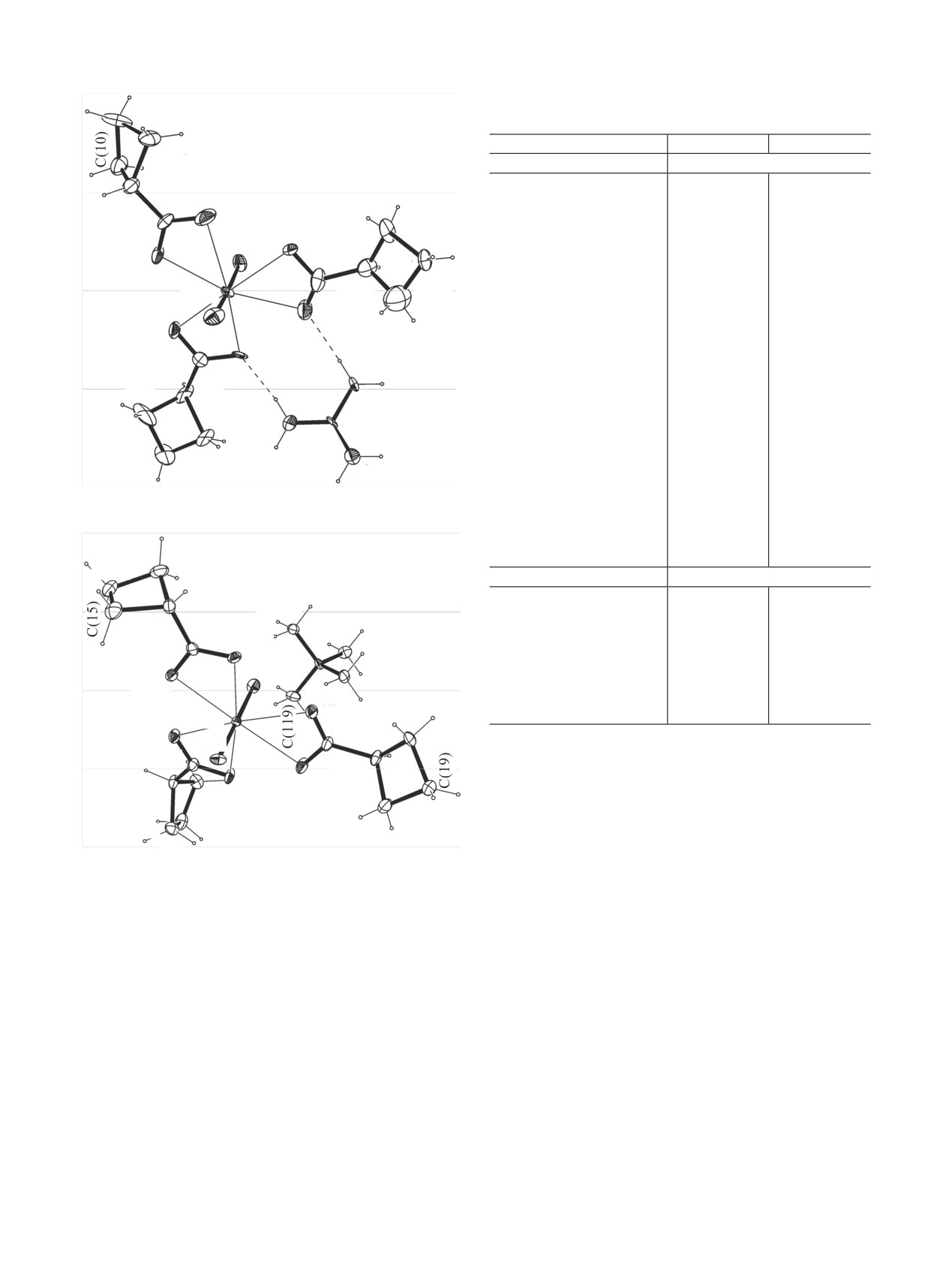
Рис. 2. Фрагмент структуры [C(NH2)3][NpO2(cbc)3] (II).
C(11)-O(8)
1.261(6)
1.21(3)
C(11)-C(12)
1.500(7)
1.54(3)
C(13)
Среднее (C-C)цикл
1.540(7)
1.48(4)
C(14)
Угол
ω, град
cbc1
O(1)=Np(1)=O(2)
179.39(17)
175.1(7)
C(117)
O(3)-Np(1)-O(4)
52.22(11)
55.9(5)
C(12)
C(11)
C(116)
O(5)-Np(1)-O(6)
52.91(12)
52.1(5)
O(14)
O(7)-Np(1)-O(8)
52.57(10)
52.5(5)
N(1)
O(12)
O(3)-Np(1)-O(8)
67.18(11)
68.7(5)
O(13)
C(118)
O(4)-Np(1)-O(5)
67.61(11)
65.4(4)
O(15)
O(6)-Np(1)-O(7)
67.72(11)
65.1(5)
Np(1)
O(18)
C(16)
O(11)
C(18)
C(111)
C(17)
Соединение I можно рассматривать как изострук-
cbc2
O(17)
O(16)
турное соединению Cs[NpO2(cbc)3] [10] с близкими
C(112)
C(115)
параметрами ячейки. В структуре I также можно
cbc3
C(114)
C(110)
выделить 3-связанную сетку, построенную на осно-
C(113)
ве катионов NH+ и NpO2+, в которой каждый атом
Np связан с тремя атомами N и каждый атом N свя-
Рис. 3. Фрагмент структуры [N(CH3)4][NpO2(cbc)3] (III), коор-
зан с тремя атомами Np. Образуется трехмерная сет-
динационное окружение атома Np(1). Температурные эллип-
соиды показаны с 30%-ной вероятностью.
ка (10,3) ([14], с. 139), построенная из десятиуголь-
ников, симметрия которой близка к кубической.
в структуре и табл. 3.
В структурах I и II водородное взаимодействие
типа N-H···O с атомами O анионов C4H7COO- явля-
Различие в строении анионных комплексов [NpO2
ется важным структурообразующим фактором. Каж-
(cbc)3]- в структурах I-III проявляется прежде всего
дый катион NH+ (I) и C(NH2)+ (II) связывает по три
в конформационных особенностях анионов
анионных комплекса [NpO2(cbc)3]- (рис. 4, табл. 5) в
C4H7COO-. Углы перегиба по средней линии цикли-
трехмерный электронейтральный каркас.
ческих фрагментов анионов изменяются в пределах
19-29 (I), 24-35 (II) и 18-32° (III). Торсионные уг-
В отличие от соединений I и II, где положение
лы, показывающие поворот циклического фрагмента
составных частей структуры друг относительно дру-
относительно карбоксилатной группы анионов cbc1,
га фиксирует также и водородное взаимодействие
cbc2, cbc3, рассчитанные через атомы [O(4)C(1)C(2)·
типа N-H···O, в структуре III катионы тетрамети-
C(3)], [O(6)C(6)C(7)C(8)] и [O(8)C(11)C(12)C(13)],
ламмония как доноры протонов образуют весьма
приведены в табл. 4.
слабые водородные связи типа C-H···O c атомами O
Комплексы Np(VI) с анионами циклобутанкарбоновой кислоты
311
Таблица 3. Длины связей (d) и валентные углы (ω) в КП атомов Np в структуре [N(CH3)4][NpO2(cbc)3] (III)
Параметр
Np(1)
Np(2)
Np(3)
Np(4)
Np(5)
Np(6)
Связь
d, Å
Np(n)=O(n1)
1.750(5)
1.748(5)
1.742(5)
1.755(5)
1.747(5)
1.752(5)
Np(n)=O(n2)
1.756(5)
1.759(5)
1.747(5)
1.752(5)
1.758(5)
1.744(6)
Np(n)-O(n3)
2.433(5)
2.473(5)
2.489(5)
2.431(5)
2.443(5)
2.454(5)
Np(n)-O(n4)
2.441(5)
2.434(5)
2.466(5)
2.467(5)
2.450(5)
2.474(5)
Np(n)-O(n5)
2.484(5)
2.475(5)
2.451(5)
2.473(5)
2.461(5)
2.449(5)
Np(n)-O(n6)
2.442(6)
2.490(5)
2.465(5)
2.496(5)
2.446(5)
2.458(5)
Np(n)-O(n7)
2.460(5)
2.448(5)
2.462(5)
2.475(5)
2.418(5)
2.445(5)
Np(n)-O(n8)
2.416(5)
2.425(5)
2.463(5)
2.423(5)
2.475(5)
2.444(5)
C(n1)-O(n3)
1.260(8)
1.252(9)
1.263(8)
1.248(9)
1.251(8)
1.269(9)
C(n1)-O(n4)
1.266(9)
1.287(9)
1.273(9)
1.272(9)
1.269(9)
1.250(8)
C(n1)-C(n2)
1.484(11)
1.497(12)
1.507(10)
1.491(10)
1.494(11)
1.513(10)
Среднее (C-C)цикл
1.548(13)
1.508(15)
1.534(11)
1.512(12)
1.527(12)
1.541(12)
C(n6)-O(n5)
1.263(9)
1.256(9)
1.261(9)
1.261(9)
1.262(9)
1.272(8)
C(n6)-O(n6)
1.262(9)
1.265(8)
1.255(9)
1.262(9)
1.284(8)
1.259(9)
C(n6)-C(n7)
1.506(11)
1.491(10)
1.520(11)
1.519(11)
1.487(11)
1.511(11)
Среднее (C-C)цикл
1.528(12)
1.533(13)
1.540(11)
1.520(14)
1.543(12)
1.527(13)
C(n11)-O(n7)
1.258(9)
1.261(10)
1.276(9)
1.261(9)
1.263(9)
1.258(9)
C(n11)-O(n8)
1.290(9)
1.265(10)
1.257(10)
1.264(8)
1.246(8)
1.280(8)
C(n11)-C(n12)
1.475(10)
1.493(11)
1.511(12)
1.489(10)
1.488(10)
1.493(11)
Среднее (C-C)цикл
1.526(12)
1.526(18)
1.506(15)
1.535(11)
1.526(15)
1.524(13)
Угол
ω, град
O(n1)=Np(n)=O(n2)
179.7(3)
179.3(3)
179.9(3)
179.9(3)
179.2(3)
179.2(3)
O(n3)-Np(n)-O(n4)
53.06(17)
52.85(17)
52.66(17)
52.72(17)
52.95(17)
52.47(17)
O(n5)-Np(n)-O(n6)
52.82(17)
52.24(17)
52.59(17)
52.58(17)
53.17(17)
52.66(16)
O(n7)-Np(n)-O(n8)
53.12(18)
53.06(19)
52.58(17)
52.84(17)
52.49(18)
53.00(16)
O(n3)-Np(n)-O(n8)
66.59(17)
67.01(18)
68.56(17)
65.36(17)
66.13(17)
68.06(17)
O(n4)-Np(n)-O(n5)
69.09(18)
67.65(18)
66.05(17)
66.26(17)
68.69(18)
65.77(16)
O(n6)-Np(n)-O(n7)
65.55(17)
68.14(18)
67.83(18)
70.40(17)
66.60(18)
68.46(16)
Np(1)
O(3)
H(1)
H(2)
Np(1)
O(7b)
O(3)
O(8)
O(8)
C(16)
H(6)
O(4a)
O(5a)
H(3)
H(1)
O(7b)
O(4a)
Np(1a)
Np(1a)
II
I
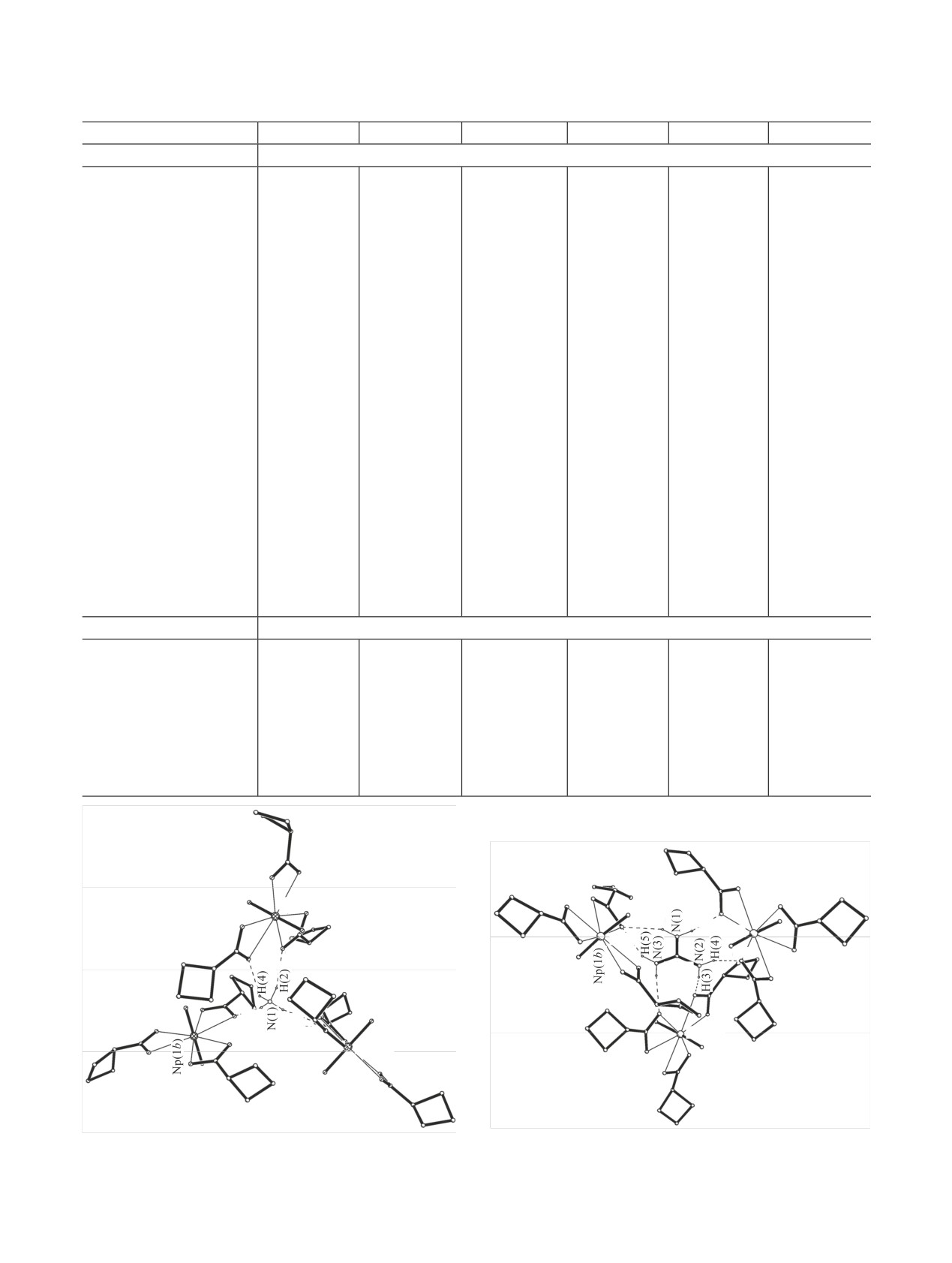
Рис. 4. Водородные связи, образованные катионами NH+ и C(NH2)+ в структурах I и II. Атомы H анионов C4H7COO- не показаны. Опе-
рации симметрии: I: a - (x + 1/2, -y + 3/2, -z), b - (1 - x, y - 1/2, -z + 1/2); II: a - (y + 5/4, -x + 5/4, z + 9/4), b - (x - 1/2, y - 1, -z - 3/2).
312
И. А. Чарушникова и др.
Np(3)
0
c
N(1)
N(2)
Np(4)
Np(1)
N(3)
Np(2)
Np(6)
N(4)
Np(5)
N(5)
N(6)
b
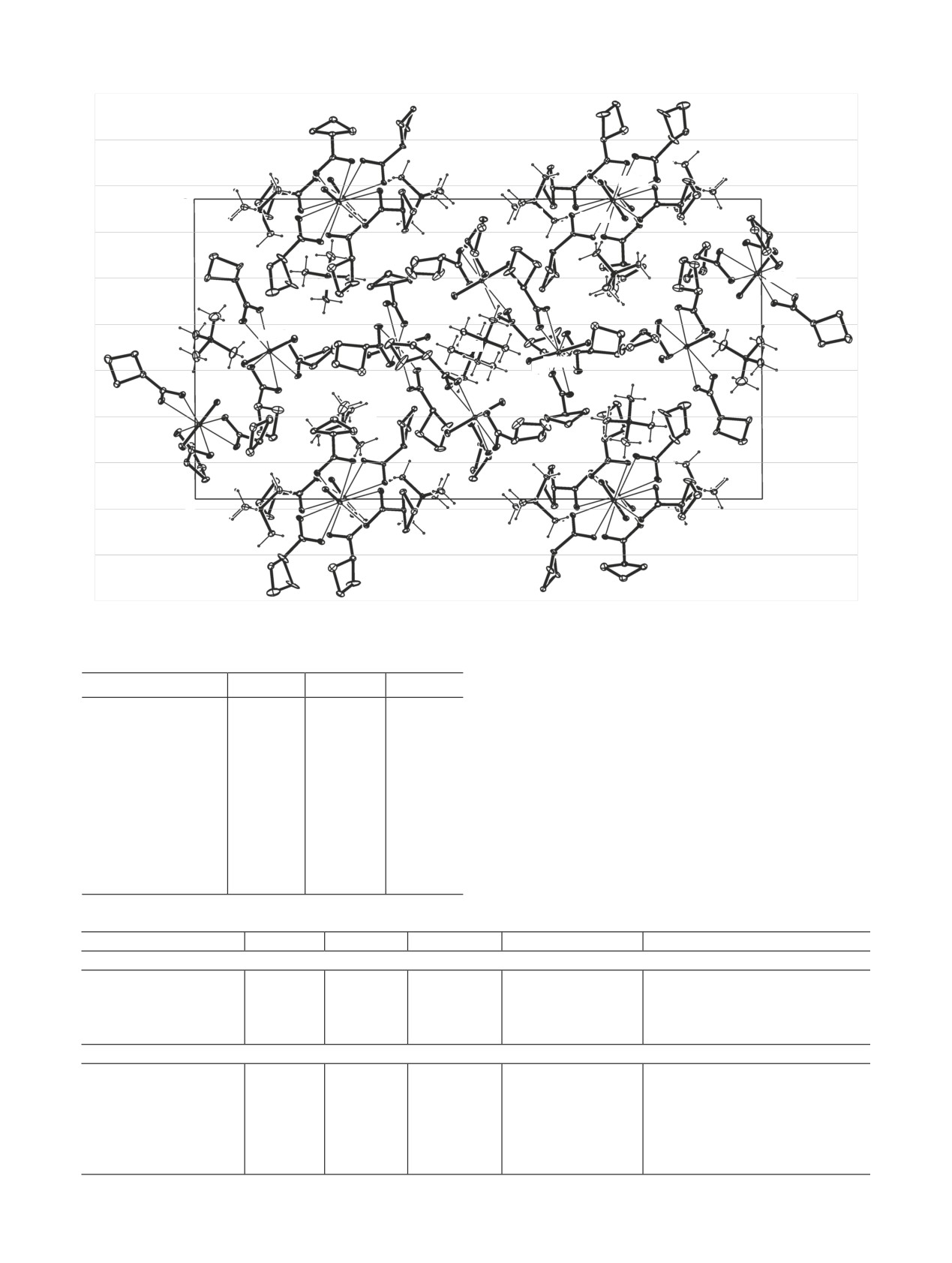
Рис. 5. Упаковка молекул в структуре III. Атомы H анионов C4H7COO- не показаны.
анионных комплексов, и межатомные контакты
Таблица 4. Торсионные углы в структурах I-III (град)
C···O лежат в пределах 3.150(9)-3.484(10) Å. Такой
Соединение
cbc1
cbc2
cbc3
тип взаимодействия не является структурообразую-
I
4.0(7)
28.4(7)
-86.3(6)
щим, но способствует стабилизации структуры. На-
личие в структуре III крупных внешнесферных ка-
II
-154(3)
17(3)
-180(2)
тионов тетраметиламмония обусловливает, по-
III, [Np(1)O2(cbc)3]-
111.6(9)
-166.94(8)
-129.4(8)
видимому, стерические затруднения при упаковке
III, [Np(2)O2(cbc)3]-
-177.1(9)
-0.7(11)
-175.1(11)
катионов и комплексных анионов. Это влияет на
III, [Np(3)O2(cbc)3]-
-175.1(6)
12.1(11)
-60.3(13)
строение анионов [NpO2(cbc)3]- и приводит к кон-
формационному различию между ними и, как след-
III, [Np(4)O2(cbc)3]-
42.5(12)
-21.9(12)
-159.6(7)
ствие, к понижению симметрии кристалла с образо-
III, [Np(5)O2(cbc)3]-
62.6(10)
72.1(10)
-32.9(12)
ванием большого количества кристаллографически
III, [Np(6)O2(cbc)3]-
-127.4(8)
136.7(9)
151.4(8)
независимых формульных единиц (рис. 5).
Таблица 5. Водородные связи в структурах I и II
D-H···A
D-H, Å
H···A, Å
D···A, Å
D-H···A, град
Операция симметрии
[NH4][NpO2(cbc)3] (I)
N(1)-H(1)···O(4)
0.86(2)
1.98(3)
2.835(6)
170(5)
x + 1/2, -y + 3/2, -z
N(1)-H(2)···O(3)
0.84(2)
2.05(4)
2.821(6)
153(6)
N(1)-H(3)···O(7)
0.84(2)
2.00(3)
2.823(5)
165(6)
1 - x, y - 1/2, -z + 1/2
N(1)-H(4)···O(8)
0.84(2)
2.21(4)
2.927(6)
143(5)
[C(NH2)3][NpO2(cbc)3] (II)
N(1)-H(1)···O(7)
0.88
2.12
2.92(2)
152
-y + 5/4, x + 1/4, z + 1/4
N(1)-H(2)···O(3)
0.88
1.89
2.76(2)
172
N(2)-H(3)···O(4)
0.88
1.90
2.77(2)
167
x, y + 1/2, 1 - z
N(2)-H(4)···O(8)
0.88
2.04
2.83(2)
149
N(3)-H(5)···O(7)
0.88
2.26
3.04(2)
148
-y + 5/4, x + 1/4, z + 1/4
N(3)-H(6)···O(5)
0.88
2.14
2.89(2)
144
x, y + 1/2, 1 - z
Комплексы Np(VI) с анионами циклобутанкарбоновой кислоты
313
Таким образом, выделены три новых комплекса
др. // Кристаллография. 2015. Т. 60, N 6. С. 906-914.
[3] Савченков А. В., Вологжанина А. В., Серёжкин В. Н. и
Np(VI) с анионами циклобутанкарбоновой кислоты
др. // Кристаллография. 2014. Т. 59, N 2. С. 235-241.
и однозарядными внешнесферными катионами:
[4] Grigoriev M. S., Fedosseev A. M. // Acta Crystallogr., Sect. C.
[NH4][NpO2(cbc)3] (I), [C(NH2)3][NpO2(cbc)3] (II) и
2011. Vol. 67, N 6. P. m205-m207.
[N(CH3)4][NpO2(cbc)3] (III). Строение комплекса I
[5] Андреев Г. Б., Буданцева Н. А., Федосеев А. М., Анти-
близко к строению изученного ранее соединения
пин М. Ю. // Пятая Рос. конф. по радиохимии «Радио-
химия-2006»: Тез. докл. Дубна, 23-27 октября 2006 г.
Cs[NpO2(cbc)3]. В комплексах I и II водородное
С. 73-74.
взаимодействие типа N-H···O с атомами O анионов
[6] Grigoriev M. S., Fedosseev A. M. // Acta Crystallogr., Sect. C.
C4H7COO- стабилизирует кристаллическую упаков-
2011. Vol. 67, N 6. P. m205-m207.
ку. В комплексе III крупные внешнесферные катио-
[7] Иванова А. Г., Юсов А. Б., Григорьев М. С., Федосе-
ны N(CH3)+ являются причиной различия в стерео-
ев А. М. // Радиохимия. 2014. Т. 56, N 4. С. 317-321.
[8] Чарушникова И. А., Григорьев М. С., Федосеев А. М. //
химии анионных комплексов [NpO2(cbc)3]-.
Радиохимия. 2017. Т. 59, N 5. С. 385-392.
Рентгенодифракционные эксперименты выполне-
[9] Чарушникова И. А., Григорьев М. С., Федосеев А. М. //
ны в ЦКП ФМИ ИФХЭ РАН. Работа выполнена при
Радиохимия. 2017. Т. 59, N 6. С. 488-494.
[10] Григорьев М. С., Чарушникова И. А., Федосеев А. М. //
частичном финансировании Министерством науки и
Радиохимия. 2018. T. 60, N 5. C. 442-446.
высшего образования Российской Федерации (тема
[11] Sheldrick G. M. SADABS. Madison, Wisconsin (USA):
N АААА-А18-118040590105-4).
Bruker AXS, 2008.
[12] Sheldrick G. M. // Acta Crystallogr., Sect. A. 2008. Vol. 64,
N 1. P. 112-122.
Список литературы
[13] Sheldrick G. M. // Acta Crystallogr., Sect. C. 2015. Vol. 71,
[1] Grigoriev M. S., Antipin M. Yu., Krot N. N. // Acta Crys-
N 1. P. 3-8.
tallogr., Sect. E. 2005. Vol. 61, N 10. P. m2078-m2079.
[14] Уэллс А. Структурная неорганическая химия. М.: Мир.
[2] Серёжкин В. Н., Григорьев М. С., Абдульмянов А. Р. и
1987. Т. 1. 408 с.