234
Радиохимия, 2019, т. 61, N 3, c. 234-239
Газофазная конверсия монокарбида урана в нитрующей атмосфере
© С. А. Кулюхин*а, Ю. М. Неволинб, А. В. Гордеева
а Институт физической химии и электрохимии им. А. Н. Фрумкина РАН,
119071, Москва, Ленинский пр., д. 31, корп. 4; * e-mail: kulyukhin@ipc.rssi.ru
б Кафедра радиохимии химического факультета Московского государственного университета им. М. В. Ломоносова,
119991, Москва, Ленинские горы, 1, стр. 10
Получена 02.04.2018, после доработки 27.02.2019, принята к публикации 28.02.2019
УДК 546.799+546.65+ 621.039.72
Исследована газофазная конверсия UC в атмосфере NOx-воздух, NOx-H2O (пар)-воздух и HNO3
(пар)-воздух в интервале температур от 298 до 673 К. Показано, что в процессе газофазной конверсии в
атмосфере NOx-воздух UC переходит в оксиды и оксигидроксиды урана, в меньших количествах обра-
зуются нитраты и гидроксинитраты уранила. В атмосфере NOx-H2O (пар)-воздух и HNO3 (пар)-воздух
основными продуктами конверсии являются гидраты нитратов уранила, при этом нитрование протекает
при меньшей температуре, чем в атмосфере NOx-воздух.
Ключевые слова: карбид урана, газофазная конверсия, нитрующая атмосфера, рентгенофазовый
анализ.
DOI: 10.1134/S0033831119030055
Нитриды или карбиды урана и плутония рас-
Поскольку в настоящее время в литературе от-
сматриваются как основные компоненты высоко-
сутствует информация о поведении UC в атмосфе-
температурного плотного топлива для реакторов на
ре NOx-H2O (пар)-воздух и HNO3 (пар)-воздух, то
быстрых нейтронах [1-5]. При этом переработка
представляло интерес изучить процесс газофазной
как некондиционного ядерного топлива (ЯТ), так и
конверсии UC в нитрирующей атмосфере. Иссле-
отработавшего ядерного топлива (ОЯТ) предусмат-
дование данного процесса и составило цель настоя-
ривает стадию растворения в HNO3. При растворе-
щей работы.
нии карбидного топлива в HNO3 образуются мно-
гоосновные органические кислоты, которые меша-
Экспериментальная часть
ют экстракции Pu [6-8]. В настоящее время найде-
Для получения плотного монолитного образца
ны перспективные пути решения проблем с лока-
UC использовали метод дуговой плавки с нерасхо-
лизацией органических кислот [9, 10]. Однако ос-
таются закономерные проблемы коллоидообразо-
дуемым W-электродом на медном охлаждаемом
вания на стадии растворения ОЯТ в HNO3.
поде [3]. Шихта состояла из графита реакторной
чистоты и металлического урана технической
В работах [11, 12] была исследована газофазная
чистоты. Основные примеси в уране приведены в
конверсия UN в атмосфере NOx-воздух, NOx-H2O
табл. 1.
(пар)-воздух и HNO3 (пар)-воздух (далее - нит-
рующая атмосфера) в интервале температур от 298
Синтез UC проводили следующим образом.
до 723 К. Показано, что в процессе газофазной кон-
Пруток графита дробили на фрагменты размером
версии в атмосфере NOx-H2O (пар)-воздух и HNO3
1-2 мм. Одновременно для удаления пленки UO2
(пар)-воздух UN переходит в водорастворимые
пруток урана диаметром 1.5 мм подвергали электро-
соединения (нитраты, гидроксинитраты). Установ-
полированию в смеси ледяной CH3COOH, насыщен-
лено, что газофазная конверсия UN в атмосфере
ного раствора CrO3 и H2O, взятых в массовом отно-
NOx-H2O (пар)-воздух протекает с меньшей эф-
шении 1 : 1 : 2, при плотности тока 50-200 мА/см2.
фективностью, чем в атмосфере HNO3 (пар)-
После окончания процесса пруток U тщательно
воздух [11]. В атмосфере NOx-воздух можно про-
промывали дистиллированной деаэрированной во-
водить конверсию при более низкой температуре.
дой и сушили в инертной атмосфере. Затем в боксе
При этом образуются как UO3, так и гидраты UO2
с атмосферой Ar из прутка нарезали фрагменты
(NO3)2. Максимальная степень конверсии UN в во-
размером 1.5-2 мм. Смешивали фрагменты графи-
дорастворимые соединения в атмосфере NOx-
та (0.26 г) и U (5.2 г), после чего смесь располагали
воздух, равная ~80%, достигается при температуре
на медном водоохлаждаемом поде дуговой печи.
процесса ~568 К [12].
Перед плавкой проводили вакуумирование камеры
Газофазная конверсия монокарбида урана в нитрующей атмосфере
235
Таблица 1. Основные примеси в металлическом уране технической чистоты
Элемент
Содержание, мас%
Элемент
Содержание, мас%
Элемент
Содержание, мас%
Al
6·10-3
Fe
6·10-3
N
5·10-3
Cu
3·10-3
Mn
1·10-3
C
6·10-2
Ni
1·10-3
Si
6·10-3
B
2·10-5
печи до р = 3-3.5 мм рт.ст. Затем камеру заполняли
Specord M40 (Carl Zeiss) в кварцевых кюветах с
Ar марки ч. и снова вакуумировали камеру печи до
толщиной поглощающего слоя 1-5 см. Концентра-
р = 3-3.5 мм рт.ст. Процедуру заполнения камеры
цию UO2+ рассчитывали по полосе λ = 414 нм [ε =
Ar и вакуумирования повторяли 4 раза с целью
7.8 л/(моль·см)].
удаления из камеры следов O2 и N2. После этого
Порошковые рентгенограммы исходных UC, а
проводили первую дуговую плавку в атмосфере Ar
также продуктов их конверсии в нитрующей атмо-
в течение 40-50 с. После первой плавки камеру
сфере получали на дифрактометре APD-10 (Philips)
вскрывали, слиток переворачивали и производили
с излучением CuKα.
второй переплав по аналогичной технологии с
целью достижения однородности образца. После
Результаты и обсуждение
второго переплава масса образца составляла 5.2 г,
т.е. потери, связанные с испарением, составили
Газовая конверсия UС в атмосфере NOx-воздух
~0.2 г.
Известно, что окисная пленка UO2+x на поверх-
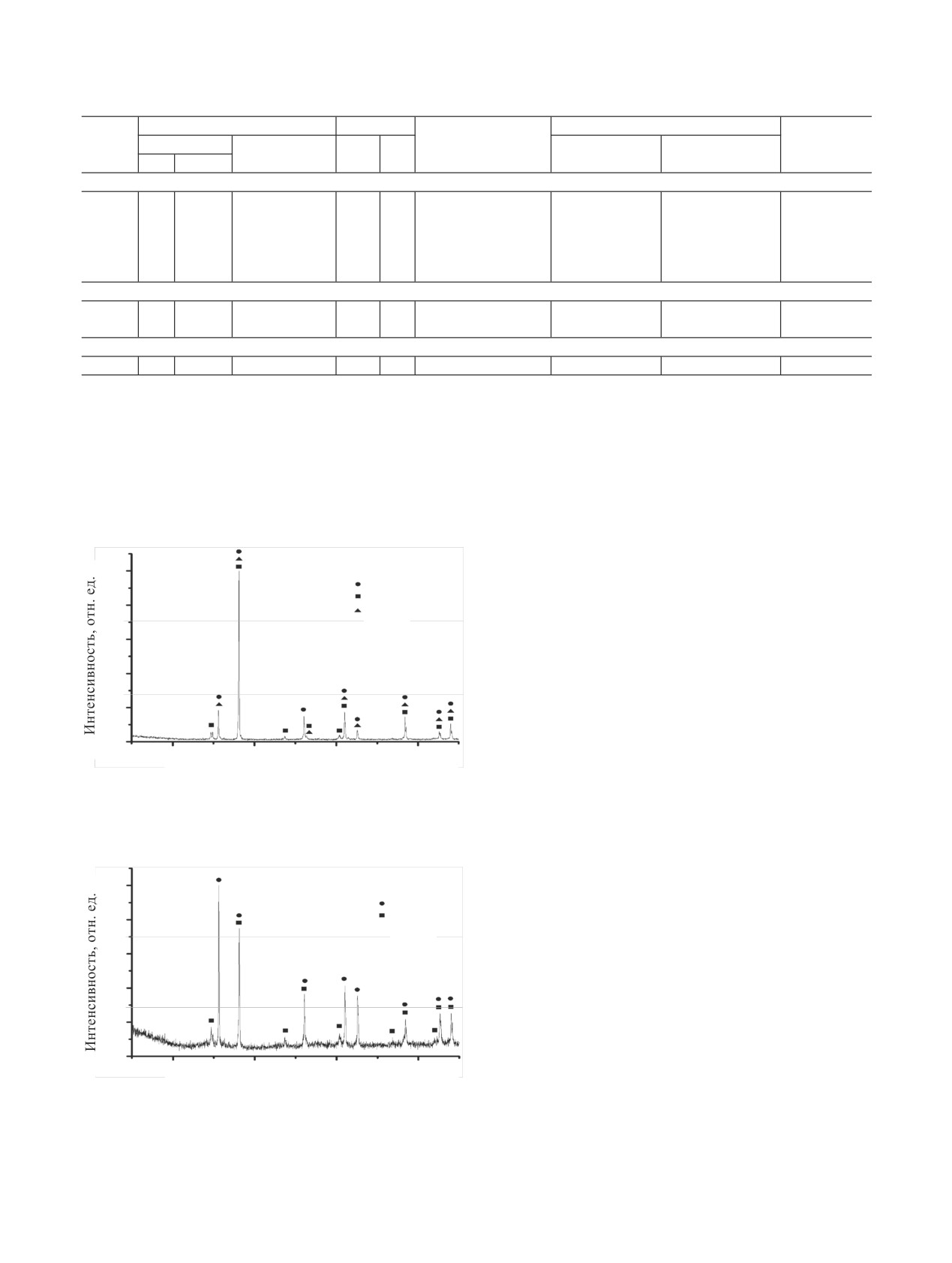
Дифрактограмма измельченного образца UC
ности UC при его хранении на воздухе может дос-
представлена на рис. 1. Анализ рентгенограммы
тигать 0.6 мас% [3]. Поэтому можно предположить,
показал, что синтезированный образец представля-
что процесс конверсии UC в атмосфере NOx-
ет собой монокарбид урана UC [13, 14] c примес-
воздух является двухстадийным, причем первая
ными фазами UC2 [15] и UOx (совпадает с рефлек-
стадия заключается в окислении UC до UO2. В
сами для UO [16]).
предположении образования многоосновных орга-
Азотная кислота, использованная в работе, была
нических кислот [6-8] газофазную конверсию UС в
марки ч. Газообразные NOx получали путем взаи-
атмосфере NOx-воздух с образованием водораство-
модействия 2 г латуни марки Л68, содержащей 67-
римых соединений можно представить следующи-
70% Cu и 30-33% Zn, с 10 мл 12 моль/л HNO3.
ми реакциями:
Эксперименты по газофазной конверсии UC в
(m + 3)UС + (0.5m + 5.5)O2 + (m + 1)H2O →
атмосфере NOx-H2O (пар)-воздух и HNO3 (пар)-
(m + 3)UO2 + СO2 + (HOOC)2(CH2)m (m = 0-3),
(1)
воздух проводили по методикам, приведенным в
работе [11], а в атмосфере NOx-воздух - по мето-
UO2 + 2NO2 + O2 + nH2O → UO2(NO3)2·nH2O
дикам, приведенным в работе [12].
(n = 0, 1, 3 или 6).
(2)
Количество U(VI) в растворе определяли мето-
Согласно реакциям (1) и (2), конверсия в нит-
дом спектрофотометрии. Спектры поглощения рас-
рующей атмосфере должна приводить к измене-
творов UO2+ в воде снимали на спектрофотометре
нию массы образцов. При этом образование новых
фаз U может привести к изменению окраски образ-
цов. Действительно, в результате конверсии UС в
100
нитрующей атмосфере цвет образца менялся с чер-
UC
UC2
ного на светло-желтый или коричневый.
80
UO
При температуре процесса менее ~473 К про-
60
дукт конверсии представлял собой компактный
образец черного цвета. При контакте с водой про-
40
дукт конверсии не растворялся, давая компактный
черный осадок. Фазовый состав отмытого черного
20
осадка соответствовал исходному UС. Анализ ре-
0
зультатов эксперимента показал, что при темпера-
20
40
60
80
турах ниже ~473 К в присутствии NOx конверсии
2θ, град
UC не происходит (опыты 1 и 2, табл. 2).
Рис. 1. Порошковая дифрактограмма монокарбида урана. На-
блюдаемые рефлексы UC [13, 14], UC2 [15], UO [16].
При температуре процесса ~473 К продукт кон-
236
С. А. Кулюхин и др.
Таблица 2. Конверсия UС в нитрующей атмосфере
Навеска
Δm
Растворимость в воде
Номер
Время выдержки/T,
Конверсия
исходная
после выдерж-
U в растворе,
нерастворимый
опыта
г
%
К
UС, %а
г
ммоль
ки, г
ммоль
остаток, г
NOx-воздух
1
0.27
1.08
0.27
~0
~0
5 ч/403
~0
0.27
~0
2
0.25
1.00
0.25
~0
~0
5 ч/423
~0
0.25
~0
3
0.41
1.64
0.46
0.05
~12
5 ч/473
0.31
0.35
~19
4
0.39
1.56
0.40
0.01
~3
5 ч/568
0.17
0.39
~11
5
0.28
1.12
0.31
0.03
~11
5 ч/673
0.09
0.30
~8
Смесь NOx и H2O (пар)
6
0.44
1.76
0.76
0.32
~73
6 сут/303
1.60
0.04
~91
7
0.37
1.48
0.66
0.29
~78
5 ч/403
1.48
~0
~100
HNO3 (пар)б
8
1.18
4.72
1.95
0.78
~66
5 ч/403
3.73
0.13
~79
а Конверсию рассчитывали как отношение содержания U в растворе к его исходному количеству
б UС выдерживали в парах 12 моль/л HNO3.
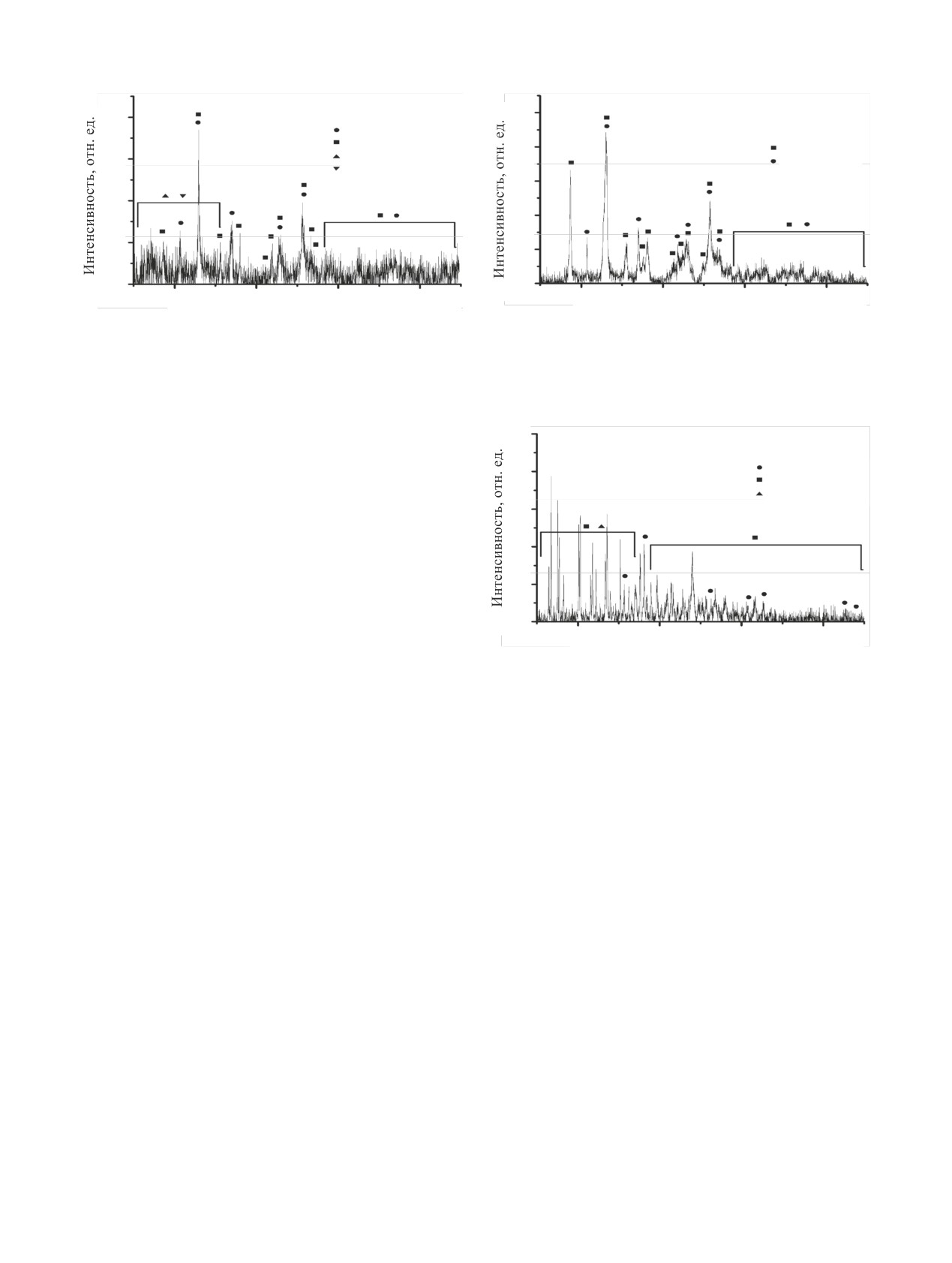
версии представлял собой компактный образец
осадок. Фазовый состав отмытого черного осадка
черного цвета, покрытый желтой пленкой. При
соответствовал исходному UC (рис. 2), а спектр
контакте с водой желтая пленка быстро растворя-
оптического поглощения водного раствора имел
лась с образованием раствора бледно-желтого цве-
полосу поглощения, характерную для UO2+. Сте-
та. При этом оставался порошкообразный черный
пень конверсии UС в водорастворимые соединения
при ~473 К составила ~19% (опыт 3, табл. 2).
100
С целью увеличения степени конверсии UС в
UC
UC2
водорастворимые соединения были проведены экс-
80
UO
перименты при ~568 и ~673 К. Однако с увеличе-
нием температуры процесса степень конверсии UС
60
в водорастворимые соединения уменьшалась
40
(опыты 4 и 5, табл. 2).
В экспериментах при ~568 К продукт конверсии
20
UС представлял собой влажный плав кирпично-
0
красного цвета, рентгенофазовый анализ которого
20
40
60
80
оказался невозможным. При контакте продукта
2θ, град
конверсии с водой образовывался желтый раствор
Рис.
2. Порошковая дифрактограмма не растворившегося в
и оставался нерастворимый красный осадок.
воде осадка, образовавшегося после контакта с водой продук-
Спектр оптического поглощения раствора содер-
тов конверсии UC в NOx, проведенной при ~473 К в течение
5 ч. Наблюдаемые рефлексы UC [13, 14], UC2 [15], UO [16].
жал полосы, характерные для UO2+. При этом сте-
пень конверсии UN в водорастворимые соединения
составляла ~11% (опыт 4, табл. 2). Порошковая
100
UC
дифрактограмма нерастворимого в воде красного
80
UC2
осадка, представленная на рис. 3, содержит уши-
ренные рефлексы исходного карбида урана. При
60
этом образования фаз UO3 или UO3·nH2O, чье при-
сутствие могло бы объяснять красный цвет осадка,
40
не наблюдалось.
20
Конверсия UС в атмосфере NOx при ~673 К при-
водила к образованию темно-красных порошков. В
0
составе продукта конверсии наблюдались гидраты
20
40
60
80
2θ, град
нитратов и гидроксинитратов уранила, с одной сто-
Рис.
3. Порошковая дифрактограмма не растворившегося в
роны, и оксиды и оксигидроксиды урана, с другой
воде осадка, образовавшегося после контакта с водой продук-
стороны (рис. 4). Соединение UO3·0.8H2O обуслов-
тов конверсии UC в атмосфере NOx-воздух, проведенной при
ливает красный оттенок продуктов конверсии. При
~568 К в течение 5 ч. Наблюдаемые рефлексы UC [13, 14], UC2
[15].
взаимодействии продуктов конверсии UС с водой
Газофазная конверсия монокарбида урана в нитрующей атмосфере
237
100
80
U3O8
UO3·0.8H2O
80
UO3·0.8H2O
60
UO2(NO3)2·3H2O
U3O8
UO2OH(NO3)·3H2O
60
40
40
20
20
0
0
20
40
60
80
20
40
60
80
2θ, град
2θ, град
Рис. 5. Порошковая дифрактограмма не растворившегося в
Рис. 4. Порошковая дифрактограмма продуктов конверсии UC
воде осадка, образовавшегося после контакта с водой продук-
в атмосфере NOx-воздух, проведенной при ~675 К в течение
тов конверсии UC в атмосфере NOx-воздух, проведенной при
5 ч. Наблюдаемые рефлексы UO3·0.8H2O [17], U3O8 [18],
~675 К в течение 5 ч. Наблюдаемые рефлексы UO3·0.8H2O
UO2(NO3)2·3H2O [19], UO2OH(NO3)·3H2O [20].
[17], U3O8 [18].
100
образовывался бледно-желтый раствор и оставался
нерастворимый темно-коричневый осадок. Спектр
UC
80
оптического поглощения раствора продуктов кон-
UO2(NO3)2·6H2O
версии содержал полосу, характерную для иона
UO2(NO3)2·3H2O
60
UO2+. Степень конверсии UС в водорастворимые
соединения составила ~8% (опыт 5, табл. 2). Фазо-
40
вый состав нерастворимого в воде осадка представ-
лял собой смесь UO3·nH2O и U3O8 (рис. 5).
20
Максимальная степень конверсии UС в нитраты
или гидроксинитраты уранила наблюдалась при
0
20
40
60
80
~473 К.
2θ, град
Как было показано в работе [12], даже неболь-
Рис. 6. Порошковая дифрактограмма продуктов конверсии UC
шие следы влаги приводили к существенному уве-
в атмосфере NOx-H2O (пар)-воздух, проведенной при ~403 К в
течение 5 ч. Наблюдаемые рефлексы UC [13, 14], UO2(NO3)2·
личению степени конверсии UN в водораствори-
3H2O [19], UO2(NO3)2·6H2O [21].
мые соединения, в связи с чем представляло инте-
рес исследовать конверсию UC в атмосфере NOx-
Согласно реакциям (3)-(5), конверсия в нитрую-
H2O (пар)-воздух и HNO3 (пар)-воздух.
щей атмосфере должна приводить к изменению
массы образцов. При этом образование новых фаз
Конверсия UC в атмосфере NOx-H2O (пар)-воздух
U может привести к изменению окраски образцов.
и HNO3 (пар)-воздух
Действительно, в результате газофазной конверсии
UC в атмосфере NOx-H2O (пар)-воздух и HNO3
Конверсия UC в атмосфере NOx-H2O (пар)-
(пар)-воздух образовывался объемный порошок
воздух и HNO3 (пар)-воздух также, по-видимому,
или плав коричневого цвета.
начинается с окисления UC до UO2. Поэтому в
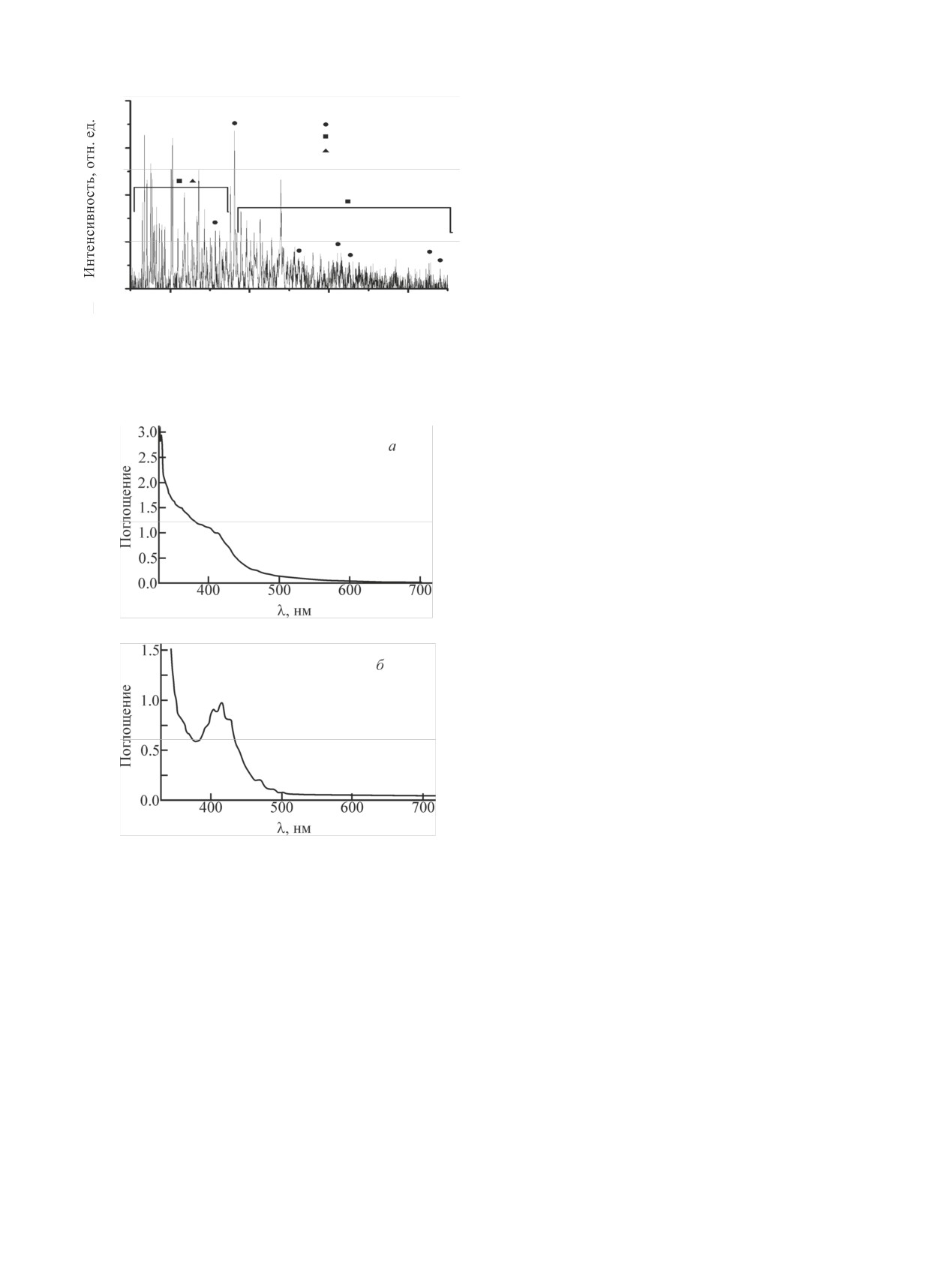
На рис. 6 и 7 приведены порошковые дифракто-
предположении образования многоосновных орга-
граммы продуктов конверсии UC в атмосфере
нических кислот [6-8] газофазная конверсия UC с
NOx-H2O (пар)-воздух и HNO3 (пар)-воздух, про-
образованием водорастворимых соединений может
веденной при температуре ~403 К и времени вы-
быть описана следующими реакциями:
держки 5 ч.
Полученные рентгенограммы продуктов кон-
(m + 3)UС + (m + 6)O2 + (m + 1)H2O → (m + 3)UO2 +
версии содержат рефлексы исходного карбида ма-
+ СO2 + (HOOC)2(CH2)m (m = 0-3),
(3)
лой интенсивности. Наблюдаются интенсивные
рефлексы, соответствующие гидратам нитрата ура-
UO2 + 2NO2 + O2 + nH2O → UO2(NO3)2·nH2O (n = 0, 1, 3
нила.
или 6),
(4)
При контакте с водой продукты конверсии рас-
UO2 + 2HNO3 + 1/2O2 → UO2(NO3)2 + H2O.
(5)
творяются с образованием темно-коричневого рас-
238
С. А. Кулюхин и др.
80
тате многочасового центрифугирования при скоро-
UC
сти 3000 об/мин оставался коричневый раствор, из
UO2(NO3)2·6H2O
которого со временем снова выделялся коричне-
60
UO2(NO3)2·3H2O
вый осадок. Подкисление раствора также не приво-
дило к его осветлению. Для определения U(VI) в
40
маточных растворах, образовавшихся при раство-
рении продуктов конверсии UС в воде, провели
20
озонирование коричневых растворов. Для барботи-
рования использовали газовый поток, содержащий
~150 мг/л О3. В результате барботирования O3 в
0
20
40
60
80
течение 3-5 мин коричневая окраска раствора, так
2θ, град
же как и следы осадков коричневого цвета, исчеза-
Рис. 7. Порошковая дифрактограмма продуктов конверсии UC
ла, и раствор принимал желтую окраску, характер-
в атмосфере HNO3 (пар)-воздух, проведенной при ~403 К в
ную для UO2+. На рис. 8 приведены спектры погло-
течение 5 ч. Наблюдаемые рефлексы UC [13, 14], UO2(NO3)2·
щения водного раствора, образовавшегося при рас-
3H2O [19], UO2(NO3)2·6H2O [21].
творении продуктов конверсии UС в атмосфере
HNO3 (пар)-воздух, проведенной при ~403 К в те-
чение 5 ч, до и после озонирования.
В табл. 2 приведены экспериментальные резуль-
таты, полученные при конверсии образцов UС в
атмосфере NOx-H2O (пар)-воздух и HNO3 (пар)-
воздух. Как видно из табл. 2, во всех эксперимен-
тах наблюдалось увеличение массы, что говорит об
изменении химического состава образцов. Конвер-
сия UС может протекать через образование на по-
верхности образца UO2, U3O8 и UO2(OH)2, которые
в дальнейшем, по-видимому, подвергаются нитро-
ванию с образованием нитрата или гидроксинитра-
тов уранила.
В работе [11] показано, что выдержка компакт-
ного монолитного образца UN в атмосфере NOx-
H2O (пар)-воздух при ~293 К за 6 сут не привела к
значительной конверсии UN в водорастворимые
соединения. Степень конверсии составляла ~4%. В
связи с этим опыты по конверсии UC в атмосфере
NOx-H2O (пар)-воздух при ~303 К за 6 сут прово-
дили на порошкообразном образце. Оказалось, что
использование порошкообразного UC позволяет
Рис. 8. Спектр поглощения водного раствора, образовавшегося
при растворении продуктов конверсии UС в атмосфере HNO3
провести его значительную конверсию в водорас-
(пар)-воздух, проведенной при ~403 К в течение 5 ч, до (а) и
творимые соединения за 6 сут даже при ~303 К.
после (б) озонирования.
Степень конверсии составляет
~91% (опыт
6,
табл. 2) По-видимому, большая удельная поверх-
твора (рН 3-5). В растворе наблюдается нераство-
ность порошка UС способствует быстрому проте-
рившийся осадок двух типов: мелкокристалличе-
канию конверсии образца.
ский черного цвета (по-видимому, UC) и хлопье-
При изучении компактного монолитного образ-
видный темно-коричневого цвета (по-видимому,
ца UC с целью сокращения времени процесса кон-
углеродсодержащие соединения).
версии и увеличения скорость процесса были про-
Суспензию центрифугировали и отделяли рас-
ведены эксперименты при повышенной температу-
твор от осадка. Осадок промывали водой, сушили
ре, но при более коротком времени выдержки сис-
при температуре ~303 К на воздухе и взвешивали.
темы. Оказалось, что сокращение времени процес-
Необходимо отметить, что провести полное отде-
са до 5 ч при одновременном увеличении темпера-
ление осадков от маточного раствора центрифуги-
туры процесса до ~403 К позволяет также получить
рованием не представляется возможным. В резуль-
высокие степени конверсии UC. Так, за 5 ч вы-
Газофазная конверсия монокарбида урана в нитрующей атмосфере
239
держки UC в атмосфере NOx-H2O (пар)-воздух и
Меньшикова Т. С. Высокотемпературное ядерное топ-
ливо. М.: Атомиздат, 1978.
HNO3 (пар)-воздух при температуре ~403 К сте-
[4] Mishra S., Kaity S., Banerjee J. et al. // J. Nucl. Mater. 2018.
пень конверсии в водорастворимые соединения
Vol. 499. P. 272-283.
составляет ~100 и ~80% соответственно (опыты 7 и
[5] Двоеглазов К. Н., Шадрин А. Н., Щудегова О. В. и др. //
8, табл. 2). Следует отметить, что при одинаковых
Вопр. атом. науки и техники. 2016. N 4 (87). С. 81-90.
[6] Zverev D. V., Kirillov S. N., Dvoeglazov K. N. et al. // Proc.
условиях выдержки степень конверсии UС в водо-
ATALANTE 2012 Int. Conf. on Nuclear Chemistry for Sus-
растворимые соединения в атмосфере HNO3 (пар)-
tainable Fuel Cycle. 2012. Vol. 7. P. 116-122.
воздух несколько меньше, чем в атмосфере NOx-
[7] Natarajan R. // Proc. 16th Annual Conf. of Indian Nuclear
H2O (пар)-воздух. Этот результат позволяет сде-
Society INSAC-2005. Mumbai, 2005. Paper IT_21.
[8] Кудинов А. С., Голецкий Н. Д., Зильберман Б. Я. и др. //
лать вывод о том, что при данной температуре в
VII Рос. конф. по радиохимии «Радиохимия-2012»: Тез.
газовой фазе происходит неполное термическое
докл. Димитровград, 2012. С. 143.
разложение HNO3 до смеси NOx-H2O (пар), кото-
[9] Кудинов А. С., Голецкий Н. Д., Зильберман Б. Я. и др. //
рая обладает большей химической активностью в
VIII Рос. конф. по радиохимии «Радиохимия-2015»: Тез.
докл. Железногорск, 2015. С. 180.
отношении UC.
[10] Кудинов А. С., Голецкий Н. Д., Зильберман Б. Я. и др. Па-
Таким образом, в результате проведенных экс-
тент RU 2529185 // Б.И. 2014. N 27.
периментов показана возможность газофазной кон-
[11] Кулюхин С. А., Неволин Ю. М., Гордеев А. В. // Радиохи-
мия. 2019. T. 61, N 1. C. 18-26.
версии UC в водорастворимые соединения в нит-
[12] Кулюхин С. А., Неволин Ю. М., Гордеев А. В., Бессо-
рующей атмосфере. В то же время необходимо от-
нов А. А. // Радиохимия. 2019. T. 61, N 2. C. 108-116.
метить, что использование данного подхода требу-
[13] JCPDS—Int. Centre for Diffraction Data. PDF 73-1709, UC
ет озонирования получаемых растворов с целью
(cubic).
[14] JCPDS—Int. Centre for Diffraction Data. PDF 03-065-8815,
удаления органических примесей, в том числе мно-
UC.
гоосновных кислот. В связи с этим необходимой
[15] JCPDS—Int. Centre for Diffraction Data. PDF 01-084-1344,
операцией перед газофазной конверсией карбидно-
UC2.
го ОЯТ в нитрующей атмосфере является его объ-
[16] JCPDS—Int. Centre for Diffraction Data. PDF 01-073-1714,
емное окисление (волоксидация) в различных ат-
UO.
[17] JCPDS—Int. Centre for Diffraction Data. PDF 00-010-0309,
мосферах.
UO3·0.8H2O.
[18] JCPDS—Int. Centre for Diffraction Data. PDF 01-074-2101,
Список литературы
α-U3O8.
[19] JCPDS—Int. Centre for Diffraction Data. PDF 00-027-0937,
[1] Алексеев С. В., Зайцев В. А. Нитридное топливо для ядер-
UO2(NO3)2·3H2O.
ной энергетики. М.: Техносфера, 2013.
[20] JCPDS—Int. Centre for Diffraction Data. PDF 00-016-0204,
[2] State-of-the-art report on innovative fuels for advanced nu-
UO2OH(NO3)·3H2O.
clear systems: NEA Report. 2014. N 6895.
[21] JCPDS—Int. Centre for Diffraction Data. PDF 01-077-0121,
[3] Котельников Р. Б., Башлыков С. Н., Каштанов А. И.,
UO2(NO3)2·6H2O.