152
Радиохимия, 2019, т. 61, N 2, c. 152-155
Поведение солей щелочных металлов и аммония
при нанофильтрации их водных растворов
© В. О. Каптаков, В. В. Милютин*, Н. А. Некрасова
Институт физической химии и электрохимии имени А. Н. Фрумкина РАН,
119071, Москва, Ленинский пр., д. 31, корп. 4; * e-mail: vmilyutin@mail.ru
Получена 26.03.2018, после доработки 26.03.2018, принята к публикации 05.04.2018
УДК 66.081+544.58
Исследовано поведение солей (хлоридов, нитратов, сульфатов, фосфатов, боратов, ферри- и ферро-
цианидов) различных щелочных металлов (Li, Na, K, Cs) и аммония при нанофильтрации (НФ) их вод-
ных растворов. Показано, что НФ полимерная мембрана в области высоких концентраций солей (более
30 г/дм3) обладает низкой (1-5%) задерживающей способностью по отношению к ионам щелочных ме-
таллов и аммония. При более низких концентрациях солей задерживающая способность НФ мембраны
увеличивается. При нанофильтрации растворов солей Na и K с анионами различного заряда задержи-
вающая способность НФ мембраны повышается при увеличении заряда аниона. Изучена зависимость
задерживающей способности НФ мембраны по нитрату натрия от рН. Показано, что данный показатель
постоянен в диапазонах рН 2.0-5.5 и 7.5-13.0, в области рН 5.5-7.5 задерживающая способность снижа-
ется примерно в 2 раза. При изучении задержания боратов натрия различного состава обнаружено, что
растворы, содержащие крупные полиядерные анионы, состоящие из 4-5 атомов бора, задерживаются
НФ мембраной с эффективностью 45-50%, а нейтральные молекулы борной кислоты мембраной прак-
тически не задерживаются. Сделан вывод о том, что метод нанофильтрации может быть использован
для селективного отделения неактивных солей щелочных металлов от радиоактивных компонентов
жидких радиоактивных отходов.
Ключевые слова: нанофильтрация, полимерная мембрана, соли щелочных металлов, извлечение.
DOI: 10.1134/S0033831119020114
В настоящее время мембранные методы (об-
обусловленную наличием на поверхности НФ мем-
ратный осмос, ультра- и микрофильтрация) все ши-
браны активных заряженных функциональных
ре используются в процессах водоподготовки и
групп, диссоциирующих при контакте с разделяе-
очистки сточных вод от токсичных примесей [1].
мым раствором. В связи с этим в процессе нано-
Применительно к очистке жидких радиоактивных
фильтрации появляется возможность более эффек-
отходов (ЖРО) эти методы имеют ряд недостатков
тивного задержания многозарядных ионов по срав-
и ограничений. Обратноосмотические мембраны
нению с однозарядными [4-6]. Данная особенность
способны к задержанию практически всех компо-
нанофильтрации делает ее весьма перспективной
нентов очищаемых растворов. При этом происхо-
для переработки ЖРО с высоким солесодержани-
дит концентрирование не только радиоактивных,
ем, в которых основной солевой фон составляют
но и всех неактивных компонентов, что приводит к
соли одновалентных щелочных металлов.
образованию значительных количеств вторичных
Ранее [7] нами исследовано извлечение из рас-
отходов - высокосолевых концентратов обратного
творов ряда двух- и трехзарядных ионов металлов,
осмоса. Другим ограничением обратного осмоса
а также микроколичеств радионуклидов 137Cs, 85Sr
является невозможность переработки высокосоле-
вых (более 30-50 г/дм3) растворов. Микро- и ульт-
и 60Co нанофильтрационной мембраной производ-
рафильтрационные мембраны весьма эффективны
ства российской компании «РМ Нанотех». Была
для очистки растворов от нерастворимых форм
показана высокая селективность НФ мембраны при
примесей (коллоидов, псевдоколллоидов, взвесей)
задержании многозарядных катионов металлов, а
[2, 3], однако, при этом не происходит удаления
также микроколичеств 85Sr и 60Co.
растворимых (ионных) форм извлекаемых компо-
В настоящей работе более детально исследована
нентов.
способность НФ мембраны компании «РМ Нано-
Метод нанофильтрации (НФ) в отличие от дру-
тех» задерживать соли различных щелочных ме-
гих баромембранных процессов включает в себя
таллов и аммония, которые, как было сказано вы-
помимо диффузионной и конвективной электроста-
ше, часто определяют основной солевой фон жид-
тическую составляющую механизма разделения,
ких радиоактивных отходов.
Поведение солей щелочных металлов и аммония при нанофильтрации их водных растворов
153
Экспериментальная часть
борной кислоте и боратам натрия различного со-
става. Для этого в раствор борной кислоты с кон-
Для изучения извлечения ионов из растворов
центрацией 0.5 моль/дм3 с рН 6.1 добавляли рас-
методом нанофильтрации (НФ) использовали нано-
твор ~12 моль/дм3 NaOH до достижения мольного
фильтрационную полимерную мембрану производ-
соотношения NaOH/Н3ВО3 = 0.20, 0.40, 0.50 и 1.00
ства компании «РМ Нанотех» (Владимир, Россия).
с образованием растворов боратов натрия состава
Мембрана имеет многослойную структуру: ниж-
NaВ5О8, Na2НВ5О9, Na2В4О7 и NaВО2 с рН 8, 9.1,
ний слой (подложка) изготовлен из нетканого по-
9.6 и 11.5 соответственно. Для поддержания посто-
лиэфира (лавсана); второй (промежуточный) слой -
янной концентрации ионов натрия в растворе
из полисульфонамида; третий (селективный) слой
(0.5 моль/дм3) в раствор добавляли рассчитанное
- из полипиперазинамида. Основные характеристи-
количество NaNO3. Концентрацию борной кислоты
ки НФ мембраны: размер пор 1-2 нм, рабочий диа-
и борат-ионов в растворах определяли объемным
пазон рН 1-12 (при 20-25°С), максимальная рабо-
методом путем титрования раствором 0.2 моль/дм3
чая температура 45°С.
NaOH в присутствии маннита [10].
НФ мембрану испытывали в составе лаборатор-
Для определения зависимости задерживающей
ной установки, состоящей из НФ модуля типа
способности НФ мембраны от pH в раствор NaNO3
NanoNF-1812 с полезной площадью фильтрации
с концентрацией
10 г/дм3 добавляли растворы
0.3 м2, циркуляционного насоса и манометров на
~1 моль/дм3 HNO3 или NaOH. Значения рН раство-
входе и на выходе модуля.
ров измеряли с использованием иономера марки
Эксперименты проводили по следующей мето-
«Экотест 2000».
дике: модельный раствор помещали в исходную
Для приготовления модельных растворов ис-
емкость и при помощи насоса пропускали его че-
пользовали дистиллированную воду и реагенты
рез НФ модуль в режиме циркуляции. Фильтрацию
квалификации ч.д.а. или х.ч.
проводили при постоянном давлении на мембране,
равном 6.5-7.0 атм. Периодически отбирали пробы
Результаты и обсуждение
фильтрата после мембраны и измеряли в нем кон-
центрацию извлекаемого компонента. По получен-
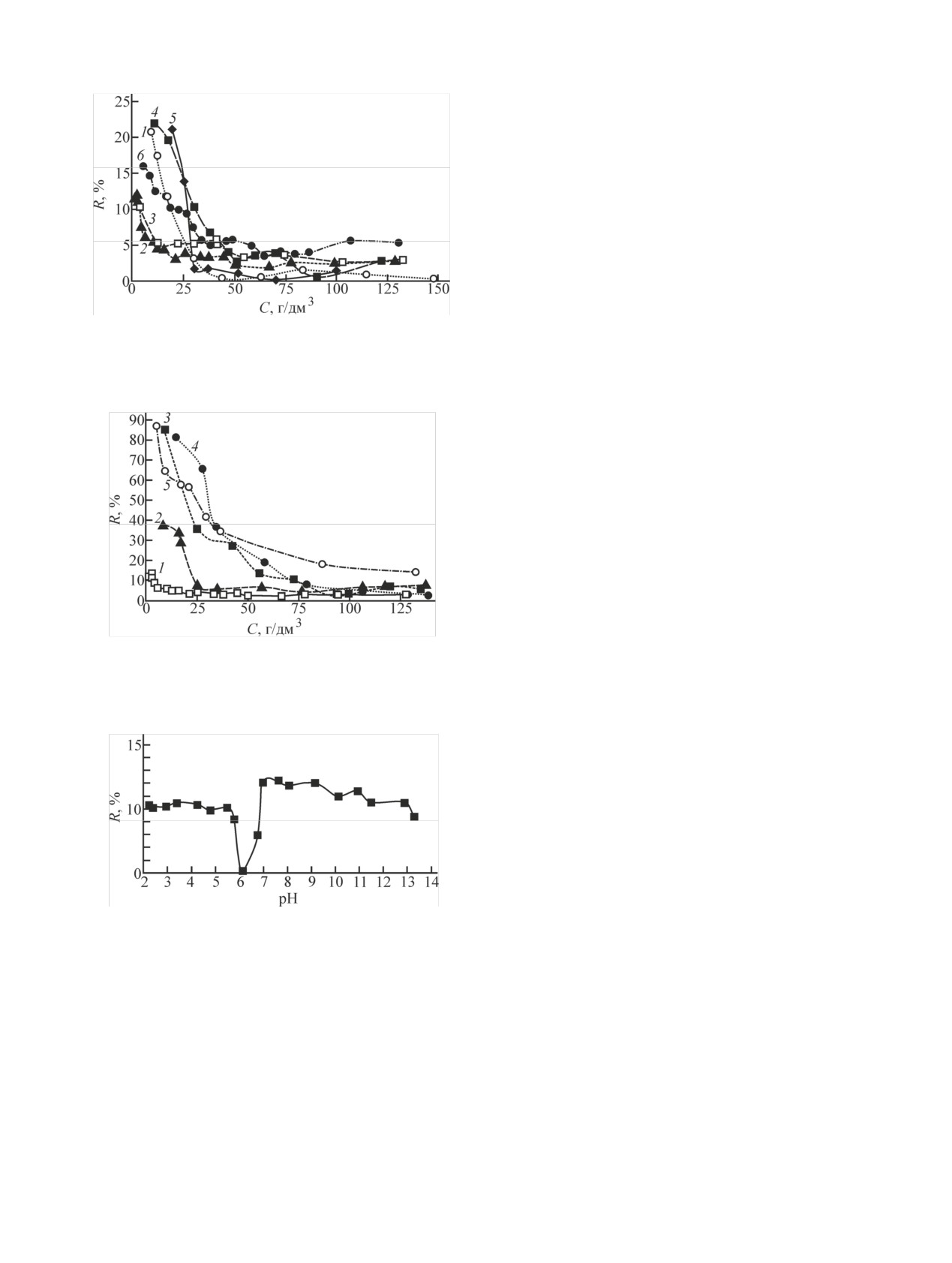
Результаты определения зависимости задержи-
ным результатам рассчитывали значение задержи-
вающей способности (R) НФ мембраны от концен-
вающей способности (R) НФ мембраны по соответ-
трации солей (хлоридов и нитратов) различных
ствующему компоненту по формуле
щелочных металлов и аммония представлены на
рис. 1. Полученные результаты показали, что для
R = (1 - Сф/С0)·100%,
растворов хлоридов и нитратов лития, натрия, ка-
лия, цезия и аммония наблюдается одна и та же
где Сф, С0 - концентрация компонента в фильтрате
закономерность. В области высоких концентраций
после мембраны и в исходном растворе соответст-
солей (более 30 г/дм3) значение R постоянно и на-
венно.
ходится на уровне 1-5%. В данной области концен-
В работе изучали задерживающую способность
траций наблюдается корреляция между размером
НФ мембраны в водных растворах следующих со-
гидратированного иона и R: более крупные ионы
лей: LiNO3, NaNO3, NaCl, KCl, NН4NO3, CsNO3,
(Cs+) задерживаются несколько сильнее ионов с
Na2SO4, Na3PO4, K3Fe(CN)6, K4Fe(CN)6. рН раство-
меньшим размером. При концентрации солей ме-
ра Na3PO4 составлял 12.0, растворов всех осталь-
нее 30 г/дм3 для всех солей наблюдается резкое
ных солей - около 6. В процессе экспериментов
увеличение задерживающей способности НФ мем-
изучали зависимость величины R НФ мембраны от
браны. Это связано, по-видимому, с увеличением
концентрации солей в исходном растворе. Концен-
степени гидратации ионов при уменьшении кон-
трацию варьировали путем разбавления исходного
центрации электролита и, соответственно, с увели-
раствора дистилированной водой с рН ~6 или рас-
чением эффективного размера ионов. Аналогич-
твором NaОН с рН 12.0 в случае Na3PO4. Концен-
ную зависимость понижения селективности нано-
трацию солей определяли по табличным значениям
фильтрационных мембран при увеличении исход-
плотности растворов [8, 9]. Плотность определяли
ной концентрации электролита отмечали авторы
весовым методом путем взвешивания мерной кол-
работы [11].
бы с раствором объемом 100 или 50 см3 на анали-
При рассмотрении зависимости R от концентра-
тических весах с точностью до 0.0001 г.
ции солей натрия и калия с анионами различного
Кроме вышеперечисленных солей определяли
заряда (рис. 2) прослеживается четкая закономер-
задерживающую способность НФ мембраны по
ность: при увеличении заряда аниона повышается
154
В. О. Каптаков и др.
имеющимся данным о том, что НФ мембраны об-
ладают большей задерживающей способностью по
отношению к многозарядным ионам по сравнению
с однозарядными независимо от знака заряда [12,
13]. Предполагается, что данный эффект связан с
увеличением вклада электростатического взаимо-
действия иона с заряженной поверхностью мем-
браны, а также с повышением степени гидратации
иона при увеличении его заряда. Различия в степе-
ни задержания ионов с одинаковым зарядом связа-
ны, по-видимому, с разной степенью гидратации, а
также со специфической адсорбцией ионов на по-
верхности мембраны [7].
Рис. 1. Зависимость задерживающей способности (R) НФ мем-
браны по солям различных щелочных металлов и аммония. 1 -
На рис. 3 приведена зависимость задерживаю-
LiNO3, 2 - NaNO3, 3 - NaCl, 4 - KCl, 5 - NН4NO3, 6 - CsNO3
щий способности НФ мембраны от pH в растворе
10 г/дм3 NaNO3.
Приведенные результаты показывают, что в ди-
апазонах рН 2.0-5.5 и 7.5-13.0 задерживающая спо-
собность мембраны остается постоянной (R ~10-
12%). В узкой области рН 5.5-7.5 задерживающая
способность снижается примерно в 2 раза (R ~5%).
Данное явление связано, по-видимому, с достиже-
нием в данном диапазоне рН изоэлектрической
точки поверхности мембраны. В этой области рН
поверхность мембраны становится незаряженной,
при этом за счет снижения эффекта электростати-
ческого отталкивания и уменьшения потенциала
Доннана облегчается ионный транспорт сквозь
Рис. 2. Зависимость задерживающей способности (R) НФ мем-
мембрану [14].
браны по различным солям натрия и калия. 1 - NaNO3, 2 -
Na2SO4, 3 - Na3PO4, 4 - K3Fe(CN)6, 5 - K4Fe(CN)6
В связи с тем что соли борной кислоты доста-
точно часто содержатся в составе ЖРО, в частно-
сти, в кубовых остатках АЭС ВВЭР, было изучено
поведение при нанофильтрации различных борсо-
держащих анионов. Известно [15], что при нейтра-
лизации борной кислоты гидроксидами щелочных
металлов образуются анионы следующего состава:
В5О–, НВ5О92-, В4О72- и ВО2-. Сама борная кислота
вследствие ее малой диссоциации в водных раство-
рах находится в основном в виде нейтральных мо-
лекул.
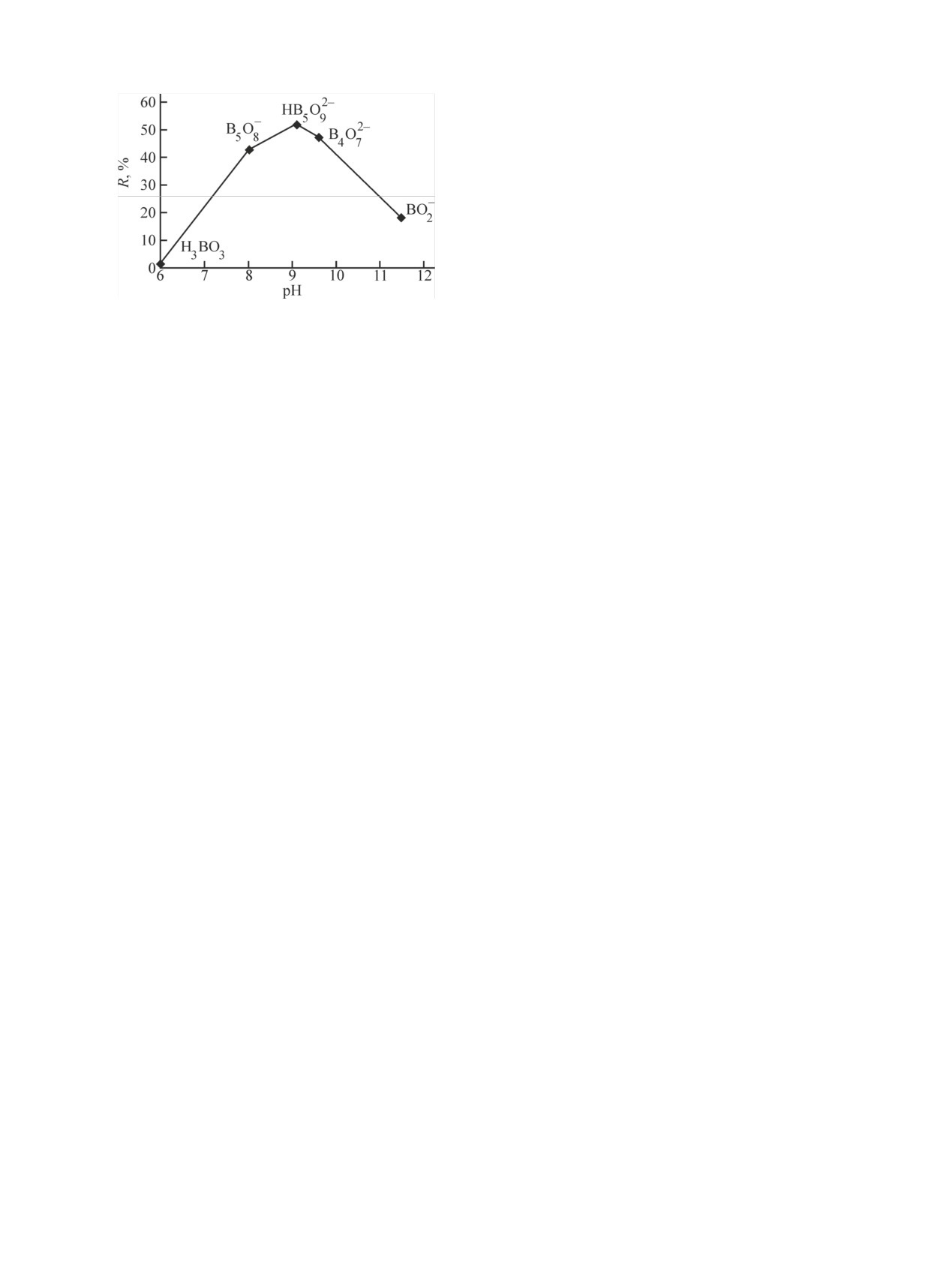
Зависимость задерживающей способности НФ
Рис. 3. Зависимость задерживающей способности (R) НФ мем-
браны по NaNO3 от pH раствора.
мембраны по борной кислоте и различным борсо-
держащим анионам от pH представлена на рис. 4.
Из представленного рисунка видно, что нейтраль-
задерживающая способность НФ мембраны. Наи-
ные молекулы борной кислоты практически не за-
более ярко эта закономерность прослеживается при
держиваются НФ мембраной. По мере нейтрализа-
переходе от однозарядных (NO–) к двух- (SO2-) и
ции Н3ВО3 происходит образование крупных поли-
трехзарядным [PO3-, Fe(CN)63-] анионам в раство-
ядерных анионов, содержащих 4-5 атомов бора,
рах с концентрацией солей менее 25 г/дм3. Разница
которые значительно лучше задерживаются мем-
в задерживающей способности трех- и четырехза-
браной (R ~45-50%). При полной нейтрализации
рядных [Fe(CN)64-] анионов прослеживается только
борной кислоты образуются однозарядные анионы
в области высоких концентраций (более 50 г/дм3).
BO–, которые относительно слабо задерживаются
Наблюдаемые явления в целом соответствуют
НФ мембраной (R ~20%).
Поведение солей щелочных металлов и аммония при нанофильтрации их водных растворов
155
[3] Милютин В. В., Некрасова Н. А., Каптаков В. О. // Радио-
химия. 2016. Т. 58, N 1. С. 30-33.
[4] Брык М. Т., Нигматулин Р. Р. // Химия и технология во-
ды. 1995. Т. 17, N 4. С. 375-396.
[5] Al-Rashdi B. A. M., Johnson D. J., Hilal N. // Desalination.
2013. Vol. 315. Р. 2-17.
[6] Pérez-González A., Ibáñez R., Gómez P. et al. // J. Membr.
Sci. 2015. Vol. 473. P. 16-27.
[7] Милютин В. В., Некрасова Н. А., Каптаков В. О. // Радио-
химия. 2016. Т. 58, N 6. С. 552-555.
[8] Рабинович В. А., Хавин З. Я. Краткий химический спра-
вочник: Справ. изд. / Под ред. А. А. Потехина и А. И.
Ефимова. Л.: Химия, 1991. 3-е изд. 432 с.
[9] Новый справочник химика и технолога. Химическое рав-
Рис. 4. Зависимость задерживающей способности (R) НФ мем-
новесие. Свойства растворов. СПб.: Профессионал, 2004.
браны от pH по борной кислоте и различным борсодержащим
998 с.
анионам.
[10] Шарло Г. Методы аналитической химии. М.: Химия,
1969. Ч. 2. 1206 с.
Таким образом, метод нанофильтрации перспек-
[11] Garcia F., Ciceron D., Saboni A., Alexandrova S. // Sep. Pu-
rif. Technol. 2006. Vol. 52. P. 196-200.
тивен для селективного отделения неактивных со-
[12] Yaroshchuk A. E. // Membr. Technol. 1998. Vol. 100. P. 9-
лей щелочных металлов - основной солевой со-
12.
ставляющей жидких радиоактивных отходов.
[13] Голованева Н. В. Особенности механизма и влияние ос-
новных технических параметров на характеристики нано-
фильтрационных мембран: Дис
к.т.н. М., 2015. 156 с.
Список литературы
[14] Савицкая Т. А., Котиков Д. А., Шичкова Т. А. Коллоидная
химия: строение двойного электрического слоя, получе-
[1] Рябчиков Б. Е. Современная водоподготовка. М.: ДеЛи
ние и устойчивость дисперсных систем. Пособие для сту-
плюс, 2013. 680 с.
дентов химического факультета. Минск: БГУ, 2011. 82 с.
[2] Ершов Б. Г., Гелис В. М., Милютин В. В. и др. // Вопр.
[15] Немодрук А. А., Каралова З. К. Аналитическая химия
радиац. безопасности. 2009. N 4. С. 28-38.
бора. М.: Наука, 1964. 285 с.