ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 6, с. 866-876
УДК 547.246
ВЗАИМОДЕЙСТВИЕ ЭФИРАТА ТРИХЛОРГЕРМАНА
И ТРИМЕТИЛГЕРМАНА С 1,3-ДИВИНИЛ-1,1,3,3-
ТЕТРАМЕТИЛ-1,3-ДИСИЛОКСАНОМ
© 2020 г. В. Г. Лахтинa, А. И. Благушинаa,*,
Н. В. Ушаковb,
И. Б. Сокольскаяa,
И. А. Семяшкинаa, Д. А. Ефименкоa, И. А. Грицковаc, Н. Г. Комаленковаa,
П. А. Стороженкоa
a Государственный научно-исследовательский институт химии и технологии элементоорганических соединений,
ш. Энтузиастов 38, Москва, 105118 Россия
b Институт нефтехимического синтеза имени А. В. Топчиева Российской академии наук, Москва, 199911 Россия
c МИРЭА - Российский технологический университет, Институт тонких химических технологий
имени М.В. Ломоносова, Москва, 119454 Россия
*e-mail: n_blag@list.ru
Поступило в Редакцию 19 января 2020 г.
После доработки 19 января 2020 г.
Принято к печати 27 января 2020 г.
Изучено влияние соотношения исходных реагентов тетраметилдисилоксан-тетрахлорид германия-
диэтиловый эфир на строение и реакционную способность образующихся комплексов трихлоргермана c
эфиром. Исследована возможность проведения реакции 1,3-дивинил-1,1,3,3-тетраметил-1,3-дисилоксана
с полученными эфиратами. Реакция гидрогермилирования 1,3-дивинил-1,1,3,3-тетраметил-1,3-диси-
локсана триметилгерманом в присутствии катализатора Карстедта высокоселективна, проходит исклю-
чительно против правила Марковникова. Получены оба продукта гидрогермилирования - по одной и по
обеим двойным связям дивинилтетраметидисилоксана
Ключевые слова: эфират, трихлоргерман, 1,1,3,3-тетраметил-1,3-дивинил-1,3-дисилоксан, четыреххло-
ристый германий, винильные группы, силоксаны
DOI: 10.31857/S0044460X20060062
Трихлоргерман легко гидрогермилирует оле-
ся двойному гермилированию, и реакция идет по
фины нормального строения (линейные, нераз-
пути обычного гермилирования [3]. В отличие от
ветвленные) при обычной температуре или при
эфирата трихлоргермана триметилгерман легко
слабом нагревании без катализатора [1, 2]. Реак-
реагирует с винилсиланами [4].
ция может идти по двум направлениям: по пути
Имея в виду крайне низкую реакционную спо-
гидрогермилирования и по пути двойного герми-
собность незамещенных двойных связей в реакции
лирования [3]. В присутствии простых эфиров, т.
гидрогермилирования, в частности при гидрогер-
е. когда реагентом является комплекс трихлоргер-
милировании эфиратом трихлоргермана винил-
мана с эфиром, он взаимодействует только по пути
силанов, и высокую реакционную способность
двойного гермилирования [1]. С олефинами, име-
триметилгермана в этих реакциях [4], мы изучили
ющими разветвленное строение, т.е. с простран-
возможность селективного гидрогермилирования
ственно экранированной двойной связью, эфират
винильных групп, связанных с атомами кремния в
трихлоргермана реагирует иначе. В присутствии
силоксановых структурах, с целью оценки устой-
трет-бутильной (в углеродном аналоге триме-
чивости силоксановых связей Si-O-Si в присут-
тилвинилсилана) и четырех метильных групп (в
ствии высокореакционноспособной связи Ge-H. В
тетраметилэтилене) двойная связь не подвергает-
качестве винилзамещенного силоксана для иссле-
866
ВЗАИМОДЕЙСТВИЕ ЭФИР
АТА ТРИХЛОРГЕРМАНА И ТРИМЕТИЛГЕРМАНА
867
слабое поле (13.2-13.4 м. д.), в то время как сигна-
Схема 1.
лы метиленовых и метильных групп эфира смеще-
ны в сильное поле (3.3 и 1.1 м. д. соответственно).
дования гидрогермилирования эфиратом трихлор-
Кроме того, показатель преломления образца А
германа и триметилгерманом использовали
ниже (nD20 1.491), чем образца Б (nD20 1.545). Если
симметричный дивинилтетраметилдисилоксан -
образец А хорошо растворим в дейтерохлорофор-
1,3-дивинил-1,1,3,3-тетраметил-1,3-дисилоксан 1.
ме, то при добавлении CDCl3 к образцу Б сразу
Взаимодействие диоксанового комплекса
выпадает ярко-желтый осадок. Поэтому для сня-
дихлоргермилена C4H8O2·GeCl2 с метилсилокса-
тия спектров ЯМР 1Н образцы эфиратов раство-
нами протекает по нескольким направлениям: (1)
ряли в ДМСО-d6. При дальнейшем увеличении в
внедрение :GeCl2 по связи Si-O, (2) внедрение
исходной смеси количества тетраметилдисилокса-
:GeCl2 по связи С-Н, (3) обмен атомов хлора у
на осадок субхлоридов германия выпадал уже на
германия на метильные группы [5, 6]. В отличие
стадии получения эфиратного комплекса.
от комплекса C4H8O2·GeCl2, являющегося источ-
По-разному реагируют образцы комплекса А и
ником дихлоргермилена, эфират трихлоргермана
Б с соединением 1. При взаимодействии с образ-
(Cl3GeH·2Et2O) в зависимости от среды и приро-
цом А образуется легкая белая взвесь, и на протя-
ды реагентов может диссоциировать по двум на-
жении всего синтеза и последующей разгонки про-
правлениям, а именно выступать и как источник
дуктов реакции желтый осадок не выпадает. При
дихлоргермилена, и как гидрогермилирующий ре-
добавлении же соединения 1 к образцу Б мгновен-
агент (схема 1).
но выпадает ярко-оранжевый осадок субхлоридов
Комплекс трихлоргермана с эфиром получали
германия.
по известной методике [7], которая заключается в
Для эфирата трихлоргермана предложена струк-
смешивании тетраметилдисилоксана, четыреххло-
турная формула [Et2O→H←OEt2]+GeCl3- [8, 9].
ристого германия и диэтилового эфира в соотно-
По-видимому, при соотношении исходных реаген-
шении 1:1:2. Реакционная смесь расслаивается,
тов тетраметилдисилоксан-GeCl4 >0.75:1 восста-
нижний желтый маслянистый слой представляет
новление GeCl4 не ограничивается первой стадией,
собой эфират трихлоргермана 2Et2O·HGeCl3 [7].
а идет дальше с образованием нестойкого комплек-
Состав и строение комплекса, полученного не-
са [Et2O→H←OEt2]GeCl2[Et2O→H←OEt2] - эфи-
посредственно из трихлоргермана и диэтилового
рата дихлоргермана, в котором GeCl2 за счет эфира
эфира, были установлены ранее [8, 9].
находится в жидкой фазе, но при контакте с други-
ми реагентами данный комплекс сразу распадает-
При получении эфирата трихлоргермана по
ся и выпадает осадок субхлоридов германия.
методике [7] нами было обнаружено, что желтая
окраска нижнего слоя сохраняется лишь при соот-
При взаимодействии образца А с соединением
ношении реагентов 0.5-0.75:1:2, а при соотноше-
1 в реакционной смеси (опыт а), как уже было упо-
нии 1:1:2 изначально желтый цвет нижнего слоя
мянуто, не наблюдалось выпадения желтого осадка
изменяется на светло-красный. Соотношение ин-
субхлоридов германия. После отгонки эфира при
тегральных интенсивностей протонов групп GeH,
атмосферном давлении вакуумной разгонкой уда-
CH2, CH3 в спектрах ЯМР 1Н в обоих случаях
лось отогнать лишь небольшое количество жидкой
примерно одинаково (1:8:12 соответственно), что
фракции (~20 мас% от всей реакционной массы
соответствует комплексу 2Et2O·HGeCl3. Данные
без учета эфира). По данным хромато-масс-спек-
ЯМР показывают, что входящие в полученные
трометрического анализа, эти фракции состоят из
комплексы молекулы эфира равноценны. Тем не
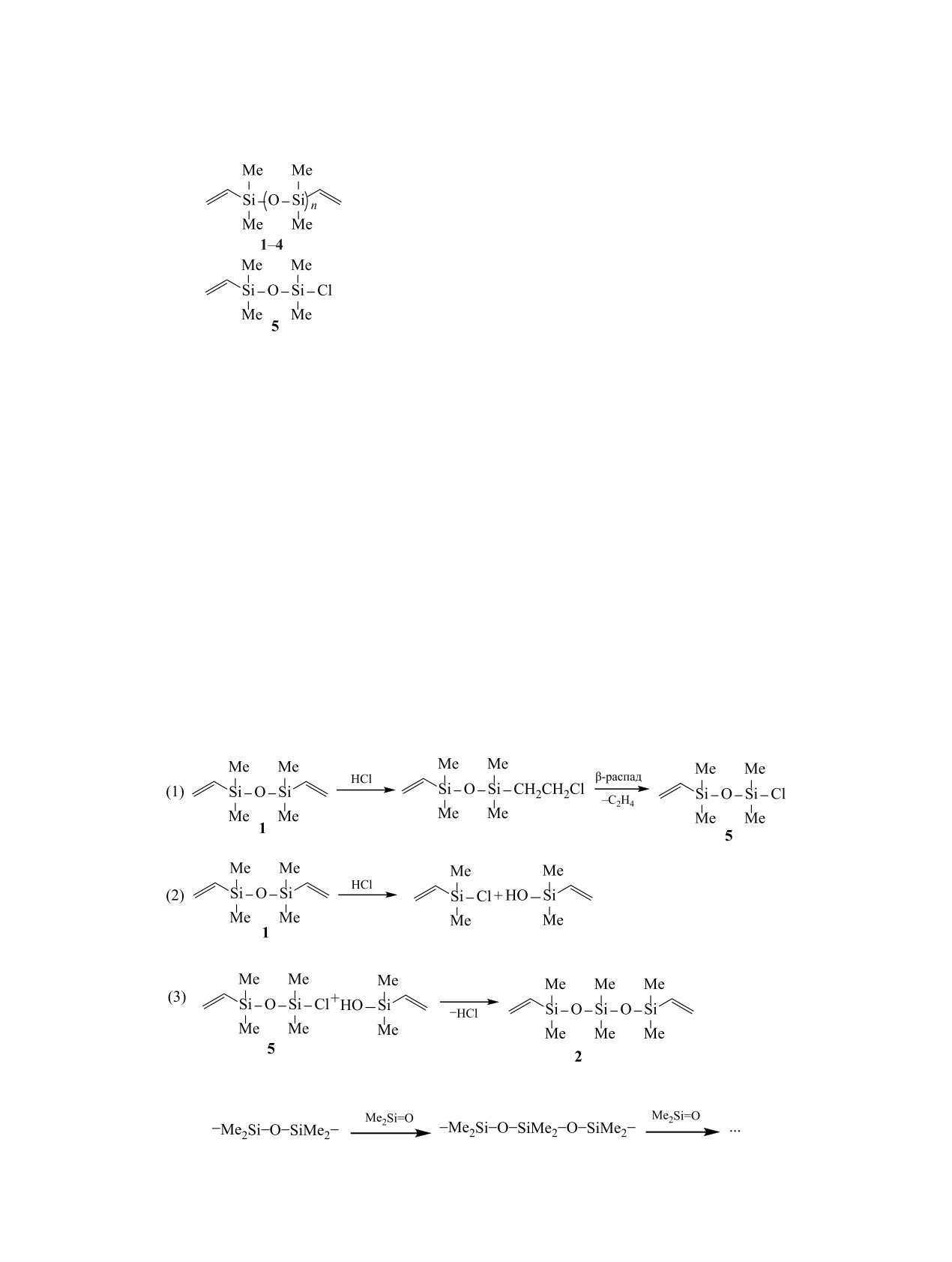
α,ω-дивинилпроизводных олигодиметилсилокса-
менее, образцы комплекса А и Б существенно раз-
нов 1-4 (от исходного дисилоксана 1 до пентаси-
локсана 4) и соединения 5, образовавшегося при
личаются: в спектре образца А гермильный водо-
замене винильной группы на хлор в исходном дис-
род имеет химический сдвиг при ~10.5-10.6 м. д.,
а сигналы эфира (квартет и триплет групп СН2 и
илоксане 1 (схема 2).
СН3) находятся при 3.9 и 1.6 м. д., а в спектре об-
Можно предположить, что образец комплекса
разца Б сигнал гермильного водорода смещен в
А диссоциирует на гермиленхлорид и хлористый
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
868
ЛАХТИН и др.
изучении взаимодействия эфирата трихлоргер-
Схема 2.
мана с этиленом установлено, что образующийся
полимер имеет строение [-СН2СН2GeCl2-]n [8, 9].
Cудя по многочисленным сигналам в спектре ЯМР
1Н, полученный нами кубовый остаток не являет-
ся полимером упорядоченного строения, а пред-
ставляет собой смесь олигомеров и полимеров,
содержащих звенья
[-OSiMe2СН2СН2GeCl2-],
[-OSiMe2GeCl2OSiMe2-], [-OSiMe2-] и т. д., в раз-
личных сочетаниях и соотношениях. Сигналы ви-
водород, который in statu nascendi реагирует по
нильных групп при 5.7-6.2 м. д. в спектре ЯМР 1Н
двойной связи (электрофильное присоединение
свидетельствуют об образовании в данной реак-
с последующим β-распадом) и по связи Si-O-Si,
ции неотделяемых перегонкой высокомолекуляр-
приводя к образованию всех идентифицированных
ных силоксанов с концевыми винильными группа-
соединений. На схеме 3 представлены возможные
ми (соотношение интегральных интенсивностей
реакции (1-3), протекающие в реакционной смеси
протонов в группах Ме, СН2, СН=СН2 16.4:4.1:1).
(вариант а).
При проведении аналогичной реакции соеди-
Можно предположить, что наращивание си-
нения 1 с образцом Б сразу выпадал ярко-желтый
локсановой цепи протекает через образование и
осадок субхлоридов германия, и после отделения
последующее внедрение в связь Si-O-Si диме-
осадка из жидкой фазы выделить вакуумной раз-
тилсиланона Me2Si=O [5, 6] (вариант б, схема 4).
гонкой продукты реакции не удалось. Спектр ЯМР
Учитывая присутствие в реакционной смеси ди-
1Н неперегоняемого вязкого остатка имеет такие
метилвинилхлорсилана и дисилоксана 5, вариант
же сигналы групп Ме, СН2, СН=СН2, как и в опыте
а представляется более вероятным.
с образцом А, но в другом соотношении (12.1:6.1:1).
В спектре ЯМР 1Н кубового вязкого остатка при-
Реакция в отсутствие эфира, т. е. при смеши-
сутствуют сигналы метильных групп (0-0.4 м. д.)
вании и нагревании эквимолярной смеси GeCl4,
и сигналы в интервале 0.9-2.7 м. д., по-видимому,
тетраметилдисилоксана и соединения 1 не проте-
относящиеся к метиленовым звеньям СН2. При
кает. Не наблюдалось никаких превращений и при
Схема 3.
Схема 4.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
ВЗАИМОДЕЙСТВИЕ ЭФИР
АТА ТРИХЛОРГЕРМАНА И ТРИМЕТИЛГЕРМАНА
869
Схема 5.
последующем прибавлении эфира к смеси указан-
тов реакции и вязкую смесь высокомолекулярных
ных реагентов.
олигомеров.
Для выяснения возможности взаимодействия
Фракция жидких продуктов реакции (~20%)
соединения 1 с образцом А в момент образования
содержала, по данным хромато-масс-спектроме-
последнего был поставлен опыт б, в котором сое-
трии, около 20 соединений, представляющих со-
динение 1 к смеси реагентов (GeCl4, тетраметил-
бой смесь диметилсилоксанов с различным соче-
дисилоксан, эфир) добавляли сразу после начала
танием концевых групп SiMe2CH=CH2, SiMe2H,
образования комплекса. Результаты этого опы-
SiMe3, а также циклосилоксанов. В составе этой
та существенно отличались от вышеописанного
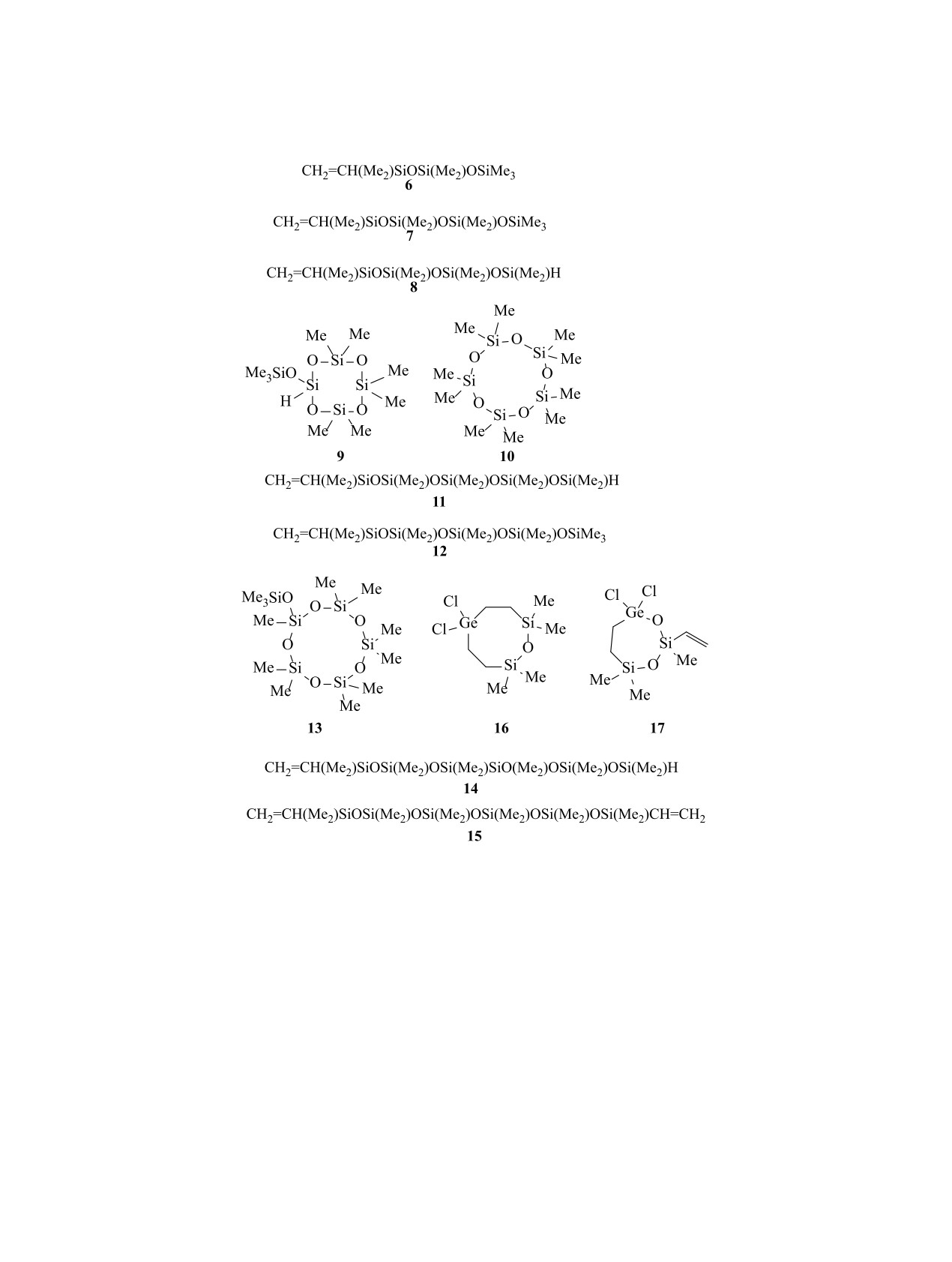
смеси были идентифицированы 15 соединений, из
опыта а с образцом А. Реакционная смесь была
которых 4 были получены и в опыте а (2-5), и два
разделена на две части: перегоняемую в вакууме
минорных (менее 0.3%) циклических силоксана,
(до 140°С при 4 мм рт. ст.) смесь жидких продук-
имеющих в гетероцикле дихлоргермильное звено
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
870
ЛАХТИН и др.
Схема 6.
(16, 17). Более глубокое превращение исходного
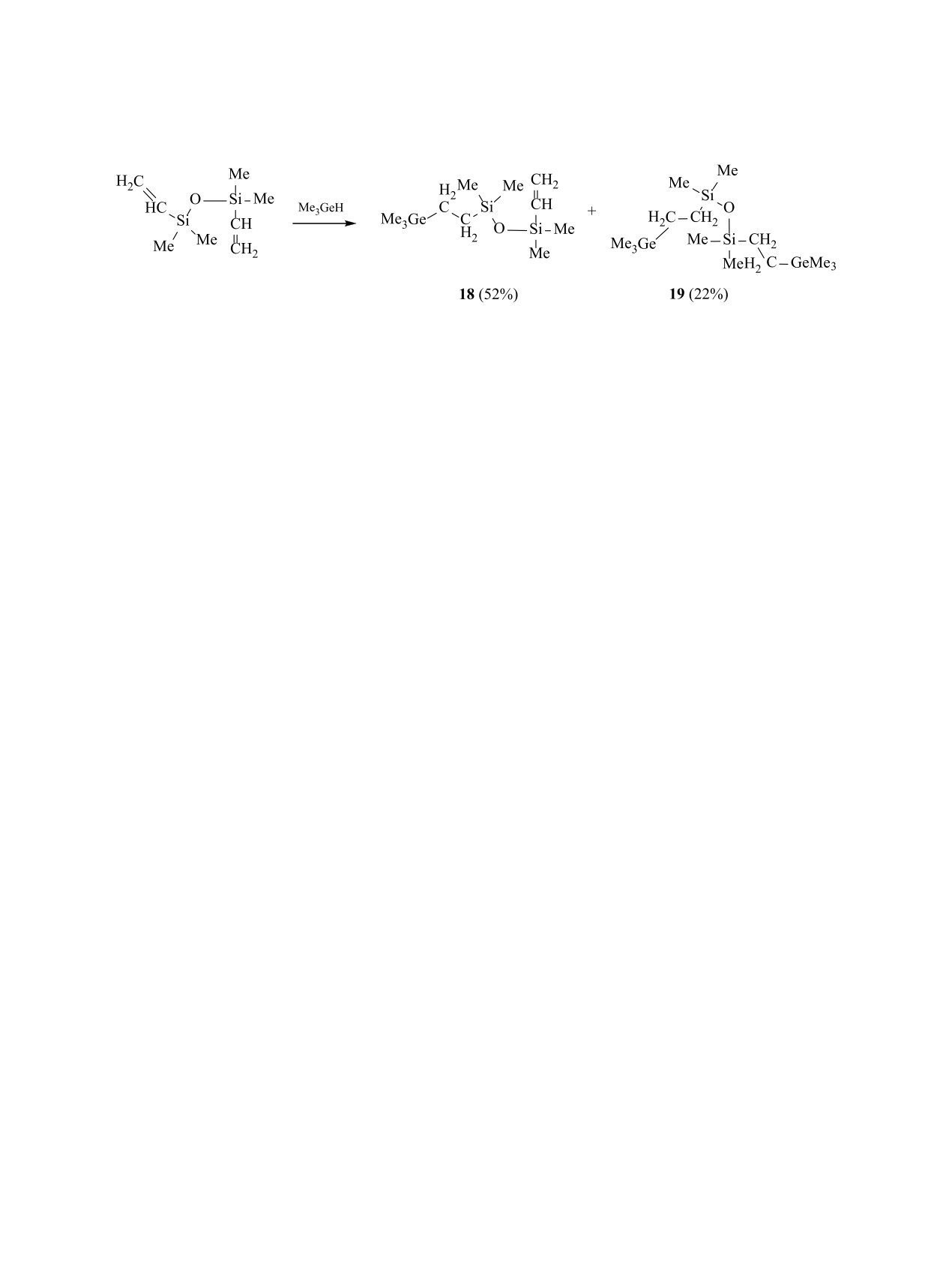
В реакционной смеси присутствуют продукты 18
соединения 1 во опыте б обусловило преимуще-
и 19 однократного и двойного присоединения (со-
ственное образование гексасилоксановых произ-
ответственно 52 и 22% в расчете на триметилгер-
водных. На схеме 5 представлены идентифици-
ман, схема 6).
рованные соединения, образовавшиеся только в
Продукты реакции идентифицированы при
опыте б. Образование силоксанов с концевыми
помощи ЯМР 1Н и хромато-масс-спектрометрии.
группами SiMe2H объясняется присутствием в ре-
Присоединение триметилгермана протекает ис-
акционной смеси тетраметилдисилоксана, продук-
ключительно против правила Марковникова. Ана-
ты уплотнения которого были идентифицированы
лиз ГЖХ показал отсутствие продуктов расще-
ранее [7].
пления связей Si-O-Si. В отсутствие катализатора
Так как в спектре ЯМР 1Н эфирата HCl в
реакция не идет.
ДМСО-d6 химический сдвиг протона наблюдает-
В масс-спектрах синтезированных соедине-
ся при 12.8 м. д., т. е. в той же слабопольной об-
ний, как и в масс-спектрах большинства силок-
ласти, что и химические сдвиги протона у атома
санов, отсутствует молекулярный ион (кроме
германия в эфиратах трихлоргермана, можно было
трисилоксана 2, имеющего молекулярный ион ин-
предположить, что в образовании силоксанов уча-
тенсивностью 1.2%). Однако именно в масс-спек-
ствует именно эфират HCl. Однако специально по-
тре соединения 2 максимален по интенсивности и
ставленные опыты показали, что взаимодействие
по массе ион [M - CH3]+, образующийся при отще-
соединения 1 с 2С2Н5О·НCl не приводит к обра-
плении метильного заместителя, в то время как в
зованию силоксанов, а при взаимодействии сое-
масс-спектрах соединений 3 и 4 его интенсивность
динения 1 с сухим HCl, как показал анализ ГЖХ,
не превышает 15% полного ионного тока. Один из
помимо газообразных веществ образуется прак-
каналов фрагментации тетра- и пентасилоксанов
тически только (СН2=СН)Me2SiCl, и лишь в сле-
3 и 4 - отщепление от молекулярного иона кон-
довых количествах обнаружены высококипящие
цевой винилдиметилсилильной группы и двух
силоксаны.
метильных групп [M - Me2SiСН=СН2 - 2CH3]+.
Полученные данные позволяют предположить,
В масс-спектре тетрасилоксана 3 образуется ион
что именно эфираты трихлоргермана способству-
с выгодной шестичленной структурой (аналог
ют наращиванию силоксановой цепи и образова-
гексаметилциклотрисилоксана D3) с винильной
нию α,ω-дивинилзамещенных и других олигоси-
группой, m/z 219 (Iотн 65%). В масс-спектре пен-
локсанов.
тасилоксана 4 при таком расщеплении возни-
Далее нами было изучено взаимодействие со-
кает также выгодный восьмичленный цикличе-
единения 1 с триметилгерманом. Реакцию про-
ский ион (аналог октаметилциклотетрасилоксана
водили в присутствии катализатора Карстедта.
D4) c винильной группой, m/z 393 (Iотн 25.2%).
В обычных условиях при температуре кипения
Циклические ионы (шестичленный из соедине-
смеси соединения 1 и триметилгермана (30-40°С)
ния 3, m/z 207 (Iотн 58.3%), и восьмичленный из
реакция протекает крайне медленно: за 5 ч превра-
соединения 4, m/z 281 (Iотн 19.5%) образуются
щение триметилгермана составляет менее 14%.
при распаде молекулярных ионов путем отще-
Однако в запаянной ампуле при 90°С реакция про-
пления винильной и винилдиметилсилильной
текает со 100%-ной конверсией триметилгермана.
групп [M - СН=СН2 - Me2SiСН=СН2]+. Ион с m/z
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
ВЗАИМОДЕЙСТВИЕ ЭФИР
АТА ТРИХЛОРГЕРМАНА И ТРИМЕТИЛГЕРМАНА
871
207, соответствующий иону, образующемуся из
типлета молекулярного иона с m/z 424, а не пик
гексаметилциклотрисилоксана D3 при отщепле-
m/z 426, соответствующий молекулярной массе,
нии метильной группы, присутствует с малой ин-
посчитанной для 74Ge.
тенсивностью (6.0%) также и в масс-спектре сое-
Таким образом, установлено, что соотношение
динения 4.
исходных реагентов симметричный тетраметил-
Некоторые одинаковые ионы, присутствующие
дисилоксан-GeCl4-Et2О существенно влияет на
в масс-спектрах соединений 3 и 4, различаются ин-
строение и реакционную способность образую-
тенсивностью (например, ион [(СН=СН2)2SiMe]+,
щихся эфиратных комплексов трихлоргермана.
m/z 97, Iотн 27.3% в спектре соединения 3 и Iотн.
Реакции эфиратных комплексов трихлоргермана с
8.9% в спектре соединения 4). Если в масс-спек-
симметричным дивинилтетраметилдисилоксаном
неселективны и протекают с образованием олиго-
тре соединения 4 у иона [СН=СН2SiMe2]+ с m/z 85
силоксанов с винильными и другими концевыми
(Iотн 15.5%), то в масс-спектре соединения 3 этот
группами и полимерных соединений. Триметил-
ион максимален (100%). Высокая интенсивность
герман не реагирует с симметричным дивинил-
иона [Me3Si]+, m/z 73, наблюдается в масс-спек-
тетраметилдисилоксаном в обычных условиях в
трах тетрасилоксана 3 и пентасилоксана 4. В спек-
присутствии катализатора Карстедта, но при ауто-
тре соединения 3 она достигает 91.0%, а в спектре
генном давлении (90°С) происходит полное пре-
соединения 4 максимальна (100%). Дублет ионов
вращение триметилгермана с образованием про-
m/z 179/181 с соотношением интенсивностей 3:1 в
дуктов гидрогермилирования по одной и по двум
масс-спектре соединения 5 свидетельствует о том,
винильным группам.
что в молекуле этого соединения находится один
атом хлора.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Масс-спектры соединений
6-15 (опыт б)
В работе использовали четыреххлористый
имеют определенное сходство с масс-спектрами
германий (ООО «Германий»), 1,1,3,3-тетраметил-
соединений 2-5 (опыт а): молекулярный ион от-
дисилоксан (98%, Acros), 1,3-дивинил-1,1,3,3-те-
сутствует, а ион [M - Me]+ максимален по массе.
траметилдисилоксан (97%, Acros) и диэтиловый
Различия обусловлены главным образом концевы-
эфир (АО «Вектон»). Эти вещества не подвергали
ми группами, например, благодаря группе Si(Me2)
дополнительной очистке.
H возникает ион [M -H]+. Идентификация изомер-
Спектры ЯМР 1H соединений измеряли на спек-
ных германийорганических соединений 16 и 17
трометре Bruker AM-360 при частоте 360 МГц. В
вызывает затруднения, связанные с присутствием
качестве внутреннего стандарта использовали
в молекулах этих соединений трех мультиизотоп-
тетраметилсилан. ГЖХ-Анализ низкокипящих
ных элемента (один атом германия и по два атома
продуктов проводили на хроматографе ЛХМ-72 с
кремния и хлора). Для интерпретации масс-спек-
детектором по теплопроводности в режиме про-
граммирования температуры от 50 до 280°С при
тров этих соединений мы использовали програм-
скорости нагревания 12 град/мин, длина колонки -
му Isotope Distribution Calculator and Mass Spec
2 м, жидкая фаза - 5% SE-30, неподвижная фаза -
Plotter. Расчетное распределение интенсивностей
Chromaton N-AW (0.250-0.315), газ-носитель - ге-
пиков ионов, образовавшихся при отщеплении
лий, скорость газа-носителя - 40 мл/мин, темпе-
метильной группы, и других ионов, содержащих
ратура детектора - 290°С, температура испарите-
эти элементы, соответствует экспериментальному.
ля 300-320°С. Масс-спектры регистрировали на
В экспериментальной части в масс-спектрах этих
хромато-масс-спектрометре Hewlett-Packard HP-
соединений приведены интенсивности всех пиков,
5971 при энергии ионизации 70 эВ. Использова-
характеризующих тот или иной ион. В масс-спек-
ли капиллярную хроматографическую колонку
трах двух продуктов гидрогермилирования соеди-
(0.032×2500 см), неподвижная фаза ДВ-5 (метил-
нения 1 триметилгерманом (по одной и по двум
фенилсилоксановый эластомер, толщина пленки -
винильным группам) присутствуют молекулярные
25 мкм). Анализ проводили в режиме температур-
ионы, которые легко интерпретируются с учетом
ного программирования колонок от 40 до 280°С,
того, что в спектре соединения 1 с двумя атомами
скорость нагревания - 7 град/мин, газ-носитель -
германия максимален по интенсивности пик муль-
гелий (0.8 мл/мин).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
872
ЛАХТИН и др.
Комплекс трихлоргермана с эфиром.
(8.5),
97/98/99
[(СН2=СН)2SiMe]+ (27.3/2.8/2.4),
Образец А. Смешивали расчетные количества те-
85/86/87 [СН2=СНSiMe2] (100.0/8.6/5.0), 73/74/75
траметилдисилоксана, четыреххлористого герма-
[Me3Si]+ (91.0/7.1/4.9), 71(9.6), 59/60/61 [MeOSi]+
ния и диэтилового эфира в мольном соотношении
(53.3/4.1/2.5), 45 [SiOH]+ (11.7), 28 [C2H4]+∙ (19.5),
соответственно (0.5-0.75):1:2. Реакцию проводи-
18 [H2O]+ (5.0).
ли без перемешивания, поддерживая температуру
1,9-Дивинил-1,1,3,3,5,5,7,7,9,9-декаметил-
~50°C. После закипания реакционной смеси внеш-
1,3,5,7,9-пентасилоксан
(4). Масс-спектр, m/z
ний нагрев прекращали и наблюдали (при помощи
(Iотн, %): 393/394/395 [M - CH3]+ (6.7/1.6/0.9),
U-образной трубки, наполненной полиметилси-
305 [M - Me2SiO - SiH]+(5.6), 293/294/295 [M -
локсаном и соединенной с обратным холодиль-
Me2SiСН2=СН - 2CH3]+(25.2/8.3/3.7), 281/282/283
ником) интенсивное выделение газа. Реакционная
[M - СН2=СН - Me2SiСН2=СН]+ (19.5/6.0/2.6),
смесь постепенно разделялась на два слоя. После
207/208/209 [D3 - CH3]+ (6.0/1.0/0.6), 159/160/161
расслоения отделяли нижний светло-желтый мас-
[Me2SiOSiMe2СН2=СН]+
(51.0/7.7/3.8),
лянистый слой эфирата трихлоргермана (А). Вы-
147/148/149 [Me2SiOSiMe3]+ (26.4/4.7/2.2), 85/86/87
ход 70-80%.
[Me2SiСН2=СН]+ (65.5/6.1/3.4), 73/74/75 [Me3Si]+
При соотношении тетраметилдисилоксан:че-
(100.0/9.3/4.7), 59/60/61 [MeSiO]+ (49.7/3.3/1.6), 32
тыреххлористый германий:диэтиловый эфир
=
[O2] (20.2), 28 [C2H4]+∙ (32.5), 18 [H2O]+∙ (9.0).
1:1:2 изначально желтый цвет нижнего слоя изме-
1-Винил-1,1,3,3-тетраметил-3-хлор-1,3-ди-
нялся на светло-красный (комплекс Б).
силоксан (5). Масс-спектр, m/z (Iотн., %): 179/181
Взаимодействие комплекса трихлоргермана
[M - CH3]+ (100.0/35.3), 167/169 [M - СН2=СН]+
с эфиром и 1,3-дивинил-1,1,3,3-тетраметилди-
(17.2/7.5), 159/160/161 [M - Cl]+ (24.0/5.0/2.3),
силоксана (1). К соединению 1 при перемешива-
153/155 [M - CH3 - C2H4]+ (21.3/7.5), 137/139
нии медленно прибавляли образец комплекса А
[СН2=СН(H)OSi(Me2)Cl]+ (8.1/8.4),
133(9.5),
73
(мольное соотношение реагентов 1:1). Наблюдали
[Me3Si]+ (30.9), 59 [MeSiO]+ (21.0), 45 [MeSiH2]+
слабое саморазогревание реакционной массы (до
(7.0),
32
[MeOH]+∙ (8.2),
28
[C2H4]+∙ (23.9),
27
43-45°C). Реакционную массу перемешивали 5 ч
[СН2=СН]+ (8.7).
при 50°C. Эфир отгоняли при атмосферном дав-
б. Соединение 1 добавляли к смеси тетраме-
лении. Продукты реакции выделяли фракционной
тилдисилоксан-GeCl4-эфир (0.5:1:2) сразу после
вакуумной разгонкой. Кубовый вязкий остаток
начала образования комплекса А.
анализировали методом ЯМР.
1-Винил-1,1,3,3,5,5,5-гептаметил-1,3,5-три-
а. К соединению 1 добавляли светло-желтый
силоксан (6). Масс-спектр, m/z (Iотн, %): 233 [M -
маслянистый образец комплекса А.
Me]+ (2.2), 219/220/221 [M - C2H5]+ (100/28.6/15.7),
1,5-Дивинил-1,1,3,3,5,5-гексаметил-1,3,5-
207 [D3 - Me]+ (13.0), 191/192/193 [M - СН2=СН -
трисилоксан (2). Масс-спектр, m/z (Iотн, %): 260
2Me]+ (70.2/19.1/10.2), 190 [M - СН2=СН - 2H2 -
[M]+∙ (1.2), 245/246/247 [M - CH3]+ (100/23.0/12.0),
H]+ (22.5), 147 [Me2SiOSiMe3]+ (9.9), 133/134/135
205/206/207
(38.8/8.0/5.0),
101/102/103
[HSi(Me2)OSiMe2]+ (19.8/3.7/1.0), 119 (3.3),
103
(19/14.6/10.0),
97/98/99
(36.5/5.0/5.2),
73/74/75
[HSi(Me)OSiMe2]+ (12.2), 102 [MeSiOSiMe]+ (12.3),
[Me3Si]+ (81.0/7.9/9.0), 59 [MeOSi]+(60.8). Неин-
89 [Me3SiO]+ (27.1), 85 [СН2=СНSiMe2]+ (38.0),
формативные пики интенсивностью менее
5%
73/74/75 [Me3Si]+ (69.8/10.0/12.0), 72 [CH2SiMe2]+
здесь и далее не приведены.
(25.5),
59/60/61
[HSiMe2]+
(47.2/3.8/4.1),
45
[MeSiH2]+ (28.0), 44 [MeSiH]+ (6.7), 43 [MeSi]+ (9.3),
1,7-Дивинил-1,1,3,3,5,5,7,7-октаметил-
32 [OH]+. (4.0), 28 [C2H4]+∙ (13.6), 27 [CH2=CH]+
1,3,5,7-тетрасилоксан
(3).
Масс-спектр, m/z
(6.2), 18 [H2O]+∙ (8.7).
(Iотн, %): 319/320/321 [M - CH3]+ (13.0/4.0/2.2),
231/232/233
[M
-Me2SiOSiH]+
(12.0/3.1/2.0),
1-Винил-1,1,3,3.5,5,7,7,7-нонаметил-1,3,5,7-
219/220/221
[M
- Me2SiСН2=СН
-
2CH3]+
тетрасилоксан (7). Масс-спектр, m/z (Iотн, %):
(65.0/12.0/7.0),
207/208/209
[M
- СН2=СН
-
281/282/283 [M - Me]+ (100/21.0/14.7), 265 [M -
Me2SiСН2=СН]+
(58.3/10.8/6.5),
203
(10.0),
2Me -2H]+ (11.6), 249 [M - 3Me - 2H]+ (10.0),
193 (12.0), 191 (11.0), 177 (6.0), 133 (10.0), 112
207 [D3 - Me]+ (4.3), 193 [D3 - Me - CH2]+ (17.2),
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
ВЗАИМОДЕЙСТВИЕ ЭФИР
АТА ТРИХЛОРГЕРМАНА И ТРИМЕТИЛГЕРМАНА
873
191 [D3 - Me - CH2 - 2H]+ (10.0), 133 [HSi(Me2)·
45 [MeSiH2]+ (6.0), 27 [CH2=CH]+ (3.6), 18 [H2O]+∙
OSiMe2]+ (16.0), 103 [HSi(Me)OSiMe]+ (2.0), 73
(3.8).
[Me3Si]+ (20.4), 59 [HSiMe2]+ (2.0), 45 [MeSiH2]+
1-Bинил-1,1,3,3,5,5,7,7,9,9,9-ундекаметил-
(2.1), 32 [MeOH]+∙ (1.6), 28 [C2H4]+∙ (7.8), 18 [H2O]+∙
1,3,5,7,9-пентасилоксан (12). Mасс-спектр, m/z
(1.2).
(Iотн, %): 381 [M - Me]+ (0.35), 353 [M - C3H7]+
1-Винил-1,1,3,3,5,5,7,7-октаметил-1,3,5,7-
(0.42),
307
[M
- Me3SiO]+ (5.3),
233/234/235
тетрасилоксан (8). Масс-спектр, m/z (Iотн, %):
[M
- Me3SiOSi(Me2)O]+
(36.0/6.1/3.7),
221
307
[M - H]+ (0.12), 293/294/295 [M - CH3]+
[CH2=CHSi(Me2)OSi(Me2)O]+ (7.8), 207 [D3 - Me]+
(45.1/18.0/10.0),
219/220/221
[M
- Me3SiO]+
(18.1), 159 [CH2=CH(Me2)SiOSMe2]+ (14.7), 147
(37.8/11.2/6.0), 207/208/209 [M - O(Me)2SiVin]+
[Me2SiOSiMe3]+ (5.8), 85/86/87 [CH2=CHSiMe2]+
(61.8/8.5/5.2), 193/194/195 [M - Me2SiCH2=CH -
(41.9/4.8/2.4), 73/74/75 [Me3Si]+ (100/8.0/3.0),
59
2Me]+
(33.7/6.1/3.3),
133/134/135
[H(Me2)
[HSiMe2]+ (14.1), 45 [Me2SiH2]+ (4.1).
SiOSi(Me2)]+
(12.0/1.2/0.7),
85/86/87
1,3,3,5,5,7,7,9,9-Hонаметил-1-триметилсил-
[CH2=CHSi(Me2)]+ (61.8/8.5/5.2), 73/74/75 [Me3Si]+
окси-1,3,5,7,9-циклопентасилоксан (13). Mасс-
(100/9.3/5.1), 59/60/61 [HSiMe2]+ (34.3/3.3/3.0), 45
спектр, m/z (Iотн., %): 429 [M - Me]+ (0.6), 367 [M -
[H2SiMe]+ (13.7), 44 [HSiMe]+ (2.2), 27 [CH2=CH]+∙
MeSiO2 - 2H]+ (1.8), 355/356/357 [M - Me3SiO]+
(4.2), 18 [H2O]+∙ (2.5).
(4.1/0.4/0.1),
341/342/343
[M
- Me3SiOCH2]+
1,1,3,3,5,5-Гексаметил-7-(триметилсилокси)-
(4.1/0.4/0.1),
307
[M
- H(Me)SiOSi(Me2)·
1,3,5,7-циклотетрасилоксан
(9). Масс-спектр,
(OH)2]+ (6.0),
293
[M
- Me2SiOSi(Me)(OH)2]+
m/z (Iотн, %): 341/342/343 [M - Me]+ (64/1.6/0.9),
(6.2),
281/282/283
[M
- OSi(Me2)OSiMe3]+
281/282/283 [M - Me3Si - 2H]+ (50.0/14.3/7.5), 280
(17.2/4.3/1.7), 265 [MeO(Me2)SiOSi(Me2)O]+ (2.2),
(10.4), 267/268/269 [M - Me3SiO]+ (92.7/20.0/11.4),
233/234/235
[(CH2)3Si(Me2)OSi(Me2)OSiMe]+
251
(5.5),
249
(6.2),
207/208/209
[D3
-Me]+
(26.2/4.3/0.7), 221(7.5), 219(6.0), 207/208/209 [D3 -
(16.2/1.7/0.5),
193
(8.1),
191
(8.1), 147/148/149
Me]+ (35.8/7.6/2.3),
159
[Me3SiOSiC3H6]+ (6.7),
[Me3SiOSiMe2]+
(23.8/1.1/0.5),
133/134/135
147/148/149 [Me3SiOMe2]+ (20.0/2.6/0.9), 146 (5.1),
[Me2SiOSi(Me2)H]+ (47.5/6.0/2.0), 73/74/75 [Me3Si]+
133/134/135
[HSi(Me2)OSiMe2]+
(11.0/0.5/0.15),
(100/7.5/4.6),
59/60/61
[Me2SiH]+ (44.0/1.7/1.3),
85/86/87
[Me2SiC2H3]+
(25.0/2.6/0.3),
73/74/75
45/46 [MeSiH2]+ (14.8/0.6).
[Me3Si]+ (100/9.6/4.0), 59 [Me2SiH]+ (10.0), 46 (4.3),
45 [Me2SiH]+ (5.0), 18 [H2O]+∙ (3.9), 15 [Me]+ (3.5).
1,1,3,3,5,5,7,7,9,9-Декаметил-1,3,5,7,9-цикло-
пентасилоксан (10). Масс-спектр, m/z (Iотн, %):
1-Bинил-1,1,3,3,5,5,7,7,9,9,11,11-додекаметил-
355/356/357 [M - CH3]+ (21.3/9.6/5.8), 339 [M - 2Me -
1,3,5,7,9,11-гексасилоксан (14). Mасс-спектр, m/z
H]+ (2.3), 323 [M - MeSiH2 - 2H]+ (1.1), 281 [M -
(Iотн., %): 441 [M - Me]+ (1.2), 367 [M - Me2SiO -
Me3SiO]+ (0.4), 267/268/269 [M - H(Me)SiOSiMe]+
Me]+ (1.5), 341/342/343 [M - CH2=CH - Me2Si -
(31.8/8.0/2.0),
251/252/253
[M
- Me2Si(Et)O]+
OCH2]+ (6.4/1.2/0.4), 325 [M - OSiMe2 - CH2=CH -
(4.2/2.0/0.6), 73/74/75 [Me3Si]+ (100/9.4/4.3),
59
2Me]+ (3.7), 307 [CH2=CH(Me2SiO)3SiMe2]+ (6.1),
[C3H7O]+ (6.0), 45 [H2SiMe]+ (9.7), 44 [SiMe]+ (2.3),
267 (3.9), 233/234/235 [CH2=CH(Me2)Si(OSiMe2)2]+
28 [C2H4]+∙ (1.6), 15 [CH3]+∙ (0.6).
(65.6/10.7/6.3),
221/222/223
[Me2SiOSi(Me2)·
OSiMe3]+ (12.7/2.4/1.7), 207/208/209 [D3 - Me]+
1-Bинил-1,1,3,3,5,5,7,7,9,9-декаметил-
(11.7/1.4/0.8),
159/160/161
[CH2=CH(Me2)Si-
1,3,5,7,9-пентасилоксан (11). Mасс-спектр, m/z
(Iотн, %): 367 [M - Me]+ (2.1), 355 [M - CH2=CH]+ (5.6),
OSiMe2]+ (23.7/1.6/0.6), 147/148/149 [Me2SiOSiMe3]+
(25.7/2.5/1.4), 133 [Me2SiOSi(Me2)H]+ (6.0), 97 (7.3),
341 [M - CH2=CH - CH2]+ (5.6), 325 [M - CH2=CH -
85/86/87 [CH2=CHSiMe2]+ (65.7/5.8/2.1), 73/74/75
2Me]+ (3.6), 293 [M - Me2SiO - Me]+ (7.0), 281
[Me3Si]+
(100/10.0/3.7),
59/60/61
[Me2SiH]+
[M - CH2=CH(Me2)SiO]+ (8.1), 233 [M - H(Me2)·
(27.5/1.8/0.3), 45 [Me2SiH2]+ (7.0), 27 [CH2=CH]+
SiOSi(Me2)O]+ (21.2),
207/208/209
[D3 - Me]+
(4.3), 18 [H2O]+∙ (5.0).
(33.1/6.1/3.0),
159
[CH2=CH(Me2)SiOSi(Me2)]+
(7.0), 147 [(Me2)SiOSiMe3]+ (14.2), 133 [(Me2)SiO·
1,11-Дивинил-1,1,3,3,5,5,7,7,9,9,11,11-додека-
Si(Me2)H]+ (9.1),
85
[CH2=CH(Me2)Si]+ (27.0),
метил-1,3,5,7,9,11-гексасилоксан
(15).
Масс-
73/74/75 [Me3Si]+ (100/6.1/3.7), 59 [Me2SiH]+ (19.0),
спектр, m/z (Iотн, %): 467 [M - Me]+ (4.1), 367/368/369
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
874
ЛАХТИН и др.
[M - CH2=CH(Me2)Si - O - CH2]+ (8.8/4.0/2.0),
HSiC2H4]+ (0.8), 167/168/169/171 [ClGeOSiCH2]+
293/294/295 [M - Me3SiOSi(Me)(CH2=CH)OCH2]+
(100/13.6/36.1/3.0),
160
[CH2(Me2)SiOSi(:CH2)·
(7.7/3.5/2.2), 267 (7.0), 245 [M - OSi(Me2)OSi(Me2)·
OCH2]+∙ (9.3), 145/146/147 [CH2(Me)SiOSi(:CH2)·
OSi(Me2)
-
Me]+
(13.7),
233/234/235
OCH2]+∙ (51.5/9.0/4.0), 103/105/107/109/111 [GeCl]+
[CH2=CH(Me)2SiOSi(Me2)OSiMe2]+ (49.3/8.4/5.0),
(5.0/10.1/11.0/12.1/4.0), 102 (4.0), 101 (4.2), 93/95
[Me2SiCl]+
(13.7/4.5),
85/86
[Me2SiCH2=CH]+
221/222/223
[Me2SiO
- Si(Me2)OSiMe3]+
(7.8/3.2), 87/88/89 [Me2SiEt]+ (8.0/1.0/2.0), 73/74/75
(10.4/2.4/1.7),
205
(6.0),
191
(5.0), 159/160/161
[Me3Si]+ (67.0/5.7/4.9), 72 [Me2SiCH2]+∙ (19.1), 43
[CH2=CH(Me2)Si
- OSi(Me2)]+
(32.1/6.2/2.0),
[MeSi]+ (17.1), 32 [MeOH]+ (3.5), 28 [C2H4]+∙ (5.0),
147/148/149
[Me2SiOSiMe3]+ (27.7/4.1/1.8),
133
27 [C2H3]+ (11.1), 18 [H2O]+∙ (8.5).
[HSi(Me2)OSiMe2]+ (8.1), 131 (4.2), 97 (7.6), 85/86/87
в. При взаимодействии образца комплекса Б c
[CH2=CHSi(Me2)]+ (74.3/8.0/3.8), 73/74/75 [Me3Si]+
соединением 1 выпадал желтый осадок. После от-
(100/9.0/2.3), 59/60/61 [HSiMe2]+ (39.8/3.8/1.1), 45
деления осадка выделить при помощи вакуумной
[Me2SiH2]+ (11.5), 27 [CH2=CH]+ (5.5), 18 [H2O]+∙ (5.5).
разгонки жидкие продукты реакции не удалось.
1,1,3,3-Тетраметил-6,6-дихлор-2-окса-1,3-ди-
Эфират HCl. В трехгорлую колбу помещали
сила-6-гермациклогептан
(16).
Масс-спектр,
расчетное количество диэтилового эфира. Через
m/z (Iотн,
%):
313/315/316/317/318/319/320/321
эфир с помощью капилляра пропускали газообраз-
[M
- Me]+
(7.7/16.2/8.3/23.7/6.0/14.1/5.1/6.
ный HCl. Реакцию проводили без перемешивания
0),
299/301/302/303/304/305/306/307
[M
-
и без подогрева. При пропускании HCl через эфир,
Et]+
(5.6/10.2/(13.8/9.7/11.5/14.5/3.0/13.8/
наблюдалось самопроизвольное повышение тем-
9.0/9.3),
285/287/288/289/290/291/292/293
[M
-
пературы на 11°С. После прекращения разогре-
C3H7]+
(11.8/24.5/12.0/31.6/15.7/19.5/4.1/9.2),
вания подачу газа прекращали. Продукт реакции
257/259/260/261/262/263/264/265
[MeSiCH2CH2]+
идентифицировали методом ЯМР 1Н.
(5.4/10.0/4.5/16.0/4.1/10.1/1.7/2.4),
207/208/209
Взаимодействие соединения 1 с эфиратом
[D3 - Me]+ (8.7/2.0/0.4), 179/181 [ClGe(C2H3)C3H7)]+
HCl. К соединению 1 и при перемешивании мед-
(11.0/4.7),
165/167/168/169
[ClGe(CH2)2SiH2]+
ленно прибавляли эфират HCl (мольное соотно-
(8.6/18.3/3.6/5.8),
160/161/162
[CH2(Me2)SiO·
шение реагентов 1:1). Саморазогрева реакционной
Si(Me2)CH2]+
(36.0/6.2/2.0),151/152/153/154/155/
смеси не наблюдалось. После окончания прибав-
156/157
[ClGeCH2SiH2]+
(13.8/9.7/22.2/5.8/6.0/
ления эфирата HCl реакционную массу переме-
2.6/6.7),
145146/147
[CH2(Me2)SiOSi(Me)CH2]+
шивали 3 ч при 30°C. Эфир отгоняли при атмос-
(100/19.5/10.0), 144 [Me2SiOSi(CH2CH)Me]+ (24.0),
ферном давлении. Продукты реакции выделяли
143
[CH2(Me)SiOSi(CH2CH)Me]+ (15.0), 137/139
фракционной вакуумной разгонкой.
[ClGeC2H3]+ (32.8/15.1), 129/130/131/132/133/135
Взаимодействие соединения 1 с сухим HCl.
[GeCH2SiMe]+
(11.0/20.5/73.7/26.0/26.3/5.5),
Через расчетное количество соединения 1 с по-
117/118/119
[GeCH2SiH]+
(44.0/10.4/16.0),
мощью капилляра пропускали газообразный HCl.
116(20.8),
115(9.8),
103/105/107/108/109/110/111
Реакцию проводили без перемешивания с нагрева-
[Cl2Ge]+
(14.0/18.1/27.5/6.8/28.3/5.2/8.4),
93/95
нием до 30°С. Реакционную смесь анализировали
[Me2SiCl]+
(31.8/9.5),
85/86
[Me2SiCH2=CH]+
методом ГЖХ.
(21.8/9.0),
87/88/89
[Me2SiEt]+
(14.8/4.4/6.0),
Взаимодействие триметилгермана с соеди-
73/74/75 [Me3Si]+ (98.0/10.0/11.0), 72 [Me2SiCH2]+
нением 1. В стеклянную ампулу загружали экви-
(49.9), 71 [CH2SiCH2]+∙ (11.2), 59/60/61 [Me3SiO]+
молярную смесь триметилгермана с соединением
(46.0/4.8/2.8), 45 [MeSiH2]+ (39.8), 44 [MeSiH]+
1 и одну каплю катализатора Карстедта. Ампулу
(15.8), 43 [MeSi]+ (17.1), 31 [MeO]+ (6.0), 28 [C2H4]+∙
запаивали и выдерживали 5 ч при 90°С. Затем ам-
(15.3), 27 [C2H3]+ (23.0), 18 [H2O]+∙ (17.1).
пулу вскрывали, реакционную смесь анализирова-
3-Bинил-1,1,3-триметил-5,5-дихлор-2,4-ди-
ли методом ГЖХ и разгоняли в вакууме. Продукты
окса-1,3-дисила-5-гермациклогептан (17). Mасс-
реакции идентифицировали методами ЯМР 1Н и
хромато-масс-спектрометрии.
спектр, m/z (Iотн, %): 317 [M - Me]+ (2.5), 302/304/306
[M
- C2H4]+
(2.8/3.2/2.6),
285/287/289/291
3-Bинил-1,1,3,3-тетраметил-1-(2-триметил-
[M
- C3H7]+ (1.0/3.8/5.0/0.8/3.0),
261
[M
-
гермилэтил)-3-винил-1,3-дисилоксан
(18).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
ВЗАИМОДЕЙСТВИЕ ЭФИР
АТА ТРИХЛОРГЕРМАНА И ТРИМЕТИЛГЕРМАНА
875
Bыход
52% (в расчете на триметилгерман),
2. Миронов В.Ф., Гар Т.К. Органические соединения
т. кип. 210-212°С, nD20 1.4320. Спектр ЯМР 1Н, δ,
германия. М.: Наука, 1967. С. 363.
м. д.: 0.08 с, 0.12 с и 0.16 с (21Н, СН3Si, CH3Ge);
3. Миронов В.Ф., Калинина Л.Н., Гар Т.К. // ЖОХ. 1968.
0.48-0.54 м (2Н, СН2Si), 0.62-0.68 м (2Н, СН2Ge),
Т. 39. Вып. 11. С. 2486.
5.71-6.20 м (3Н, СН=СН2). Масс-спектр, m/z (Iотн,
4. Лахтин В.Г., Князев С.П., Павлов К.В., Гусельни-
%): 306 [M]+· (2.3), 291 [M - Me]+ (12.1), 159/160/161
ков Л.Е., Буравцева Е.Н., Куянцева Н.А., Паршко-
[CH2=CH(Me2)SiOSiMe2]+ (100/18.2/8.6), 147 /148/
ва Л.А., Мидько А.А., Быковченко В.Г., Кисин А.В.,
149
[Me2SiOSiMe3]+
(12.3/2.1/0.4),
145
(10.0),
Чернышев Е.А. // ЖОХ. 2008. Т. 78. Вып. 5. С. 756;
133/134/135
[H(Me2)SiOSiMe2]+
(20.3/3.4/1.7),
Lakhtin V.G., Knyazev S.P., Pavlov K.V., Gusel’ni-
131
[Me2GeVin]+ (28.1),
119
[GeMe3]+ (57.3),
kov L.E., Buravtseva E.N., Kuyantseva N.A., Parshko-
105
(6.0),
103
(7.5),
85
[CH2=CHSiMe2]+ (8.0),
va L.A., Mid’ko A.A., Bykovchenko V.G., Kisin A.V.,
73/74/75 [Me3Si]+ (23.5/3.0/3.2), 59/60/61 [Me2SiH]+
Chernyshev E.A. // Russ. J. Gen. Chem. 2008. Vol. 78.
(23.8/2.1/1.6), 45 [MeSiH2]+ (4.1), 32 [O2]+∙ (1.3), 28
N 5. P. 898. doi 10.1134/S1070363208050101
5. Щербинин В.В., Пушкина О.Ю., Криволапова О.В.,
[C2H4]+∙ (6.3), 18 [H2O]+∙ (1.3).
Быковченко В.Г., Хромых Н.Н., Комаленкова Н.Г.,
1,1,3,3-Тетраметил-1,3-ди-(2-триметилгер-
Чернышев Е.А. // ЖОХ. 2002. Т. 72. Вып. 12. C. 2015;
милэтил)-1,3-дисилоксан (19). Выход 22% (в
Shcherbinin V.V., Krivolapova O.V., Bykovchenko V.G.,
расчете на триметилгерман), т. кип. 240-243°С,
Pushkina O.Yu., Khromykh N.N., Komalenkova N.G.,
nD20 1.4441. Спектр ЯМР 1Н, δ, м. д.: 0.6 с (12Н,
Chernyshev E.A. // Russ. J. Gen. Chem. 2002. Vol. 72.
СН3Si), 0.11 с (18Н, СН3Ge), 0.45-0.51 м (4Н,
N 12. P. 1907. doi 10.1023/A:1023455010746
СН2Si), 0.60-0.66 м (4Н, СН2Ge). Масс-спектр, m/z
6. Щербинин В.В., Криволапова О.В., Быковченко В.Г.,
(Iотн, %): 424/426 [M]+· (1.1/0.4), 409/411 [M - Me]+
Пушкина О.Ю., Хромых Н.Н., Комаленкова Н.Г.,
(1.3/1.0), 277/279 [M - Me2SiOSiMe3]+ (17.2/3.6),
Чернышев Е.А. // ЖОХ. 2001. Т. 71. Вып. 4. С. 581;
147/148/149
[Me2SiOSiMe3]+
(13.6/1.7/0.9),
Shcherbinin V.V., Krivolapova O.V., Bykovchenko V.G.,
145
(13.1),
133
[H(Me2)SiOSiMe2]+ (6.1),
131
Pushkina O.Yu., Khromykh N.N., Komalenkova N.G.,
[Me2GeCH2=CH]+ (6.0),
119
[GeMe3]+ (100),
73
Chernyshev E.A. // Russ. J. Gen. Chem. 2001. Vol. 71.
[Me3Si]+ (21.0), 59 [Me2SiH]+ (3.9), 45 [MeSiH2]+
N 4. P. 540. doi 10.1023/A:1012327017109
(1.2), 28 [C2H4]+∙ (1.7).
7. Миронов В.Ф., Гар Т.К. // ЖОХ. 1975. Т. 45. Вып. 1.
С. 103.
КОНФЛИКТ ИНТЕРЕСОВ
8. Нефедов О.М., Колесников С.П., Шейченко В.И.,
Авторы заявляют об отсутствии конфликта
Шейнкер Ю.Н. // Докл. АН СССР. 1965. Т. 162.
интересов.
№ 3. С. 589.
9. Нефедов О.М., Колесников С.П. // Изв. АН СССР,
СПИСОК ЛИТЕРАТУРЫ
ОХН. 1966. № 2. С. 201; Nefedov O.M., Kolesnikov S.P. //
1. Миронов В.Ф., Джуринская Н.Г., Гар Т.К., Пет-
Bull. Acad. Sci. USSR. Div. Chem. Sci. 1966. Vol. 15.
ров А.Д. // Изв. АН СССР, ОХН. 1962. № 3. С. 460.
P. 187. doi 10.1007/BF00856036
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020
876
ЛАХТИН и др.
Interaction of Trichlorogermane Etherate and Trimethylgermane
with 1,1,3,3-Tetramethyl-1,3-divinyl-1,3-disiloxane
V. G. Lakhtina, A. I. Blagushinaa,*,
N. V. Ushakovb,
I. B. Sokolskayaa, D. A. Efimenkoa,
I. A. Semyashkinaa, I. A. Gritskovac, N. G. Komalenkovaa, and P. A. Storozhekoa
a State Research Institute of Chemistry and Technology of Organoelement Compounds, Moscow, 105118 Russia
b A.V. Topchiev Institute of Petrochemical Synthesis of the Russian Academy of Sciences, Moscow, 199911 Russia
c MIREA - Russian Technological University, Lomonosov Institute of Fine Chemical Technologies, Moscow, 199454 Russia
*e-mail: n_blag@list.ru
Received January 19, 2020; revised January 19, 2020; accepted January 27, 2020
The effect of the ratio of the starting reagents tetramethyldisiloxane-germanium tetrachloride-diethyl ether on
the structure and reactivity of the resulting trichlorogermane etherate complexes was studied. The possibility
of carrying out the reaction of 1,1,3,3-tetramethyl-1,3-divinyl-1,3-disiloxane with the obtained etherates was
investigated. The hydrogermylation reaction of 1,1,3,3-tetramethyl-1,3-divinyl-1,3-disiloxane with trimethylger-
mane in the presence of a Karstedt catalyst was studied. The reaction is highly selective, it proceeds exclusively
against the Markovnikov rule, both hydrogermylation products are obtained - on one and on both double bonds
of tetravinyl disiloxane.
Keywords: etherate, trichlorogermane, 1,1,3,3-tetramethyl-1,3-divinyl-1,3-disiloxane, germanium tetrachloride,
vinyl groups, siloxanes
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 6 2020