БИОФИЗИКА, 2023, том 68, № 5, с. 863-870
МОЛЕКУЛЯРНАЯ БИОФИЗИКА
УДК 543.645.9
ДЕЙСТВИЕ ЭЛЕКТРОХИМИЧЕСКИ АКТИВИРОВАННОГО ВОДНОГО
РАСТВОРА НА РАСТИТЕЛЬНЫЕ ПОЛИСАХАРИДЫ:
ФЕНОМЕНОЛОГИЯ И СПЕКТРОМЕТРИЯ
© 2023 г. А.Г. Погорелов*, #, Л.Г. Ипатова*, А.И. Панаит*,
М.А. Погорелова*, А.А. Гулин**, В.Н. Погорелова*
*Институт теоретической и экспериментальной биофизики РАН,
ул. Институтская, 3, Пущино Московской области, 142290, Россия
**Федеральный исследовательский центр химической физики им. Н.Н. Семёнова РАН,
ул. Косыгина, 4, Москва, 119991, Россия
#Е-mail: agpogorelov@rambler.ru
Поступила в редакцию 07.04.2023 г.
После доработки 12.05.2023 г.
Принята к публикации 07.06.2023 г.
С использованием UV-Vis спектрометрии, времяпролетной масс-спектрометрии вторичных ионов
и сканирующей электронной микроскопии изучено изменение свойств полисахаридов в электро-
химически активированном водном растворе. Показано, что исследуемые растворы полисахаридов
растительного происхождения (агар, растворимый крахмал, пищевой крахмал) подвержены моди-
фикации, направленность которой обусловлена используемой фракцией электрохимически акти-
вированного раствора (католит или анолит). Выявленные особенности могут быть востребованы
при разработке новых способов управления свойствами биологического сырья в технологии произ-
водства пищевых продуктов. Отмечено, что технология электрохимически активированного водно-
го раствора, которую относят к разряду «зеленых», может быть воспроизведена в промышленных
масштабах.
Ключевые слова: электрохимически активированный водный раствор, агар, крахмал, полисахарид,
олигосахар, UV-Vis спектрометрия, масс-спектрометрия вторичных ионов, сканирующая электронная
микроскопия.
DOI: 10.31857/S0006302923050046, EDN: PGOKRQ
активированного водного раствора (ЭХАР). От-
Исходным сырьем для пищевых технологий
метим, что подходы, разработанные на основе
является биологическая матрица, основу которой
ЭХАР, относят к «зеленым» технологиям, так как
составляют органические молекулы, включая по-
воздействие остается экологически безопасным и
лисахариды растительного происхождения. В
не несет техногенной нагрузки.
производственном цикле данный класс макро-
нутриентов, в зависимости от амфифильности,
Принцип получения ЭХАР состоит в накопле-
используют в виде раствора (модифицированный
нии метастабильной фракции воды в области,
крахмал, агар) или суспензии (крахмал). При об-
прилегающей к аноду или катоду электролизера,
работке сырья, а также в процессе получения по-
анолита или католита соответственно [1, 2]. В ин-
луфабрикатов и конечного продукта, вещество
тервале релаксации длительностью до несколь-
преобразуют так, чтобы улучшить его реологиче-
ких дней эти фракции обладают характерными
ские свойства, ускорить или оптимизировать тех-
свойствами [3, 4]. После катодной обработки вод-
нологические процессы, улучшить органолепти-
ный раствор приобретает щелочную реакцию, а
ческие характеристики готовой продукции. Для
его окислительно-восстановительный потенциал
безреагентного управления свойствами пищевых
(ОВП) может снизиться до отрицательных значе-
систем применяют фракции электрохимически
ний, в нем уменьшается содержание растворен-
ного кислорода, но возрастает уровень молеку-
Сокращения: ЭХАР - электрохимически активированный
лярного водорода. Наоборот, в результате анод-
водный раствор, ОВП - окислительно-восстановитель-
ной обработки возрастает до аномально высокого
ный потенциал, ToF-SIMS - масс-спектрометрия вторич-
ных ионов.
значения ОВП раствора, увеличивается его кис-
863
864
ПОГОРЕЛОВ и др.
лотность, а также содержание растворенного кис-
МЕТОДИКА ИССЛЕДОВАНИЯ
лорода.
Подготовка образцов. Для экспериментов бра-
ли артезианскую воду (рН 7.2, ОВП +360 мВ) из
Фракции ЭХАР показали себя в качестве пер-
городского водопровода (г. Пущино Московской
спективных экстрагирующих и гидролизующих
области). На установке «Стел» («Делфин Аква»,
агентов. Например, в области переработки расти-
Россия), рекомендованной для бытового исполь-
тельного сырья разработан метод экстрактивного
зования, получали фракции ЭХАР: католит
получения красителя из кожуры лука в среде ка-
(рН 8.2, ОВП -800 мВ) или анолит (рН 2.2,
толита [5]. Извлечение виннокислых соединений
ОВП +800 мВ). Исследование проводили на трех
из виноградной выжимки в непрерывном потоке
образцах полисахаридов растительного проис-
анолита повышает выход виннокислых соедине-
хождения: растворимый в воде модифицирован-
ний, сокращает длительность процесса и снижает
ный крахмал или агар марки Gelagar (B&V S.R.L.,
потребление энергии [6]. Похожий метод исполь-
Италия), а также нерастворимый в воде пищевой
зован для обработки бурых водорослей, что дела-
крахмал. Из растворимых препаратов готовили
ет более эффективным производство альгиновой
маточный водный раствор, который в пропорции
кислоты и альгината натрия, улучшает санитар-
1 : 4 разводили водой или одной из фракций
но-гигиенические условия и экологическую без-
ЭХАР. Для агара, учитывая его низкую раствори-
опасность, а также упрощает технологические
мость, в маточном растворе весовая концентра-
ция составляла 0.3%, для модифицированного
процессы [7]. Сравнительные исследования по-
крахмала - 2.5%. Полученные растворы изучали
казали, что эффективность экстракции белка из
посредством UV-спектрометрии и молекулярной
абрикоса или муки рапса у электролизной воды
масс-спектрометрии вторичных ионов (ToF-
выше, по сравнению с обычной водой [8, 9].
SIMS).
Схожие процессы описаны для такой сложной
Для пищевого крахмала, нерастворимого в во-
физико-химической системы, как тесто. Показа-
де, препараты готовили следующим образом.
но, что использование католита ускорят набуха-
Одинаковые объемы (27 мл) воды (контроль) или
ние крахмальных зерен, способствуя формирова-
фракций ЭХАР (католит, анолит) добавляли к на-
нию однородной структуры конечного продукта,
веске крахмала (3 г). Полученную взвесь выдер-
живали в течение суток при горизонтальном
увеличению выхода клейковины и количества ад-
встряхивании при комнатной температуре. Затем
сорбированной влаги [10]. В цитируемой работе
частицы крахмала осаждали 15 мин в центрифуге
установлено влияние католита на удельный объ-
при 600 g. Жидкость, полученную над осадком,
ем и пространственную структуру готового про-
анализировали с помощью UV-vis-спектромет-
дукта. Описанные закономерности наблюдали и в
рии и молекулярной масс-спектрометрии. По-
других исследованиях, где для опытных образцов
верхность частиц крахмала, содержащихся в
отмечали изменение цвета, удельного объема,
осадке, исследовали методом сканирующей элек-
текстуры, степени желатинизации и твердости
тронной микроскопии.
[11-13]. Показано, что применение ЭХАР спо-
UV-Vis спектрометрия. Наличие эффекта дей-
собствует интенсификации получения сусла за
ствия ЭХАР оценивали посредством спектромет-
счет более глубокого гидролиза полисахаридов
рии водных растворов полисахаридов (агар, крах-
[14, 15]. При этом обработка сырья анолитом уве-
мал). Для этого регистрировали оптическую
личивает амилолитический эффект за счет акти-
плотность в спектре поглощения образца на дли-
визации фермента амилазы [14, 16].
не волны 225 нм на спектрофотометре UV-
2401PC (Shimadzu, Япония). Растворы крахмала
Таким образом, в области пищевых произ-
дополнительно окрашивали иодитным методом,
водств накоплен значительный эмпирический
что позволило получить в видимой области спе-
опыт использования ЭХАР притом, что механиз-
цифичные спектры поглощения олигосахаров.
мы действия фракций электрохимически активи-
Данную реакцию проводили в среде с избытком
рованного водного раствора на растительные
йода, чему соответствует наличие характерного
полисахариды остаются мало изученными. По-
пика на длине волны 355 нм в спектре поглоще-
этому целью данной работы было сравнительное
ния анализируемого раствора.
исследование in vitro взаимодействия католита и
Времяпролетная масс-спектрометрия вторич-
анолита с крахмалом или агаром, которые пред-
ных ионов. Образцы для масс-спектрометрии по-
ставляют важный класс макронутриентов. Моди-
лучали следующим образом. Капли препарата
фицируя методику подготовки препарата, в экс-
объемом 2 мкл наносили на чистую стеклянную
перименте применили ряд аналитических мето-
подложку, поверхность которой покрыта токо-
дов спектрометрии и сканирующую электронную
проводящей пленкой. После высушивания в
микроскопию.
струе инертного газа образец переносили в каме-
БИОФИЗИКА том 68
№ 5
2023
ДЕЙСТВИЕ ЭЛЕКТРОХИМИЧЕСКИ АКТИВИРОВАННОГО ВОДНОГО РАСТВОРА
865
действия длительностью 70 нс и последующей ре-
гистрации вторичных ионов (~80 мкс) пучок пе-
ремещался в следующую точку поверхности.
Плотность дозы облучения первичными ионами
не превышала 5·1012 ионов/см2. Для оценки раз-
личий между полученными масс-спектрами при-
менили метод главных компонент (РСА - princi-
pal component analysis) [17-19].
Сканирующая электронная микроскопия. Дан-
ный метод применили для визуализации поверх-
ности зерен пищевого крахмала. Образец нерас-
творимого в воде полисахарида, обработанного
водой или фракциями ЭХАР, отмывали дистил-
лированной водой. Каплю (~2 мкл) полученной
суспензии частиц крахмала наносили на поверх-
ность держателя образцов электронного микро-
скопа и сушили в потоке чистого инертного газа
(N2) при комнатной температуре. Затем в среде
аргоновой плазмы на поверхность напыляли слой
платины, используя установку JFC-1600 (JEOL,
Япония). Тонкую структуру рельефа изучали в
сканирующем электронном микроскопе JSM-
6390A (JEOL, Япония) при ускоряющем напря-
жении 20 кВ в режиме вторичных электронов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Спектрометрия водных растворов агара и моди-
фицированного крахмала. Изучали полисахариды
растительного происхождения со свойствами
гидроколлоидов, которые в воде образуют вязкие
растворов. Гидроколлоиды применяют в пище-
вых технологиях в качестве добавок с функциями
загустителей, стабилизаторов и гелеобразовате-
лей. Спектры поглощения водных растворов по-
лисахарида (агар, модифицированный крахмал)
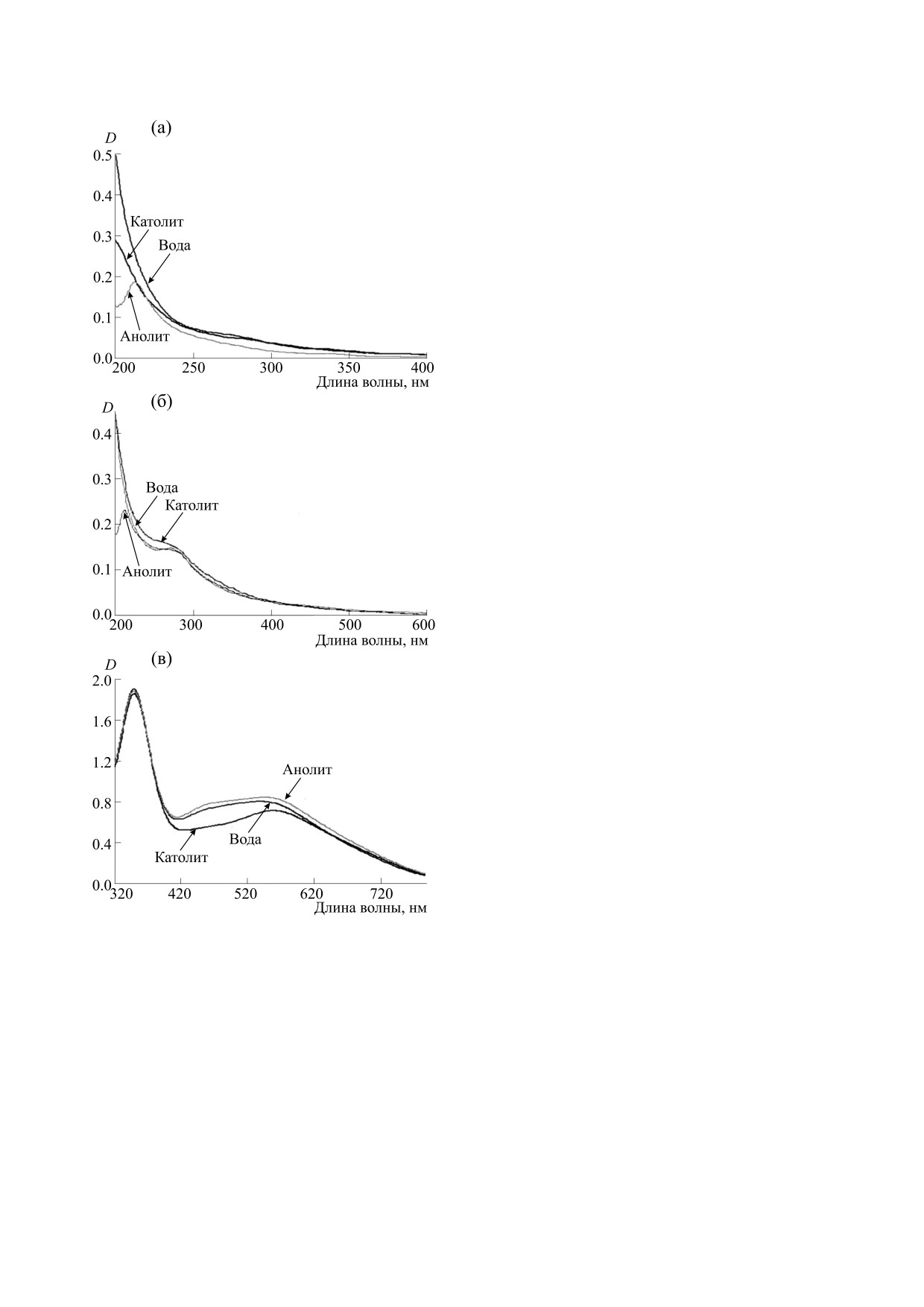
показаны на рис. 1.
По сравнению с раствором в воде, качествен-
ное изменение спектра поглощения обоих поли-
сахаридов наблюдается только в среде анолита
(рис. 1а,б), что характеризует пик в области
225 нм. Отметим, что для агара в растворе католи-
та также наблюдается тенденция к трансформа-
ции спектра (рис. 1а), который соответствует
промежуточному состоянию между контролем и
раствором в анолите. Возможно, завершение пе-
Рис. 1. Спектры поглощения растворов полисахарида
рехода требует более длительного воздействия
растительного происхождения в воде (контроль) или
восстановленной фракцией ЭХАР.
фракциях ЭХАР (анолит, католит): (а) - неспецифи-
ческие UV-спектры агара, (б) - неспецифические UV-
Растворы модифицированного крахмала до-
спектры модифицированного крахмала, (в) - харак-
полнительно окрашивали иодитным методом,
терные спектры раствора модифицированного крах-
мала после окраски олигосахаров посредством иодит-
что позволило получить специфичные спектры
ной реакции.
поглощения в видимой области (рис. 1в). Данную
цветную реакцию проводят на олигосахара с пи-
ком в характерной области 520 нм при условии
ру масс-спектрометра вторичных ионов TOF-
насыщения раствора йодом (пик 355 нм). Значи-
SIMS 5 (ION-TOF GmbH, Германия). Препарат
мое снижение интенсивности характерного спек-
ионизировали пучком первичных ионов Bi3+ с
тра наблюдается только для раствора крахмала в
энергией 30 кэВ, диаметром 200 нм. После воз-
католите (рис. 1в). Учитывая то, что во всех вари-
БИОФИЗИКА том 68
№ 5
2023
866
ПОГОРЕЛОВ и др.
Рис. 2. Результаты ToF-SIMS-анализа образцов агара, приготовленных из раствора полисахарида в воде (контроль) или
фракциях ЭХАР (анолит, католит): (а) - диапазоны молекулярных масс, где везде нижний масс-спектр соответствует
контролю (вода), средний масс-спектр - после обработки католитом, верхний масс-спектр - после обработки аноли-
том; (б) - график счетов в координатах первых двух главных компонент, эллипсами обозначены 95%-е доверительные
интервалы для групп из шести измерений в каждой.
антах исходный маточный раствор модифициро-
выявить пики, вносящие наибольший вклад в это
ванного крахмала разбавляли одинаковым спосо-
различие. Анализ проводили по наиболее интен-
бом, уменьшение содержания олигосахаров мож-
сивным пикам. Эллипсы, ограничивающие на
но объяснить наличием амилолитической
графике область результатов, при условии, что
активности у католита. Дело в том, что модифи-
они не пересекаются, отражают достоверность
цированный крахмал представляет собой смесь
различий в составе сравниваемых образцов с
олигосахаров, фрагментация которых α-амила-
95%-м доверительным интервалом (рис. 2б).
зой или, например, католитом приводит к обра-
Полученные данные (рис. 2б) свидетельствуют
зованию моносахаров и, следовательно, к умень-
о значимом отличии масс-спектра агара в водном
шению интенсивности цветной окраски.
растворе (контроль) от масс-спектров полисаха-
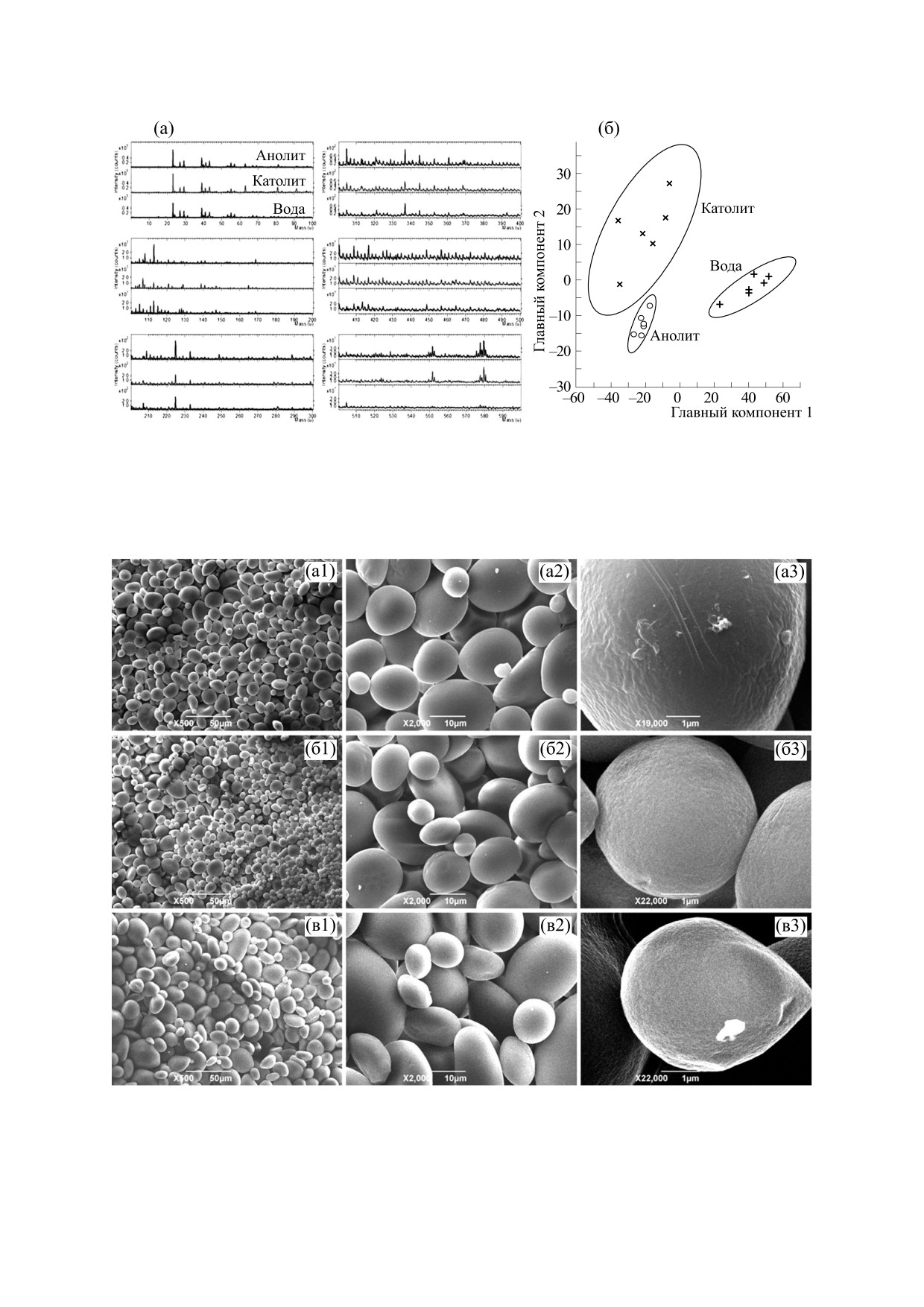
Характерные масс-спектры молекулярного со-
рида, обработанного фракциями ЭХАР. Масс-
става раствора агара в воде, анолите и католите
спектры агара в анолите и католите между собой
приведены на рис. 2а. Для выявления отличий
достоверно не различаются, что соответствует
между образцами проводили анализ методом
тенденции на сближение, отмеченной для UV-
главных компонент. Суть анализа заключается в
спектров (рис. 1а). Характерные масс-спектры
уменьшении размерности матрицы больших дан-
молекулярного состава раствора модифициро-
ных, т. е. n выборок с m массовыми пиками до
ванного крахмала в воде, анолите и католите при-
комбинации нескольких ключевых переменных,
ведены на рис. 3а. Для указанных вариантов с по-
описывающих основные различия (вариацию) в
мощью метода главных компонент проведен
результатах. Уменьшение размерности достигает-
сравнительный анализа данных молекулярного
ся путем линейного преобразования данных в но-
анализа (рис. 3б).
вую систему координат, в которой большую часть
вариации можно описать меньшим количеством
Ситуация для образцов модифицированного
параметров. Таким образом, формируются оси
крахмала (рис. 3) отличается от той, что наблюда-
главных компонент PC1, PC2 и т.д. В большин-
ется для агара (рис. 2). Отметим значимое разли-
стве случаев используются первые две главные
чие в молекулярном составе между фракциями
компоненты, чтобы отображать данные в двух из-
ЭХАР (рис. 3б), что соответствует данным UV-vis-
мерениях (плоскостях) и визуально идентифици-
спектрометрии (рис. 1б). Однако различие между
ровать кластеры связанных экспериментальных
масс-спектрами для образца крахмала в воде и ка-
измерений. Такой способ отображения данных
толите более выражено, по сравнению с тем, что
называется графиком счетов и он показывает, от-
регистрируется на UV-спектрах. Возможно, в
личаются ли образцы или группа образцов в ко-
указанном диапазоне изменение в молекулярном
ординатах PC1-PC2. Соответствующий график
составе, обусловленное обработкой католитом,
показывает различие в масс-спектрах и позволяет
существенно не повлияло на спектральные ха-
БИОФИЗИКА том 68
№ 5
2023
ДЕЙСТВИЕ ЭЛЕКТРОХИМИЧЕСКИ АКТИВИРОВАННОГО ВОДНОГО РАСТВОРА
867
Рис. 3. Результаты ToF-SIMS-анализа образцов модифицированного крахмала, приготовленных из раствора полисаха-
рида в воде (контроль) или фракциях ЭХАР (анолит, католит): (а) - диапазоны молекулярных масс, где везде нижний
масс-спектр соответствует контролю, средний масс-спектр - после обработки католитом, верхний масс-спектр - после
обработки анолитом; (б) - график счетов в координатах первых двух главных компонент, эллипсами обозначены 95%-е
доверительные интервалы для групп из шести измерений в каждой.
рактеристики раствора модифицированного
псевдоферментативной активности и/или ослаб-
крахмала.
ление экстракции материала из зерен крахмала.
Микровзвешивание с помощью кварцевого изме-
Спектрометрия нерастворимого в воде пищевого
рителя сухого остатка в капле (2 мкл) супернатан-
крахмала. Многие виды сырья для пищевой про-
та позволило установить, что относительное
мышленности содержат макронутриенты в не-
уменьшение уровня олигосахаров, растворенных
растворимой форме. В их ряду наиболее пред-
в католите, не обусловлено снижением количе-
ставлены крахмалосодержащие материалы, тех-
ства экстрагированного вещества (рис. 4в). На-
нология подготовки которых предполагает
оборот, в этом случае содержание материала в
обработку водой. В результате чего получают вод-
растворе возросло, имитируя сочетанную актив-
ную суспензию крахмала, которая является объ-
ность α- и β-амилазы.
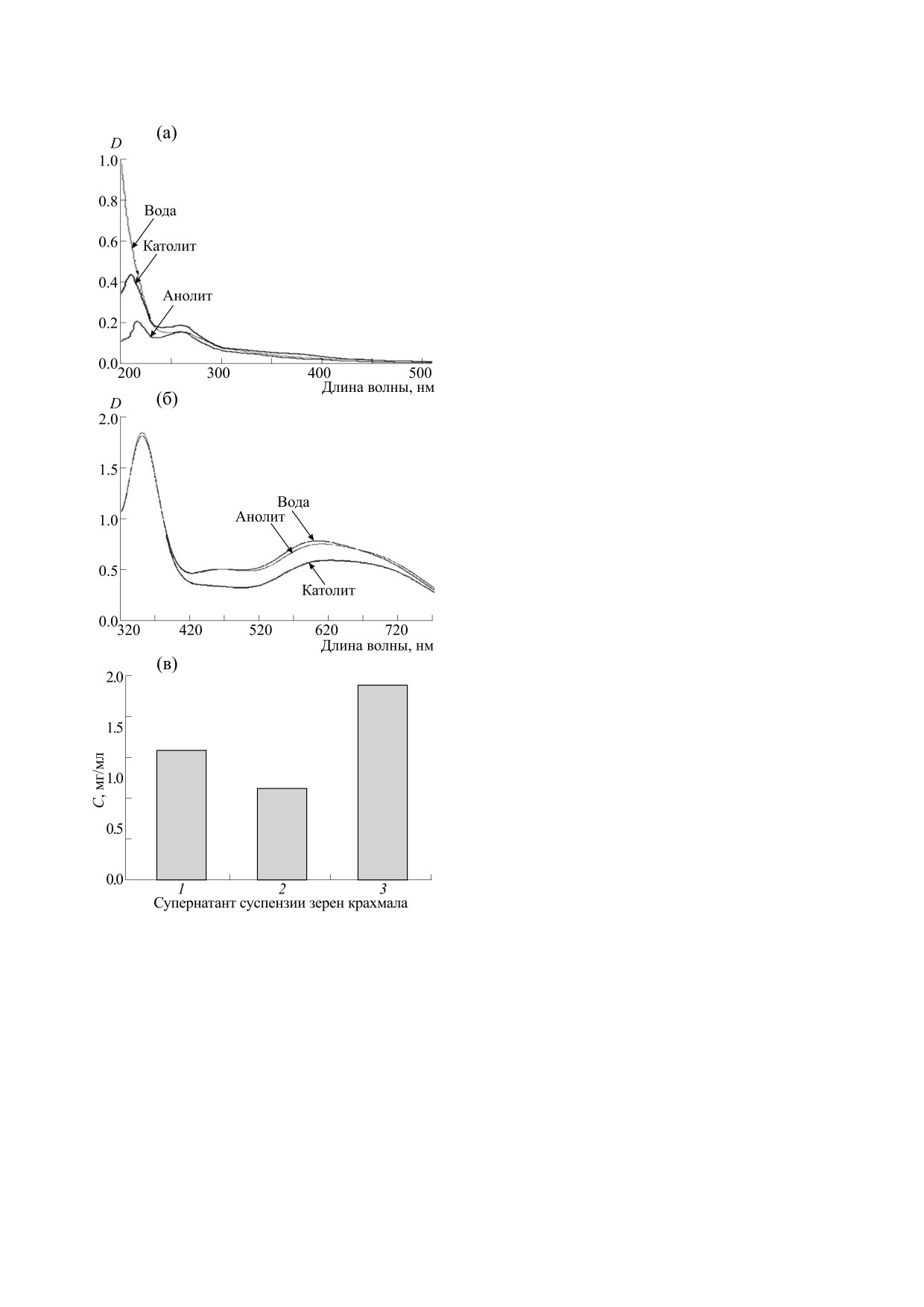
ектом исследования данного раздела. На рис. 4
показаны спектры поглощения супернатанта, по-
Результаты ToF-SIMS-анализа супернатанта,
лученного в результате осаждения частиц пище-
полученного после центрифугирования суспен-
вого крахмала, обработанных предварительно во-
зии зерен крахмала, которые обрабатывали водой
дой, анолитом или католитом.
или фракциями ЭХАР, приведены на рис. 5.
Для масс-спектров экстрактов пищевого крах-
Анализ UV-спектров (рис. 4а) супернатанта
мала (рис. 5а) посредством метода главных ком-
суспензии частиц пищевого крахмала показыва-
ет, что обе фракции ЭХАР одинаковым образом
понент проведен статистический анализ
влияют на образец с появлением пиков в областях
(рис. 5б). Сравнение данных молекулярного ана-
230 и 275 нм. Специфичные спектры поглощения
лиза показывает значимое отличие между кон-
трольным образцом (вода) и парой эксперимен-
(рис. 4б), полученные после иодитной окраски,
тальных групп, а также наличие различия между
соответствуют таким же спектрам для модифици-
рованного крахмала (рис. 1в). Отметим, что в от-
фракциями ЭХАР, что согласуется с данными
личие от данных UV-спектрометрии цветная ре-
UV-спектрометрии (рис. 4а). Учитывая выражен-
акция на олигосахара не показывает различия
ный амилолитический эффект католита, можно
ожидать изменение рельефа поверхности зерен
между образцами, обработанными водой или
крахмала. Данное предположение исследовали с
анолитом (рис. 4б). Этот факт свидетельствует о
том, что обработка анолитом пищевого крахмала
помощью сканирующей электронной микроско-
не вызывает изменение содержания олигосахаров
пии (рис. 6).
в супенатанте, но влияет на вид спектра в UV об-
Сравнение изображений, полученных при вы-
ласти (рис. 4а). После обработки крахмала като-
соком увеличении, позволяет установить связь
литом уровень олигосахаров в растворе значи-
качества поверхности зерен пищевого крахмала
тельно ниже, чем в воде или анолите (рис. 4б). Та-
со способом обработки. Видно, что для образца
кой результат может означать наличие у католита
после воздействия водой (рис. 6а3) характерен
БИОФИЗИКА том 68
№ 5
2023
868
ПОГОРЕЛОВ и др.
поверхности зерен крахмала. Такой результат со-
гласуется с данными спектрометрии, которые по-
казывают действие о ЭХАР на пищевой крахмал.
Отметим, что после обработки католитом в рас-
творе уменьшается концентрация олигосахаров,
но при этом увеличивается масса экстрагируемо-
го вещества, что показано микро взвешиванием
сухого остатка. Другими словами, католит демон-
стрирует псевдоферментативную активность,
свойственную одновременно α- и β-амилазе.
Завершая обсуждение результатов, можно
прийти к следующему заключению. Полисахари-
ды растительного происхождения (агар, крахмал)
подвержены действию фракций ЭХАР. Анализ
проб агара показывает идентичность эффекта об-
работки полисахарида обеими фракциями ЭХАР.
Для модифицированного крахмала методом ToF-
SIMS показано статистически значимое различие
молекулярного состава олигосахаров в зависимо-
сти от фракции ЭХАР. При использовании спе-
цифической цветной реакции с йодом было по-
казано амилолитическое действие католита на
раствор модифицированного крахмала, что обу-
словлено снижением содержания олигосахаров.
Под действием католита также уменьшается кон-
центрация олигосахаров в супернатанте суспен-
зии зерен пищевого крахмала, что может быть
следствием снижения экстрагирующей способ-
ности данной фракции ЭХАР. Однако методом
микровзвешивания сухого остатка показано на-
оборот увеличение массы растворенного веще-
ства. Этот результат согласуется с ультраструк-
турным анализом, который визуально демон-
стрирует травление католитом поверхности зерен
крахмала. Другими словами, подтверждено нали-
чие у католита псевдо ферментативной активно-
сти по типу одновременно α- и β-амилазы. Учи-
тывая широкое применение гидроколлоидов по-
лисахаридной природы в качестве загустителей и
гелеобразователей, использование ЭХАР можно
рассматривать как перспективное технологиче-
ское решение для производства пищевых продук-
тов.
Рис. 4. Параметры образцов супернатанта, полученно-
го после центрифугирования суспензии зерен пище-
вого крахмала, обработанных предварительно водой
БЛАГОДАРНОСТИ
или фракциями ЭХАР (анолит, католит): (а) - неспе-
цифичные UV спектры супернатанта; (б) - характер-
ToF-SIMS-анализ проведен на оборудовании
ные спектры супернатанта после окраски олигосаха-
ЦКП АХБС ФИЦ ХФ РАН (№ 506694).
ров посредством иодитной реакции; (в) - содержание
вещества, экстрагированного из зерен крахмала (1) во-
дой, (2) анолитом или (3) католитом.
ФИНАНСИРОВАНИЕ РАБОТЫ
более грубый рельеф, чем после фракций ЭХАР
Исследование выполнено при финансовой
(рис. 6б3,в3). Таким образом, результаты уль-
поддержке Российского научного фонда (проект
траструктурного анализа визуально демонстриру-
ют эффект травления фракциями ЭХАР рельефа
00019).
БИОФИЗИКА том 68
№ 5
2023
ДЕЙСТВИЕ ЭЛЕКТРОХИМИЧЕСКИ АКТИВИРОВАННОГО ВОДНОГО РАСТВОРА
869
Рис. 5. Результаты ToF-SIMS-анализа образцов пищевого крахмала, приготовленных из супернатанта суспензии зерен
полисахарида в воде (контроль) или фракциях ЭХАР (анолит, католит): (а) - диапазоны молекулярных масс, где везде
нижний масс-спектр соответствует контролю, средний масс-спектр - после обработки католитом, верхний масс-
спектр - после обработки анолитом; (б) - график счетов в координатах первых двух главных компонент, эллипсами обо-
значены 95%-е доверительные интервалы для групп из шести измерений в каждой.
Рис. 6. Микрофотографии рельефа поверхности зерен пищевого крахмала, полученные методом сканирующей
электронной микроскопии, режим вторичных электронов: (серия а1-а3) - зерна крахмала после обработки водой,
(серия б1-б3) - зерна крахмала после обработки католитом, (серия в1-в3) - зерна крахмала после обработки анолитом.
БИОФИЗИКА том 68
№ 5
2023
870
ПОГОРЕЛОВ и др.
КОНФЛИКТ ИНТЕРЕСОВ
7. Патент RU 2197840, Способ получения альгиновой
кислоты и альгината натрия из бурых водорослей
Авторы заявляют об отсутствии конфликта
(2003).
интересов.
8. A. Gerzhova, M. Benali, M. Mondor, and M. Aider,
Food Biosci., 11, 56 (2015).
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
9. Z. H. Li, B. Zhou, X. T. Li, and S. G. Li, Food Sci.
Biotechnol., 28, 15 (2018).
Настоящая работа не содержит описания ка-
10. Н. В. Науменко, Дис. … канд. техн. наук (М., 2007).
ких-либо исследований с использованием людей
11. K. Kobayashi, N. Tosa, Y. Hara, and S. Horie, Nippon
и животных в качестве объектов.
Shokuhin Kagayu Kogaku Kaisha, 43, 930 (1996).
12. R. Onishi, Y. Hara, and E. Arai, Food Sci. Technol.
СПИСОК ЛИТЕРАТУРЫ
Res., 5, 388 (1999).
13. Патент US 6326048, Preparation method of dough for
1. В. М. Бахир, Электрохимическая активация: изоб-
flour foods (2001).
ретения, техника, технологии (Вива-Стар, М.,
14. С. Н. Храпенков, М. В. Гернет, Д. А. Свиридов и
2014).
др., Пиво и напитки, 4, 18 (2003).
2. V. M. Bakhir and A. G. Pogorelov, Int. J. Pharm. Res.
15. Б. В. Кругликов, М. В. Гернет и И. В. Козлов, Пиво
Allied Sci., 7, 41 (2018).
и напитки, 5, 36 (2008).
3. К. Chyer, H. Yen-Con, and R. E. Brackett, J. Food
16. С. Н. Храпенков, М. В. Гернет и В. М. Бахир, Пиво
Protection, 63, 19 (2000).
и напитки, 5, 20 (2002).
4. T. Takenouchi and S. Wakabayashi, J. Appl. Electro-
17. M. S. Wagner and D. G. Castner, Langmuir, 17, 4649
chem., 36, 1127 (2006).
(2001).
5. Патент RU 2130472, Способ производства красите-
18. D. J. Graham, M. S. Wagner, and D. G. Castner, Appl.
ля из шелухи лука (1999).
Surf. Sci., 252, 6860 (2006).
6. Патент RU 2372399, Способ извлечения виннокислых
19. D. J. Graham and D. G. Castner, Biointerphases, 7, 49
соединений из виноградных выжимок (2009).
(2012).
Impact of Electrochemically Activated Water Solution on Plant Polysaccharides:
Phenomenology and Spectrophotometry
A.G. Pogorelov*, L.G. Ipatova*, A.I. Panait*, M.A. Pogorelova*, A.A. Gulin**, and V.N. Pogorelova*
*Institute of Theoretical and Experimental Biophysics, Russian Academy of Sciences,
Institutskaya ul. 3, Pushchino, Moscow Region, 142290 Russia
**Semenov Federal Research Center for Chemical Physics, Russian Academy of Sciences,
ul. Kosygina 4, Moscow, 119991 Russia
The determination of changes in the properties of polysaccharides in electrochemically activated water solu-
tion were carried out by means of UV-Vis spectrophotometry, time-of-flight secondary ion mass spectrom-
etry and scanning electron microscopy. It was shown how the properties of samples analyzed (agar, modified
starch, edible starch) changed depending on a fraction of electrochemically activated water solution (cathol-
yte/anolyte). Our findings demonstrate that the determined changes can be valuable information in designing
novel approaches to managing the properties of biological raw material used for food manufacturing process.
Furthermore, the technology of electrochemically activated water solutions is a suitable green chemical pro-
cess that can be translated to industrial level.
Keywords: electrochemically activated water solution, agar, starch, polysaccharide, oligosugar, UV-Vis spectro-
photometry, time-of-flight secondary ion mass spectrometry, scanning electron microscopy
БИОФИЗИКА том 68
№ 5
2023