БИОФИЗИКА, 2023, том 68, № 1, с. 20-32
МОЛЕКУЛЯРНАЯ БИОФИЗИКА
УДК 57.023, 573.3
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР:
ОБОСНОВАНИЕ НА ЭКСПЕРИМЕНТАХ in vitro
И ФИЗИКО-ХИМИЧЕСКИХ СВОЙСТВАХ
© 2023 г. С.В. Козин*, **, Л.И. Иващенко*, А.А. Кравцов*, **, Л.В. Васильева*,
А.М. Васильев*, Н.Н. Буков*, А.А. Дорохова*, **, #, О.М. Лясота*, **,
А.В. Беспалов*, С.С. Джимак*, **
*Кубанский государственный университет, Ставропольская ул., 149, Краснодар, 350040, Россия
**ФИЦ «Южный научный центр РАН», пр. Чехова, 41, Ростов-на-Дону, 344006, Россия
#E-mail: 013194@mail.ru
Поступила в редакцию 12.09.2022 г.
После доработки 23.09.2022 г.
Принята к публикации 26.09.2022 г.
Основными представителями гамма-пироновых кислот являются меконовая, коменовая,
хелидоновая и койевая кислоты. В отношении коменовой кислоты обнаружен нейропротекторный
эффект, а хелидоновая кислота обладает выраженным противовоспалительным действием. В
отношении меконовой кислоты нейропротекторное действие не было изучено. Целью настоящей
работы было установление нейропротекторного потенциала меконовой кислоты на модели
ишемического инсульта in vitro, в том числе и исходя из ее физико-химических свойств. Первичную
нейро-глиальную культуру получали из мозжечка семи-восьмисуточных крысят линии Wistar
методом механической-диссоциации. Защитное действие меконовой кислоты на культуру
нейронов мозжечка изучали на модели глутаматной токсичности и кислородо-глюкозной
депривации. Антиоксидантную активность меконовой кислоты изучали квантово-механическими
расчетами и экспериментально в модельной системе
«цитрат-фосфат-люминол» методом
хемилюминесцентного анализа. Хелатирующие свойства меконовой кислоты по отношению к Fe3+
в растворах изучены Job's-методом. Было установлено, что меконовая кислота оказывает защитный
эффект на моделях ишемии in vitro. Ее действие приводит к снижению уровня внутриклеточного
кальция и восстановлению мембранного потенциала митохондрий в культуре нейронов мозжечка
при глутаматном воздействии, и увеличению процента живых клеток при кислородо-глюкозной
депривации. Меконовая кислота имеет высокий расчетный антиоксидантный потенциал,
подтвержденный экспериментально. При повышении рН среды происходит ступенчатое
связывание меконовой кислоты с Fe3+ с образованием комплексов разного соотношения
лиганд/металл. При физиологических значениях pH полученный комплекс имеет состав 1:3.
Выявленное антиоксидантное, хелатирующее и цитопротекторное действие меконовой кислоты
дает основание для дальнейшего изучения возможных нейропротекторных свойств данного
соединения в экспериментах in vivo, а полученные в работе данные о ее физико-химических
свойствах могут быть полезны для синтеза и изучения новых координационных соединений на
основе меконовой кислоты.
Ключевые слова: антиоксидантная активность, меконовая кислота, культура нейронов мозжечка,
глутаматная токсичность, кислородо-глюкозная депривация, нейропротекция, комплексы железа.
DOI: 10.31857/S0006302923010039, EDN: NYXBTR
семейства γ-пироновых кислот, в отношении ко-
Меконовая кислота (МК, 3-гидрокси-4-оксо-
торых установлено терапевтическое действие.
4H-пиран-2,6-дикарбоновая кислота) является
Так, например, коменовая кислота (5-гидрокси-
представителем класса гамма-пироновых соеди-
4-оксо-4H-пиран-2-карбоновая кислота), входя-
нений, входит в состав опия снотворного мака
щая в состав лекарственного препарата «Бализ-
Papaver somniferum. С точки зрения фармакологии
2», способствует ускорению сроков заживления
МК интересна тем, что является представителем
язв двенадцатиперстной кишки. На модели
Сокращения: МК - меконовая кислота, ЭМГПС - этилме-
сквозной неинфицированной раны у кроликов
тилгидроксипиридина сукцинат.
было установлено, что коменовая кислота приво-
20
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
21
дила к уменьшению сроков закрытия раны. Ко-
малое количество витамина А [12]. Гиперпродук-
меновая кислота способствует снижению сроков
ция активных форм кислорода и азота, а также
заживления ожоговых ран и отторжению некро-
развитие процессов перекисного окисления ли-
за, не оставляя на теле грубых рубцов. Фармако-
пидов приводят к нарушению гематоэнцефали-
логическое средство «Бализ-2» на основе комено-
ческого барьера, развитию воспалительного про-
вой кислоты хорошо зарекомендовало себя в кли-
цесса, апоптотической и некротической гибели
нической практике и успешно применялось в
нейронов. Поэтому для снижения последствий
ходе военных действий, а также на борту косми-
инсульта и нейродегенеративных процессов была
ческой станции «Союз» [1]. Установлено, что ко-
предложена антиоксидантная терапия. Антиок-
меновая кислота оказывает антигипоксическое и
сиданты подразделяются на прямые и косвенные.
нейропротекторное действие у крыс на модели
Первые осуществляют захват радикалов за счет
гипоксического воздействия и острого иммоби-
особенностей структурного строения, эффект
лизационного стресса [2, 3] и оказывает протек-
вторых достигается активацией первичных и вто-
торное действие на культуру нейронов мозжечка
ричных мессенджеров клетки, ведущих к увели-
при глутаматном воздействии, снижая гибель
чению экспрессии ряда низкомолекулярных бел-
нейрональных клеток и уменьшая уровень ионов
ков и ферментов антиоксидантной защиты. В
кальция внутри клеток [4]. Она положительно
процессе старения происходит нарушение гомео-
влияет на рост спинальных ганглиев при дей-
стаза металлов переменной валентности, таких
ствии окислительного стресса [5], а также восста-
как медь и железо, что приводит к их накоплению
навливает амплитуду длительной потенциации
в тканях головного мозга [13]. У пациентов, стра-
переживающих срезов гиппокампа у стрессиро-
дающих нейродегенеративными расстройствами,
ванных животных [6]. Еще один представитель
обнаруживается избыточная концентрация
семейства 4H-пирановых кислот - хелидоновая
ионов железа в соответствующих областях голов-
кислота
(4-оксо-4H-пиран-2,6-дикарбоновая
ного мозга. При болезни Альцгеймера происхо-
кислота), входит в состав лекарственного расте-
дит активное накопление ионов железа в амило-
ния Chelidonium majus L. и оказывает противовос-
идных бляшках и нейрофибриллярных клубках и
палительное действие при моделировании у жи-
вокруг них [14]. При паркинсонизме накопление
вотных язвенного колита и аллергического рини-
ионов железа происходит в черной субстанции и
та [7, 8]. В отношении МК известно, что она,
тельцах Леви [15]. Усиление агрегации β-амило-
также как и коменовая кислота, снижает частоту
идного белка и α-синуклеина, а также отягоще-
повторных ответов ноцицептивных нейронов [9]
ние окислительного стресса на фоне накопления
и входит в состав неопиоидного анальгетика
железа приводит к прогрессированию данных за-
«Аноцептин» [10].
болеваний. Большое количество ионов железа
может резко высвобождаться в поврежденных об-
С точки зрения химии молекула МК интерес-
ластях мозга после местного кровоизлияния, вы-
на тем, что выступает потенциальным донорным
биолигандом для ряда жестких и умеренно жест-
званного травмой или эпизодов инсульта различ-
ной этиологии [16]. На основании этих данных
ких кислот Льюиса из d- и f-металлов [11], это да-
хелатотерапия металлов рассматривается как
ет основание для изучения координационных
перспективное направление в нейропротекции,
свойств МК с ионами биометаллов.
но в связи с высокой токсичностью многие хела-
Цереброваскулярные и нейродегенеративные
тирующие агенты не нашли клинического приме-
заболевания являются самыми распространен-
нения [17, 18].
ными неврологическими расстройствами и зани-
Еще одним патологическим звеном при ней-
мают второе место по смертности населения по-
родегенерации является эксайтотоксичность.
сле сердечно-сосудистых заболеваний. Послед-
Поэтому наряду с антиоксидантами используют
ствия данных заболеваний опасны высоким
лекарственные препараты, действие которых на-
уровнем инвалидизации всех слоев населения,
включая и трудоспособное. Основной стратегией
правленно на уменьшение токсического действия
глутамата. К таким веществам относят антагони-
лечения является фармакологическая коррекция,
сты глутаматных рецепторов, блокаторы кальци-
направленная на устранение ключевых патологи-
евых каналов, а также агонисты рецепторов гам-
ческих звеньев, развивающихся в поврежденных
ма-аминомасляной кислоты [19].
отделах головного мозга. Одним из таких звеньев
является окислительный стресс. В головном моз-
Современная нейрофармакология использует
ге есть необходимые предпосылки для развития
стратегию полипрагиазии, использующую одно-
свободнорадикальных процессов, особенно при
временно несколько препаратов, действующих
гипоксических условиях. Например, таковыми
на разные звенья патологического процесса [20].
являются наличие высокого содержания полине-
Применение нескольких препаратов создают не-
насыщенных жирных кислот, очень низкая ак-
которые проблемы: во-первых, из-за большой
тивность каталазы и глутатионпероксидазы, вы-
токсической нагрузки на организм пациента, во-
сокое содержание ионов двухвалентного железа и
вторых, необходимо учитывать взаимное влия-
БИОФИЗИКА том 68
№ 1
2023
22
КОЗИН и др.
ния веществ друг на друга в условиях организма.
меконовой кислоты (молярное соотношение 1:5)
Несмотря на большое количество известных мо-
изучали в условиях различной кислотности среды
лекул с нейропротекторной активностью, многие
(рН = 1-10). Регулирование pH среды осуществ-
из них не проходят стадии клинического испыта-
ляли концентрированными растворами гидрок-
ния [19, 21]. Поэтому вопрос поиска эффектив-
сида калия и хлорной кислоты, поскольку анион
ных и безопасных нейропротекторов, обладаю-
хлорной кислоты (ClO4-) не склонен к образова-
щих одновременно несколькими терапевтиче-
скими свойствами, является актуальной задачей.
нию комплексов с катионами Fe3+. Ионную силу
В литературе отсутствуют сведения о комплексо-
во всех экспериментах поддерживали 0.1 М рас-
образующих свойствах МК с ионами железа. Ра-
твором хлорида калия.
нее было сказано, что родственные меконовой
Определение состава комплексов осуществля-
кислоте коменовая и хелидоновая кислоты обла-
дают высокой биологической активностью, в том
ли методом изомолярных серий (метод Остро-
числе антиоксидантной и противовоспалитель-
мысленского-Жоба) [24]. Для этого готовили три
ной. В исследовании, проведенном нами раннее,
серии растворов смеси трехвалентного железа и
было установлено, что МК ингибировала разви-
меконовой кислоты в антибатных соотношениях
тие реакции свободнорадикального окисления
от 1:9 до 9:1, сохраняя постоянным общий объем
липидов желтка и повышала выживаемость ней-
раствора в каждом опыте (рН 3.0, 5.0 и 7.5). Необ-
ронов мозжечка при глутаматном воздействии
ходимое значение кислотности задавали раство-
[22]. Целью настоящей работы было исследова-
ром HCl/KCl для рН 3.0 и ацетатным буфером для
ние нейропротекторного потенциала меконовой
рН 5.0; физиологическое значение pH 7.4 поддер-
кислоты на моделях ишемического инсульта in vi-
живали HEPES-буфером. Используя полученные
tro, а именно, оценить уровень внутриклеточного
кривые «состав-свойство», определяли ступен-
кальция и мембранный потенциал митохондрий
чатые константы нестойкости образующихся
нейронов мозжечка при глутаматной токсично-
комплексных соединений. Так, путем линейной
сти, исследовать ее защитный эффект при кисло-
экстраполяции начальных участков каждой кри-
род-глюкозной депривации, а также дальнейшее
исследование антиоксидантных свойств МК ис-
вой до точки пересечения определяли оптиче-
ходя из ее физико-химических свойств.
скую плотность A0, соответствующую комплексу
при полном отсутствии диссоциации, и далее
рассчитывали ступенчатую константу нестойко-
МАТЕРИАЛЫ И МЕТОДЫ
сти по формуле K = α2С/(1 - α), где С - концен-
Меконовая кислота была получена в отделе
трация несвязанного в комплекс лиганда; α - сте-
биологически активных веществ Кубанского го-
пень диссоциации комплекса, которую рассчи-
сударственного университета из койевой кислоты
тывали по формуле α = (A0 - A1)/A0 где A1 -
по методике, подробно описанной немецкими
оптическая плотность, соответствующая макси-
исследователями [23]. Чистоту полученного со-
муму кривой изомолярной серии (эксперимен-
единения контролировали методом тонкослой-
тальное значение).
ной хроматографии на пластинах «Сорбфил-А»,
элюент - изопропанол, растворитель - диметил-
Полученные константы нестойкости допол-
сульфоксид, проявитель - пары йода, щелочной
нительно уточняли методом кажущегося откло-
раствор KMnO4. Качественный фазовый состав
нения от закона Бугера-Ламберта-Бера (метод
Бабко) [24].
устанавливали рентгенодифрактометическим ме-
тодом на приборе XRD-7000 (Shimadzu, Япония).
Антиоксидантную активность МК изучали ме-
Идентификацию пиков на дифрактограммах и
тодом хемилюминесцентного анализа на приборе
количественное содержание фаз проводили с по-
Lum-100 (Россия) в модельной системе - «цит-
мощью программного комплекса PDWin 2.0 и па-
рат-фосфат-люминол» [25]. Веществом сравне-
кета Crystallographica Search-Match, интегриро-
ния служил антиоксидант - этилметилгидрокси-
ванных в программно-аппаратный комплекс
пиридина сукцинат (ЭМГПС). Модельная систе-
прибора. Инфракрасные спектры записывали на
ма
«цитрат-фосфат-люминол» состоит из
ИК-Фурье-спектрометре VERTEX
70 (Bruker,
цитрата натрия
(4 мМ), фосфатного буфера
Германия). Электронные спектры фиксировали
(105 мМ KCl,
20 мМ KH2PO4) и люминола
на двулучевом спектрофотометре U-2900 (Hita-
(10 мМ). Инициацию свечения проводили добав-
chi, Япония).
лением 35 мМ Fe2+ в форме сульфата железа. Ре-
Электронные спектры поглощения меконовой
гистрацию вели пять минут. Антиоксидантный
кислоты и комплексных соединений, образую-
статус исследуемого вещества оценивали по ин-
щихся в растворе при сливании растворов FeCl3 и
тенсивности свечения (площадь под спектраль-
БИОФИЗИКА том 68
№ 1
2023
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
23
ной кривой) в усл. ед., а также по тангенсу угла
рый добавляли к культурам перед воздействием
наклона восходящего участка графика.
глутамата на 30 мин. Регистрацию флуоресцен-
ции проводили при длине волны возбуждения
Квантово-химическое исследование осу-
485 нм, эмиссии 535 нм. Результаты представле-
ществляли в программном пакете ORCA 5.0.1
ны в процентах, за 100% принят уровень флуорес-
[26]. Оптимизацию геометрии нейтральных мо-
ценции контрольных культур, не подвергавшихся
лекул, анионов и радикалов, а также расчет тер-
воздействию глутамата и меконовой кислоты.
модинамических параметров осуществляли в
Мембранный потенциал митохондрий после глу-
рамках теории DFT с помощью хорошо известно-
таматного воздействия определяли с использова-
го гибридного функционала B3LYP [27] с диспер-
нием флуоресцентного зонда тетраметилродами-
сионной поправкой D3BJ [28] в валентно-рас-
на (ThermoFicher Scientific, США), который до-
щепленном базисном наборе def2-TZVPD [29].
бавляли к культурам перед воздействием
Все найденные геометрии подтверждались отсут-
глутамата на 30 мин. Регистрацию флуоресцен-
ствием мнимых колебательных частот. Все расче-
ции проводили при длине волны возбуждения
ты проводили с учетом неспецифической сольва-
535 нм, эмиссии 595 нм. Результаты представле-
тации в рамках модели СРСМ (растворитель -
ны в процентах, за 100% принят уровень флуорес-
вода) [30]. Для генерации Input-файлов применя-
ценции контрольных культур, не подвергавшихся
ли программу Gabedit 2.5. Для визуализации мо-
воздействию глутамата и меконовой кислоты.
лекулярной геометрии и колебательных частот
использовали программу ChemCraft 1.8.
Все измерения с использованием зондов про-
водили на многофункциональном ридере для
Первичную нейроглиальную культуру получа-
микропланшетов FilterMax F5 (США).
ли из мозжечка 7-8-суточных крысят линии Wis-
tar методом ферментно-механической диссоциа-
Статистическую обработку полученных дан-
ных проводили с помощью STATISTICA 10. До-
ции, с последующей недельной инкубацией в пи-
стоверность различий средних значений (М),
тательной среде, состоящей из фетальной
найденных между группами, статистически оце-
телячьей сыворотки (10%) и среды Игла (90%)
нивали с помощью непараметрического U-крите-
[31]. Для определения доли живых клеток исполь-
рия (Манна-Уитни), различие считали достовер-
зовали ручной подсчет, для этого культивирован-
ным для р < 0.05. Данные представлены в виде
ные клетки фиксировали смесью «этанол-фор-
M ± m, где M - среднее значение, m - стандарт-
мальдегид-уксусная кислота» (7:2:1) с последую-
ная ошибка среднего.
щем окрашиванием трипановым синим.
Кислородно-глюкозную депривацию моделиро-
вали, заменяя на 45 мин культуральную среду на
РЕЗУЛЬТАТЫ
солевой раствор (состав (в мм): NaCl - 154, KCl -
Полученное соединение характеризуется ря-
25, CaCl2 - 2.3, MgCl2 - 1, NaHCO3 - 3.6,
дом специфических полос в инфракрасном спек-
Na2HPO4 - 0.35, HEPES - 10) и помещая культу-
тре, характерных для меконовой кислоты и ука-
занных в работе [23]: 3508, 3362, 3092, 1752, 1676,
ры в аргоновую атмосферу вместе с безглюкоз-
ным солевым раствором [32]. Через 45 мин куль-
1622, 1269, 1232, 1196, 1053, 906, 783, 667 см-1.
туры промывали и возвращали в солевой раствор
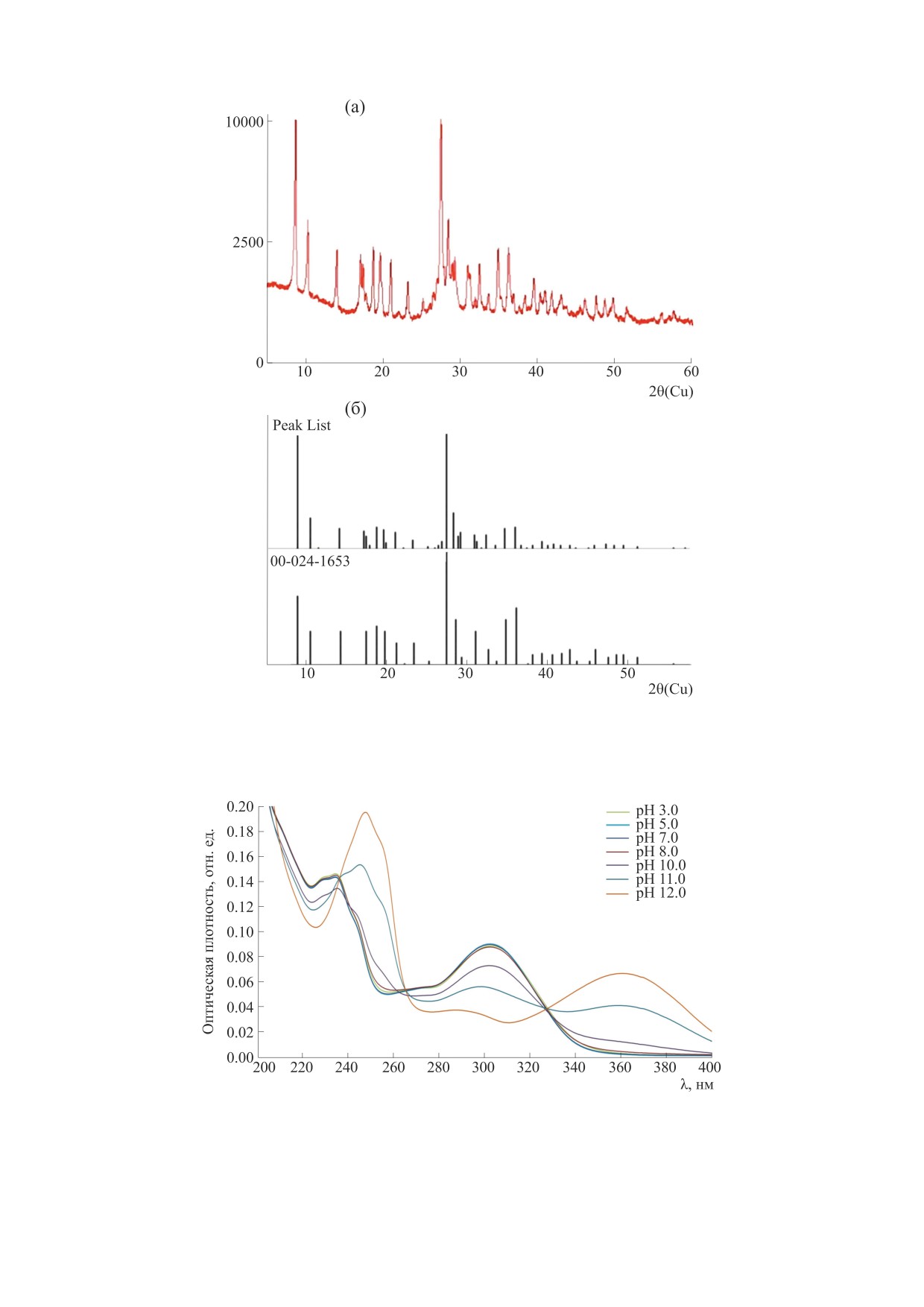
Согласно данным рентгенофазового анализа
с глюкозой и МК в исследуемых концентрациях
исследуемый образец имеет кристаллическую
1.0, 0.1, 0.01 и 0.001 мМ; через сутки промывали от
структуру (рис. 1а) и характеризуется определен-
вещества и проводили фиксацию с последующим
ным набором значений 2θ, межплоскостных рас-
окрашиванием. Результат пересчитывали в про-
стояний dhkl и относительных интенсивностей I
центах от контроля.
(%), которые сравнивали с табличными значени-
ями эталонных дифрактограмм однофазных ве-
Эксайтотоксичность моделировали добавле-
ществ, представленных в базе данных ICDD-PDF-2.
нием глутамата (Sigma, США) концентрацией
Исследуемый образец идентифицируется как
50 мкМ на 10 мин в солевом растворе следующего
гидрат меконовой кислоты с брутто-формулой
состава (в мМ): NaCl - 154, KCl - 25, CaCl2 - 2.3,
С7H4O7 ∙ 3H2O орторомбической кристалличе-
NaHCO3 - 3.6, Na2HPO4 - 0.35, HEPES - 5, глю-
ской системы (код ссылки: 00-024-1653) (рис. 1б).
коза - 5.6. Затем культуры возвращали в исход-
Для определения области существования раз-
ную питательную среду. В часть лунок добавляли
личных форм комплексных соединений, во-пер-
МК в концентрации 1.0, 0.1, 0.01 и 0.001 мМ. Уро-
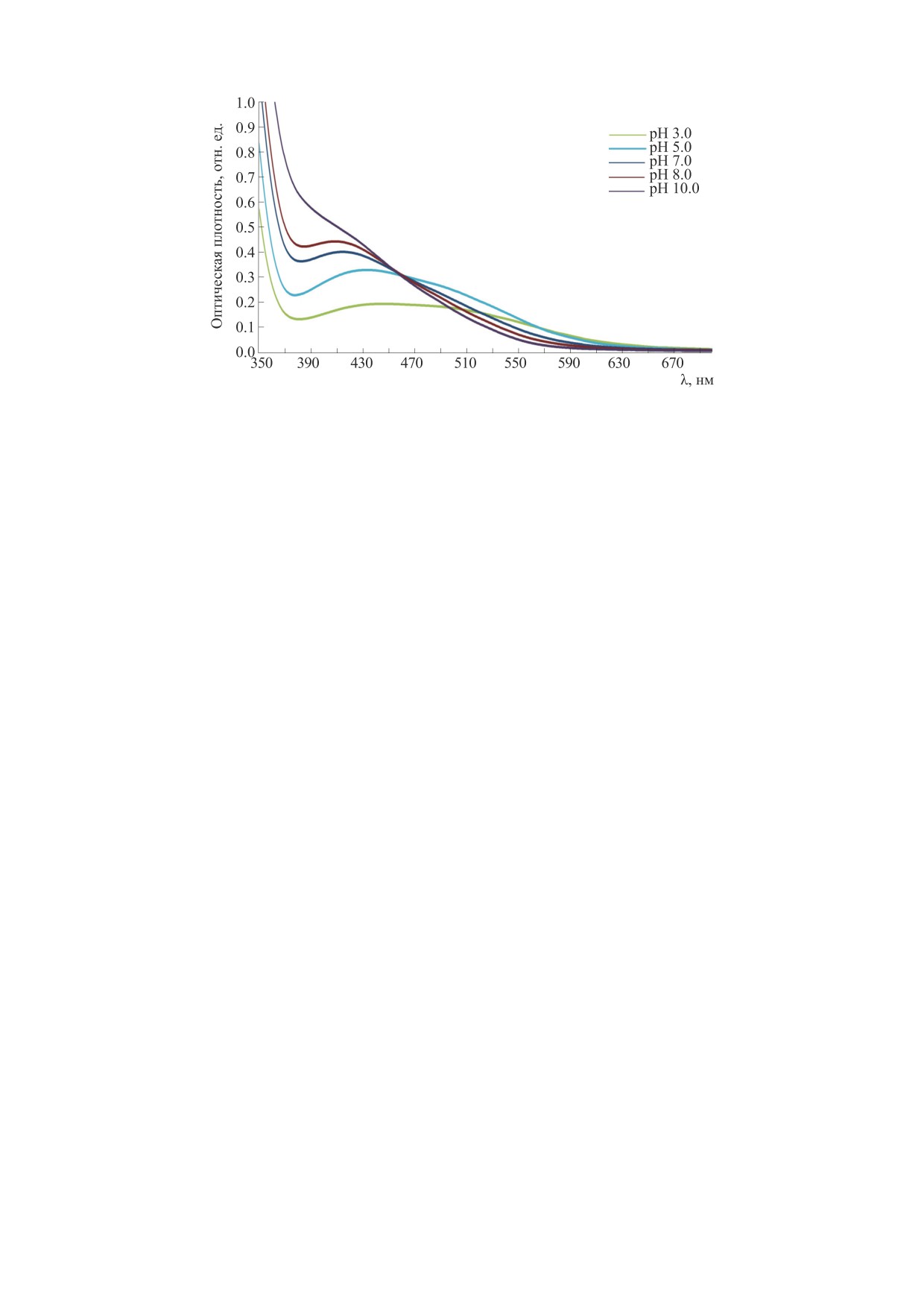
вых, изучено спектральное поведение меконовой
вень кальция после действия глутамата определя-
кислоты при различных рН среды. Из рис. 2 вид-
ли с использованием флуоресцентного зонда
но, что спектр поглощения меконовой кислоты
Fluo4-AM (ThermoFicher Scientific, США), кото-
при повышении рН среды от 3 до 10 не испытыва-
БИОФИЗИКА том 68
№ 1
2023
24
КОЗИН и др.
Рис. 1. (а) - Дифрактограмма исследуемого образца, (б) - штрих-диаграммы исследуемого и эталонного образца.
Рис. 2. Электронные спектры водных растворов меконовой кислоты при различных pH.
БИОФИЗИКА том 68
№ 1
2023
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
25
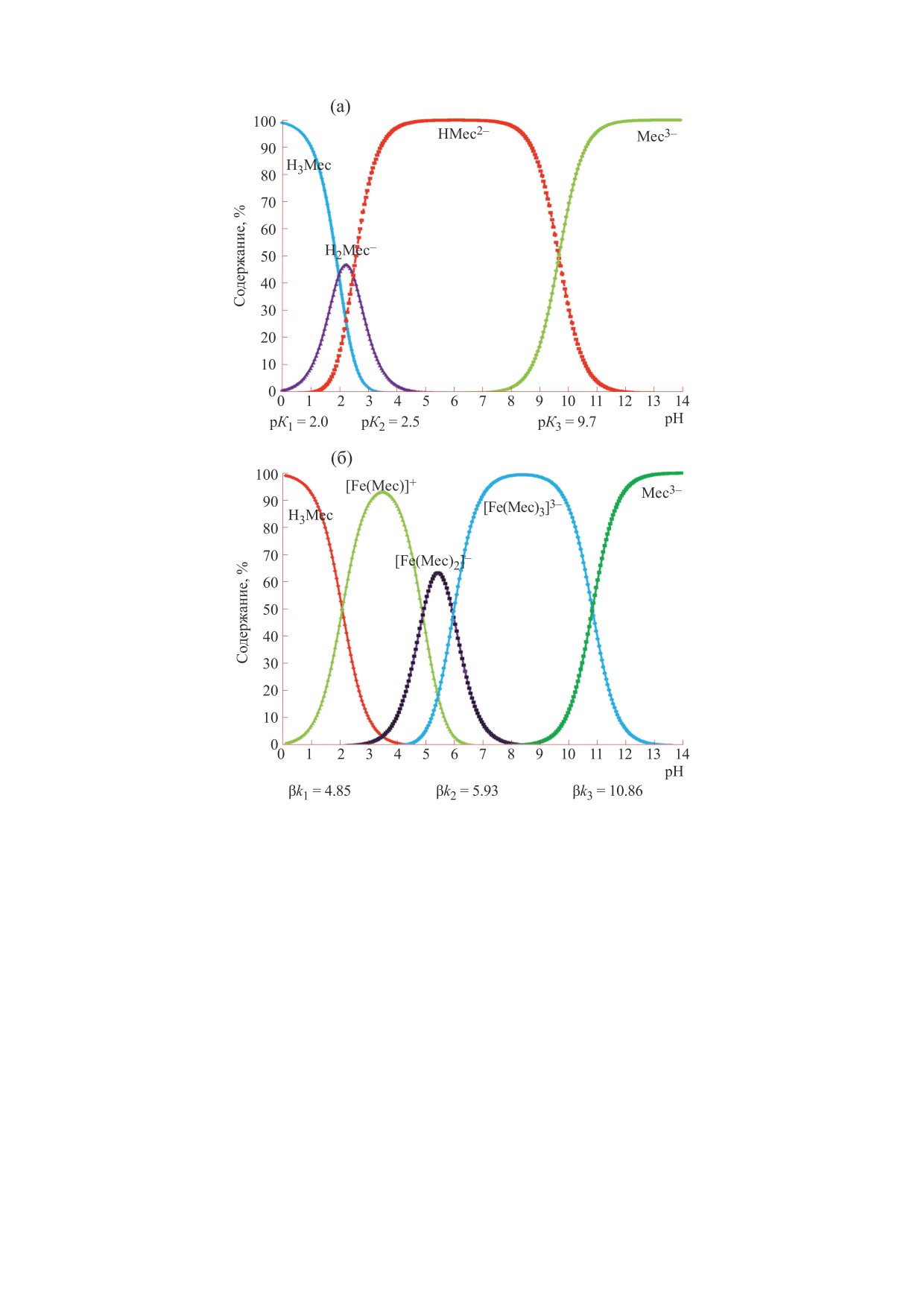
Рис. 3. Электронные спектры водных растворов FeCl3 (5.0 · 10-5 М) и меконовой кислоты (мольное соотношение 1 : 5).
ет заметных изменений и обладает двумя харак-
чен комплекс с соотношением лиганд/металл 1 : 2
терными максимумами: λ1 = 233 нм и λ2 = 303 нм.
с K2 = 1.07·10-6 моль/л и lgβk2 = 5.93. При физио-
При pH свыше 10 происходит депротонирование
логическом значении pH раствора состав ком-
ОН-группы, которое приводит к батохромному
плекса 1 : 3 с K3 = 1.21 · 10-11 моль/л и lgβk3 = 10.86.
сдвигу максимумов полос поглощения, отвечаю-
щей за переход π→π, в результате чего максимум
Методом Бабко были получены близкие зна-
поглощения смещается к 247 и 360 нм. Во-вто-
чения констант. Для комплекса составом 1 : 1
рых, записаны электронные спектры поглощения
при разбавлении в два и пять раз
комплексных соединений, образующихся в рас-
получены K1 = 1.58 · 10-5 моль/л, lgβk1 = 4.80, K1* =
творе при сливании растворов FeCl3 и меконовой
= 1.48 · 10-5 моль/л, lgβk1* = 4.83. При разбавле-
кислоты (молярное соотношение 1 : 5) в условиях
различной кислотности среды (рН = 1÷10).
нии в два раза для комплекса 1 : 2 значения кон-
Из рис. 3 видно, что максимумы полос погло-
стант следующие: K2 = 1.26 · 10-6 моль/л, lgβk2 =
щения различных форм комплексов лежат в обла-
= 5.90, а при разбавлении в пять раз комплекса
сти 380-600 нм, а изобестическая точка располо-
данного состава получили K2* = 1.20 · 10-6 моль/л,
жена при 460 нм. В качестве аналитической дли-
lgβk2* = 5.92. При соотношении лиганд/металл,
ны волны для метода изомолярных серий и
метода Бабко использовали длину волны 420 нм
равном 1 : 3, K3 = 1.35 · 10-11 моль/л, lgβk3 = 10.87 (при
(средняя величина, при которой каждая из форм
разбавлении в два раза) и K3* = 1.55 · 10-11 моль/л,
комплексов имеет поглощение в электронном
спектре).
lgβk3* = 10.81 (при разбавлении в пять раз). На ос-
Из рис. 4а видно, что первая и вторая констан-
новании величин констант устойчивости, полу-
та диссоциации меконовой кислоты составляют
ченных на основании двух экспериментальных
2.0 и 2.5 и соответствуют депротонированию двух
методов, была построена диаграмма распределе-
карбоксильных групп, третья константа находит-
ния различных форм комплексов от pH раствора.
ся в щелочной области и равна 9.7 и обусловлена
Из нее видно, что при физиологическом значе-
диссоциацией гидроксильной группы. Таким об-
нии pH преобладает комплекс состава
1:3
разом, при значениях pH, близких к физиологи-
(~97%), на долю комплекса составом 1 : 2 прихо-
ческим, меконовая кислота находится в дважды
дится ~3%. Таким образом, при повышении рН
депротонированной форме (~ 99%). С использо-
среды происходит ступенчатое образование ком-
ванием диаграмм изомолярных серий были полу-
плексов по следующей схеме:
чены константы нестойкости и полные констан-
Fe3+ + H3Mec ↔ [Fe(HMec)]+ + 2H+,
ты устойчивости вышеуказанных комплексов
при трех значениях pH. При pH 3.0 получен ком-
[Fe(HMec)]+ + H3Mec ↔ [Fe(HMec)2]- + 2H+,
плекс с соотношением лиганд/металл 1 : 1 с K1 =
1.20·10-5 моль/л и lgβk1 = 4.85. При pH 5.0 полу-
[Fe(HMec)2]- + H3Mec ↔ [Fe(HMec)3]3- + 2H+,
БИОФИЗИКА том 68
№ 1
2023
26
КОЗИН и др.
Рис. 4. (а) - Диаграмма зависимости распределения ионных форм меконовой кислоты от pH; (б) - диаграмма
распределения различных форм комплекса Fe3+ с меконовой кислотой в зависимости от pH.
472.4 кДж/моль, тогда как для анионной формы -
Fe3+ + nH3Mec ↔ [Fe(HMec)n](3-n) + nH+,
322.3 кДж/моль.
где H3Mec
- молекула меконовой кислоты,
В модельной системе «цитрат-фосфат-люми-
[Fe(HMec)]+ - комплекс состава 1 : 1, [Fe(HMec)2]- -
нол» МК проявила дозозависимое снижение ин-
комплекс состава 1:2, [Fe(HMec)3]3- - комплекс
тенсивности свечения и уменьшение тангенса на-
состава 1 : 3.
клона восходящего графика хемилюминесцент-
Согласно расчетным данным, меконовая кис-
ной реакции (табл. 1). При концентрации 0.2 мМ
лота обладает наименьшим значением энтальпии
МК уменьшает хемилюминесценцию на 73%
одноэлектронного переноса в трианионной фор-
против 48% в случае ЭМГПС. Снижение инте-
ме и составляет 318.7 кДж/моль, тогда как для ди-
грального показателя свечения при концентра-
анионой формы данное значение равно
циях антиоксидантов 0.3 и 0.6 мМ составило 80 и
421.3 кДж/моль. Для нейтральной молекулы
87% у МК против 55 и 73% у ЭМГПС (p < 0.05).
ЭМГПС данный показатель составляет
Меконовая кислота также, как и вещество срав-
БИОФИЗИКА том 68
№ 1
2023
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
27
Таблица 1. Показатели хемилюминесцентной реакции в модельной системе «цитрат-фосфат-люминол»
Интенсивность свечения, усл. ед.
tgα ⋅ 10-4
Концентрация, мМ
МК
ЭМГПС
МК
ЭМГПС
0
141.0 ± 1.9
141.0 ± 1.9
360 ± 9
360 ± 9
0.2
38.0 ± 0.8*#
73.0 ± 3.2*
90 ± 3*#
190 ± 3*
0.3
28.0 ± 0.5*#
64.0 ± 1.4*
56 ± 3*#
160 ± 6*
0.6
16.0 ± 0.6*#
38.0 ± 1.1*
24 ± 4*#
100 ± 6*
Примечание. МК - меконовая кислота, ЭМГПС - этилметилгидроксипиридина сукцинат, * - p < 0.05 по сравнению с
контролем, # - p < 0.05 по сравнению с ЭМГПС.
нения этилметилгидроксипиридина сукцинат
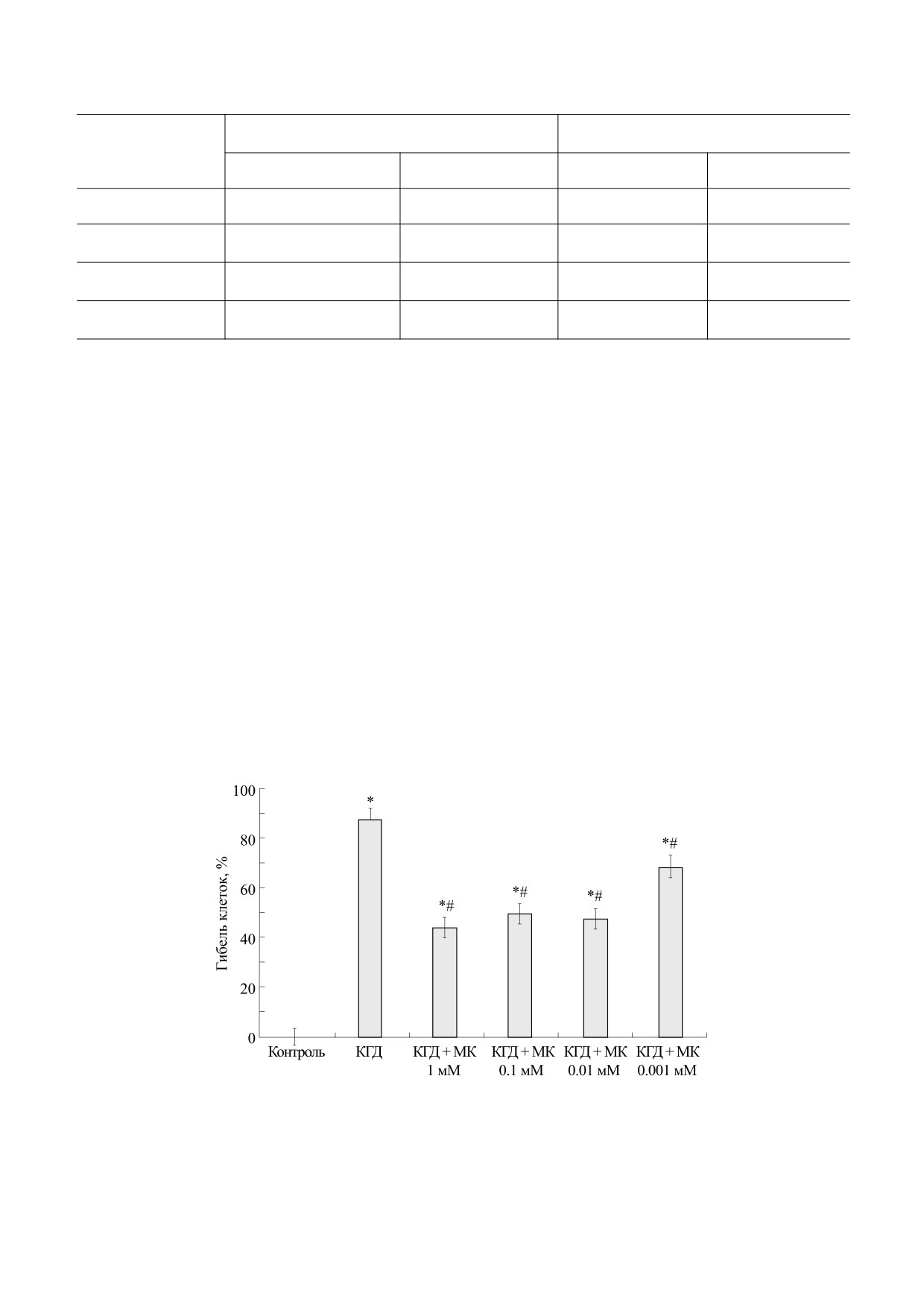
вали только после воздействия - кислородо-глю-
ингибировали образование аминофталевой кис-
козной депривации. Из рис. 5 видно, что при
лоты (конечного продукта окисления люминола).
действии кислородо-глюкозной депривации в от-
Данные этого эксперимента хорошо согласуется с
сутствие меконовой кислоты количество живых
результатами раннее проведенного нами иссле-
клеток составило 12%. Добавление МК в культуру
дования. В работе [22] показано, что МК и
нейронов мозжечка, подвергшихся кислородо-
ЭМГПС оказывали дозозависимое снижение ин-
глюкозной депривации, способствовало увеличе-
тенсивности развития свободнорадикальной ре-
нию выживаемости клеток. Статистически зна-
акции окисления липидов желтка в модельной
чимое отличие в количестве живых клеток между
системе желточных-липопротеинов. Получен-
исследуемыми концентрациями не наблюдалось,
ные экспериментальные данные в двух модель-
однако максимальный эффект наблюдался при
ных системах и расчетные данные указывают на
концентрации 1 мМ и составил 56%, а минималь-
высокий антиоксидантный потенциал МК.
ный - при концентрации 0.001 мМ и составил
31%.
Ранее было показано [22], что добавление МК
в культуры нейронов мозжечка, не подвергшихся
На рис. 6 представлены результаты исследова-
воздействию, во всех исследуемых концентраци-
ния влияния меконовой кислоты на уровень
ях не влияла на жизнеспособность клеток, поэто-
внутриклеточного кальция при эксайтотоксиче-
му действие МК на выживаемость клеток оцени-
ском воздействии глутаматом.
Рис. 5. Влияние меконовой кислоты на выживаемость нейронов мозжечка при кислородо-глюкозной депривации. Данные
представлены в виде M ± m; * - p < 0.05 к контролю; # - p < 0.05 к кислородо-глюкозной депривации.
БИОФИЗИКА том 68
№ 1
2023
28
КОЗИН и др.
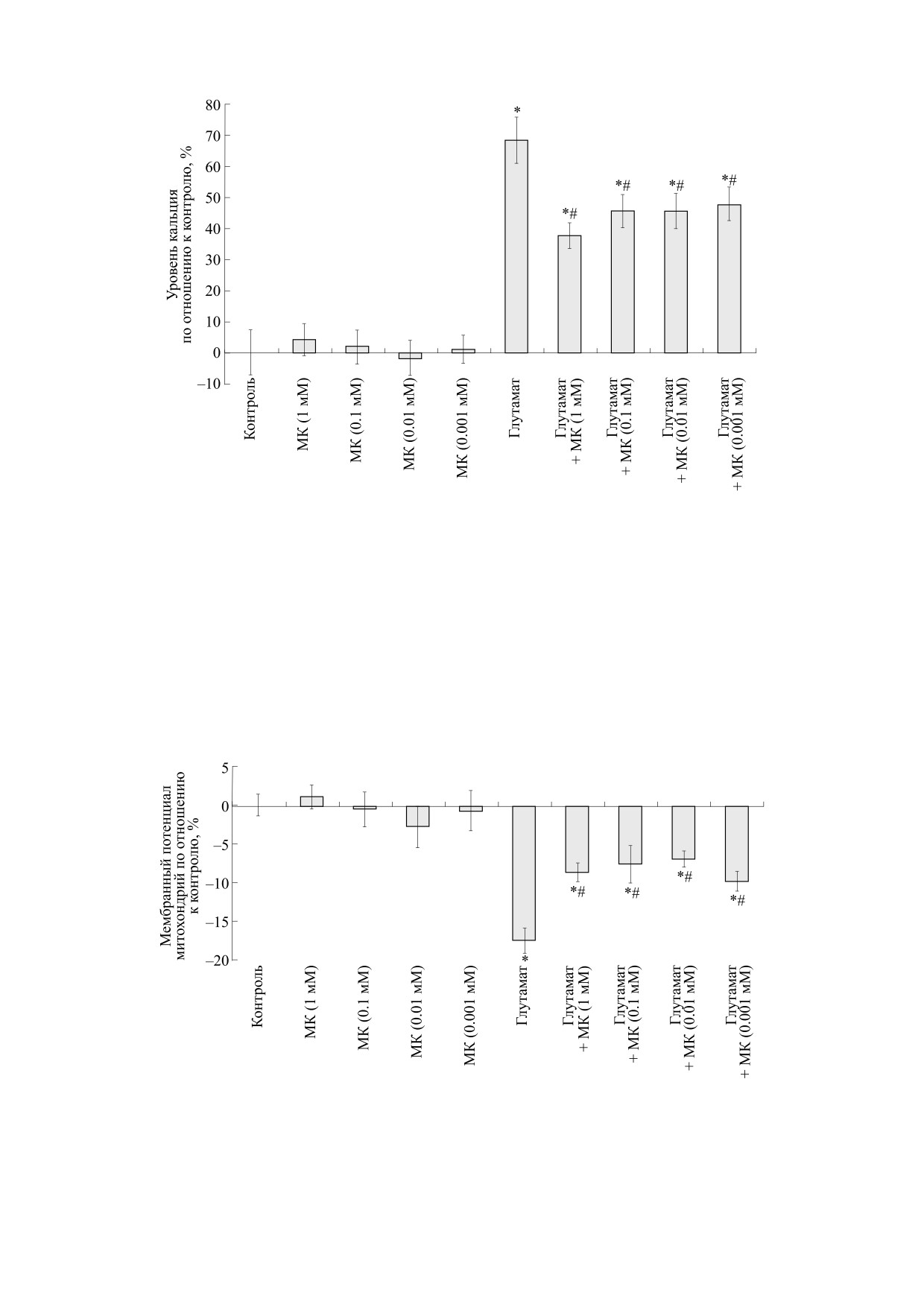
Рис. 6. Влияние меконовой кислоты на уровень внутриклеточного ионов кальция при глутаматной токсичности. Данные
представлены в виде M ± m; * - p < 0.05 к контролю; # - p < 0.05 к глутамату.
Анализ полученных данных показал, что воз-
траций 1.0, 0.1, 0.01 и 0.001 мМ. В культурах, не
действие глутаматом приводит к возрастанию
подвергшихся глутаматному воздействию, МК не
уровня кальция на 69% по отношению к контро-
оказала статистически достоверного влияния на
концентрацию ионов кальция в цитозоле нейро-
лю. С другой стороны, в культурах с добавлением
нов мозжечка.
МК повышение уровня кальция было существен-
но меньше и составило 38, 46, 46 и 48% по отно-
На рис. 7 показано, что воздействие глутама-
шению к контролю соответственно для концен- том на клетки головного мозга приводит к сниже-
Рис. 7. Влияние меконовой кислоты на мембранный потенциал митохондрий при глутаматной токсичности. Данные
представлены в виде M ± m; * - p < 0.05 к контролю; # - p < 0.05 к глутамату.
БИОФИЗИКА том 68
№ 1
2023
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
29
нию мембранного потенциала митохондрий на
болизма железа и развития неврологических за-
17% по отношению к контролю. Меконовая кис-
болеваний. Так, у пациентов, страдающих болез-
лота способствовала меньшему снижению значе-
нью Альцгеймера, наблюдается повышенное на-
ния мембранного потенциала митохондрий - на
копление ионов железа в гиппокампе
[36].
9, 8, 7 и 10% по сравнению с контролем соответ-
Применение хелаторов железа, таких как дефе-
ственно для концентраций
1.0,
0.1,
0.01 и
роксамин, увеличивает уровень дофамина в клет-
0.001 мМ.
ках черной субстанции и предупреждает развитие
Добавление меконовой кислоты в культуру
окислительного стресса у пациентов, страдаю-
нейронов мозжечка способствует снижению ги-
щих болезнью Паркинсона [37]. Эксперименты in
бели клеток при кислородном и глюкозном голо-
vitro и in vivo на грызунах показали, что примене-
дании, препятствует повышению внутриклеточ-
ние ферростатина-1 оказало защитный эффект
ного уровня кальция и снижению мембранного
при моделировании болезни Гентингтона [38].
потенциала митохондрий при глутаматном воз-
Установлено, что при всех видах инсульта проис-
действии - одних из ключевых факторов, приво-
ходит аккумуляция ионов железа, а применение
дящих к повреждению клеток. Таким образом,
их хелаторов приводит к значительному улучше-
МК препятствует эксайтотоксическому действию
глутамата, оказывая цитопротекторный эффект
нию состояния пациентов [39]. Основной причи-
на культуры нейронов мозжечка.
ной патологического действия ионов Fe2+ явля-
ется развитие реакции Фентона и усиление на
фоне этой реакции процессов перекисного окис-
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
ления липидов, которое сопровождается сниже-
Для МК возможна реализация трех возмож-
нием восстановленного глутатиона и активности
ных механизмов антиоксидантной активности:
глутатионпероксидазы в нейронах головного
прямой перенос атома водорода (HAT), одно-
мозга. Следует отметить роль ионов железа (III) в
электронный перенос с последующим депрото-
развитии повреждающего эффекта. Восстановле-
нированием (SET-PT) и депротонирование с по-
ние ионов Fe3+, образующихся в результате реак-
следующим одноэлектронным переносом
ции Фентона, аскорбиновой кислотой открывает
(SPLET) [33]. Поскольку вероятность реализации
дополнительный канал для образования актив-
механизмов HAT и SET-PT в водной среде неве-
ных форм кислорода [40]. Относительно высокие
лика [34], то можно предположить, что основным
концентрации аскорбиновой кислоты и ионов
механизмом реализации прямого антиоксидант-
железа в головном мозге способствуют развитию
ного эффекта меконовой кислоты является
следующих реакций и созданию повреждающего
SPLET-механизм, для которого и была рассчита-
цикла:
на энтальпия одноэлектронного переноса. Как
видно из диаграммы протеолитического равнове-
1) Fe2+ + H2O2 = Fe3++OH∙+OH-,
сия МК при физиологических pH может находит-
2) Fe3+ + AscH2 (или AscH) = Fe2+ + AscH (или
ся в двух состояниях: дианионной форме НMec2-
Asc-) +H+.
(99.82%) и трианионной Mec3- (0.018%) с соот-
Разорвать данный замкнутый круг можно при-
ветствующими энергиями отрыва электрона
менением хелаторных лигандов или/и веществ с
421.3и 318.7 кДж/моль. Расчетные значения энер-
прямым антиоксидантным эффектом. Таким об-
гии переноса электрона для МК ниже, чем у при-
разом, хелатирование ионов Fe2+ и Fe3+ в тканях
родных антиоксидантов - катехинов [33], а экс-
головного мозга при окислительном стрессе мо-
периментально полученные значения ингибиро-
жет ингибировать развитие реакции Фентона и
вания развития свободнорадикальных реакций
обрывать одну из цепей свободнорадикального
выше, чем у лекарственного антиоксидантного
окисления, а также выводить избыточное железо
препарата «Мексидола». Все это указывает на вы-
из поврежденных отделов головного мозга при
сокий уровень прямого антиоксидантного потен-
нейродегенеративных процессах. Имеющиеся на
циала меконовой кислоты. Также ее прямой ан-
сегодняшний день данные позволяют рассматри-
тиоксидантный эффект может реализоваться за
вать хелаторы железа как потенциальные нейро-
счет способности МК вступать во взаимодей-
протекторы [16-18]. Результаты наших исследо-
ствие с ионами железа и образовывать координа-
ваний показали, что при физиологическом значе-
ционные комплексы. Койевая кислота, близкая
нии pH преобладает комплекс с соотношением
по строению к МК, способна к образованию хе-
латных комплексов с ионами железа и алюминия
меконовая кислота/Fe3+ 3 : 1 в значении ~97% с
[35]. В последнее время в литературе появляется
высокой константой устойчивости, тогда как на
все больше сведений о влиянии нарушения мета-
долю комплекса составом 2 : 1 приходится ~3%.
БИОФИЗИКА том 68
№ 1
2023
30
КОЗИН и др.
Эти данные позволяют говорить о возможном хе-
тотоксический эффект глутамата. Можно пред-
латировании ионов железа МК в тканях головно-
положить, что действие МК приводит к актива-
го мозга и уменьшению интенсивности окисли-
ции некоторых сигнальных путей, за счет
тельных процессов за счет ингибирования реак-
которых может развиться нейропротекторный
ции Фентона, и, как следствие, снижению
потенциал. В литературе встречаются данные, на
повреждения и гибели нейронов.
основании которых можно выдвинуть вышеука-
занное предположение, однако, таких работ ма-
При развитии нейродегенеративных заболева-
ло, и это требует более детальных эксперимен-
ний появляется астроцитарная дисфункция, обу-
тальных исследований. В работе [48] было пока-
словленная нарушением работы глутаматного
зано, что коменовая кислота подавляет
транспортера EAAT-1 [41]. При болезни Альцгей-
фокальный ответ нейронов на переживающих
мера Aβ 1-42 индуцирует глутаматную токсич-
срезах гиппокампа. Предварительная апплика-
ность за счет изменения функциональной актив-
ция срезов пикротоксином, являющимся анта-
ности обратного захвата глутамата из синаптиче-
гонистом рецепторов гамма-аминомасляной
ской щели
[42]. При рассеянном склерозе
кислоты, предотвращала тормозное действие
происходит подавление экспрессии генов, ответ-
коменовой кислоты. Можно предположить, что
ственных за синтез переносчика глутамата в оли-
меконовая кислота, схожая по строению с коме-
годендроцитах и астроцитах за счет повышения
новой кислотой также может являться агони-
провоспалительных факторов [43]. Вызванная на
стом рецепторов гамма-аминомасляной кисло-
фоне ишемического повреждении головного
ты и оказывать тем самым защитный эффект при
мозга деполяризация приводит к нарушению ра-
гиперстимуляции глутаматных рецепторов.
боты глутаматного транспортера и накоплению
возбуждающей аминокислоты в синаптической
щели [44]. Эксайтотоксичность и окислительный
ЗАКЛЮЧЕНИЕ
стресс являются взаимоусиливающими звеньями
Полученные в данном исследовании экспери-
одного патологического процесса. С одной сто-
ментальные данные о физико-химических свой-
роны, активация AMPA- и NMDA-рецепторов и
ствах меконовой кислоты и установленный в от-
Ca2+-каналов L-типа приводит к активации ряда
ношении данного соединения цитопротектор-
ферментов и вторичных мессенджеров, приводя-
ный и антиоксидантный эффект в экспериментах
щих к развитию воспалительного процесса и отя-
in vitro дает основания рассматривать данное ве-
гощению окислительного стресса. Например, ги-
щество как возможный нейропротектор и создает
перактивность Ca2+-зависимой n-NOS приводит
необходимые предпосылки для дальнейшего изу-
к гиперпродукции активных форм азота, таких
чения защитного действия меконовой кислоты, а
как оксид азота и высокотоксичный пироксинт-
также других представителей кислот гамма-пиро-
рит, и усилению интенсивности окислительных
нового ряда на ткани головного мозга при моде-
процессов в нейронах [45]. Высвобождение ара-
лировании различных нейродегенеративных про-
хидоновой кислоты в результате активации фос-
цессов. Полученные в работе данные о ее физи-
ко-химических свойствах могут быть полезны для
фолипазы А способствует выработке эйказаной-
синтеза и изучения биологических свойств новых
дов, стимулирующих провоспалительный ответ
координационных соединений на основе меко-
[46]. С другой стороны, повышенная продукция
новой кислоты.
свободных радикалов в поврежденных отделах
головного мозга приводит к повреждению гли-
альных клеток и, как следствие, еще более силь-
ФИНАНСИРОВАНИЕ РАБОТЫ
ному нарушению работы глутамат/глутамино-
вой системы и накоплению возбуждающей ами-
Работа выполнена при финансовой поддержке
нокислоты в синаптическом пространстве [47].
Кубанского научного фонда в рамках Конкурса
Снижение уровня гибели нейронов мозжечка и
научно-инновационных проектов, ориенти-
уровня цитозольного кальция в них на фоне глу-
рованных на коммерциализацию № НИП-20.1/15
таматной токсичности, установленное в нашей
и государственного задания ЮНЦ РАН
экспериментальной работе, может быть реали-
№ 122020100351-9.
зовано за счет прямого антиоксидантного эф-
фекта меконовой кислоты по механизму одно-
КОНФЛИКТ ИНТЕРЕСОВ
электронного переноса на радикальную частицу.
Таким образом, снижение интенсивности окис-
Авторы заявляют об отсутствии конфликта
лительного стресса МК может облегчить эксай-
интересов.
БИОФИЗИКА том 68
№ 1
2023
МЕКОНОВАЯ КИСЛОТА - ВОЗМОЖНЫЙ НЕЙРОПРОТЕКТОР
31
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
23. P. Güntzel, L. Forster, C. Schollmayer, et al., Org.
Prepar. Procedures Int., 50 (5), 512 (2018).
Настоящая работа не содержит описания ис-
следований с использованием людей и животных
24. I. A. Antipova, S. A. Mukha, and S. A. Medvedeva,
в качестве объектов.
Rus. Chem. Bull., 53 (4), 780 (2004).
25. Л. В. Шурыгина, А. А. Кравцов, С. В. Козин и др.,
Растительные ресурсы, 53 (2), 291 (2017).
СПИСОК ЛИТЕРАТУРЫ
26. F. Neese, WIREs Comput. Mol. Sci., 2, 73 (2011).
1.
А. Я. Шурыгин, Препарат Бализ (Периодика Куба-
ни, Краснодар, 2002).
27. A. D. Becke, Phys. Rev. A, 38, 3098 (1988).
2.
Л. В. Шурыгина, Э. И. Злищева и А. А. Кравцов,
28. S. Grimme, S. Ehrlich, and L. Goerigk, J. Comput.
Эксперим. клинич. фармакология, 81 (4), 3 (2018).
Chem., 32, 1456 (2011).
3.
Л. В. Шурыгин, Э. И. Злищев, А. Н. Кравцова
29. F. Weigend and R. Ahlrichs, Phys. Chem. Chem. Phys.,
и др., Бюл. эксперим биологии и медицины, 163
7, 3297 (2005).
(3), 325 (2017).
30. J. Tomasi, B. Mennucci, and R. Cammi, Chem. Rev.,
4.
А. А. Кравцов, А. Я. Шурыгин, Н. С. Скороход
105, 2999 (2005).
и др., Бюл. эксперим. биологии и медицины, 150
(10), 410 (2010).
31. С. В. Козин, А. А. Кравцов, А. А. Елкина и др.,
5.
Л. В. Шурыгина, Э. И. Злищева и А. А. Кравцов,
Биофизика, 64 (2), 362 (2019).
Бюл. эксперим. биологии и медицины, 165 (4), 457
32. A. Kravtsov, S. Kozin, A. Basov, et al., Molecules, 27
(2018).
(1), 243 (2022).
6.
Р. В. Кондратенко, А. Н. Чепкова, А. Я. Шурыгин
33. S. Anitha, S. Krishnan, K. Senthilkumar, et al., Mol.
и др., Бюл. эксперим. биологии и медицины, 136
Physics, 118, 17 (2020).
(11), 523 (2003).
7.
D. S. Kim, S. J. Kim, M. C. Kim, et al., Biol. Pharm.
34. J. Rimarcik, V. Lukes, E. Klein, et al., J. Mol. Struct.:
Bull., 35 (5), 666 (2012).
THEOCHEM, 952, 25 (2010).
8.
H. A. Oh, H. M. Kim, and H. J. Jeong, Int. Immuno-
35. V. M. Nurchi, G. Crisponi, J. I. Lachowicz, et al., J, In-
pharmacol., 11 (1), 39 (2011).
org. Biochem., 104 (5), 560 (2010).
9.
И. В. Рогачевский, В. Б. Плахова, И. Н. Домнин
36. E. P. Raven, P. H. Lu, T. A. Tishler, et al., J. Alzhei-
и др., Клинич. патофизиология, 1, 15 (2006).
mer's Dis., 37 (1), 127 (2013).
10.
Б. В. Крылов и др., Пат. РФ № 2322977 С1, Бюл.
37. B. Do Van, F. Gouel, A. Jonneaux, et al., Neurobiol.
изобретений, № 12 (2008).
Dis., 94, 169 (2016).
11.
N. N. Bukov, L. I. Ivashchenko, and V. T. Panyushkin,
Rus. J. Gen. Chem., 91 (4) 1 (2021).
38. J. J. Zhang, J. Du, N. Kong, et al., Ann. Translat. Med.,
9 (19), 1503 (2021).
12.
O. V. Vetrovoy, E. A. Rybnikova, and M. O. Samoilov,
Biochemistry, 82 (3), 392 (2017).
39. X. L. Fang, S. Y. Ding, X. Z. Du, et al., Front. Neurol.,
13.
L. Mezzaroba, D. F. Alfieri, and A. N. Colado Simão,
13 (2022).
Neurotoxicology 74, 230 (2019).
40. O. Y. Selyutina, P. A. Kononova, V. E. Koshman, et al.,
14.
J. Li, F. Cao, H.L. Yin, et al., Cell Death Dis., 11 (2),
Antioxidants (Basel), 11 (2), 376 (2022).
88 (2020).
41. S. Satarker, S. L. Bojja, P. C. Gurram, et al., Cells, 11
15.
P. Dusek, P. M. Roos, T. Litwin, et al., J. Trace Ele-
(7), 1139 (2022).
ments in Medicine and Biology, 31, 193 (2015).
42. A. Scimemi, J. S. Meabon, R. L. Woltjer, et al., J. Neu-
16.
X. Wei, X. Yi, X. H. Zhu, et al., Oxidative Medicine and
rosci., 33 (12), 5312 (2013).
Cellular Longevity, 2020, 1 (2020).
17.
R. J. Ward, D. T. Dexter, A. Martin-Bastida, et al., Int.
43. S. Garofalo, G. Cocozza, G. Bernardini, et al., Brain,
J. Mol. Sci., 22 (7), 3338 (2021).
Behavior, and Immunity, 105, 1 (2022).
18.
S. Entezari, S. M. Haghi, N. Norouzkhani, et al., J.
44. Z. Shen, M. Xiang, C. Chen, et al., Biomed. Pharma-
Toxicol., 2022, 1 (2022).
cother., 151 (2022).
19.
I. A. Mulder, E. T. van Bavel, H. E. de Vries, et al., Flu-
45. A. Jurcau and A. I. Ardelean, Biomedicines, 10 (3), 574
ids and Barriers of the CNS, 18 (1), 46 (2021).
(2022).
20.
B. Bargagna, L. Ciccone, S. Nencetti, et al., Molecules,
46. M. Regulska, M. Szuster-Głuszczak, E. Trojan, et al.,
26 (19), 6015 (2021).
Curr. Neuropharmacol., 19 (2), 278 (2021).
21.
S. Paul and E. Candelario-Jalil, Exp. Neurol., 335, 1
(2021).
47. M. Verma, B. N. Lizama, and C. T. Chu, Translat.
Neurodegeneration., 11 (1), 3 (2022).
22. С. В. Козин, А. А. Кравцов, С. В. Кравченко и др.,
Бюл. эксперим. биологии и медицины, 171 (5), 592
48. A. A. Khrapov, A. N. Chepkova, A. Y. Shurygin, et al.,
(2021).
Bull. Exp. Biol. Med., 125 (1), 53 (1998).
БИОФИЗИКА том 68
№ 1
2023
32
КОЗИН и др.
Meconic Acid Is a Possible Neuroprotector: Justification on In Vitro Experiments
and Its Physico-Chemical Properties
S.V. Kozin*, **, L.I. Ivashchenko*, A.A. Kravtsov*, **, L.V. Vasilyeva*, A.M. Vasiliev*, N.N. Bukov*,
A.A. Dorohova*, **, O.M. Lyasota*, **, A.V. Bespalov*, and S.S. Dzhimak*, **
*Kuban State University, Stavropolskaya ul. 149, Krasnodar, 350040 Russia
**Federal Research Center "Southern Scientific Center of the Russian Academy of Sciences",
prosp. Chekhova 41, Rostov-on-Don, 344006 Russia
Main representatives of gamma pyronic acid are meconic, comenic, chelidonic and kojic acid. It was found
that comenic acid exerts a neuroprotective effect, and chelidonic acid has a pronounced anti-inflammatory
effect. It was not studied whether meconic acid exhibits neuroprotective effects. The aim of this work was to
assess the neuroprotective potential of meconic acid, taking into accout its physicochemical properties,
using an in vitro model of ischemic stroke. Primary neuroglial culture was obtained from the cerebellum of
7-8-day-old Wistar rat pups by mechanical tissue dissociation. The protective effect of meconic acid on the
culture of cerebellar neurons was studied using the model of glutamate toxicity and oxygen-glucose depriva-
tion. Quantum mechanical calculations were used and experiments in the model system citrate-phosphate-
luminol were conducted by the method of chemiluminescent analysis to investigate the antioxidant activity
of meconic acid. The chelating properties of meconic acid with respect to Fe3+ in solutions were studied using
Job's method. Meconic acid has been found to have a protective effect in in vitro models of ischemia. Its action
leads to a decrease in the level of intracellular calcium and the restoration of the membrane potential of mi-
tochondria in a culture of cerebellar neurons under glutamate exposure, resulting in an increase in the per-
centage of living cells under oxygen-glucose deprivation. Meconic acid has a high calculated antioxidant po-
tential, confirmed experimentally. With an increase in the pH of the medium, stepwise binding of meconic
acid with Fe3+ occurs with the formation of complexes with different ligand/metal ratios. At physiological
pH, the composition of the resulting complex is 1 : 3. The obtained antioxidant, chelating, and cytoprotective
action of meconic acid provides a basis for further study of the possible neuroprotective properties of this
compound in in vivo experiments, and the data obtained in the work on its physicochemical properties can
be useful for the synthesis and study of new coordination compounds based on meconic acid.
Keywords: antioxidant activity, meconic acid, cerebellar neuron culture, glutamate toxicity, oxygen-glucose depri-
vation, neuroprotection, iron complexes
БИОФИЗИКА том 68
№ 1
2023