БИОФИЗИКА, 2022, том 67, № 1, с. 160-167
БИОФИЗИКА CЛОЖНЫX CИCТЕМ
УДК 57.085.23: 617-089.844
ПАССИВНЫЙ АСЕПТИЧЕСКИЙ КАЛЬЦИНОЗ ФИКСИРОВАННЫХ
ПЕРИКАРДИАЛЬНЫХ БИОМАТЕРИАЛОВ ОПОСРЕДОВАН
НАРУШЕНИЯМИ СТРУКТУРЫ И МИКРОАРХИТЕКТОНИКИ
ИХ ВНЕКЛЕТОЧНОГО МАТРИКСА
© 2022 г. А.И. Звягина*, А.И. Даль*, В.В. Минайчев*, О.А. Краснова*,**,
В.С. Акатов*, И.С. Фадеева*,**
*Институт теоретической и экспериментальной биофизики РАН,
142290, Пущино Московской области, Институтская ул., 3
**Пущинский государственный естественно-научный институт,
142290, Пущино Московской области, просп. Науки, 3
E-mail: fadeeva.iteb@gmail.com
Поступила в редакцию 09.09.2021 г.
После доработки 09.09.2021 г.
Принята к публикации 06.10.2021 г.
Изучен механизм пассивного (независимого от клеток реципиента) асептического кальциноза фик-
сированных глутеральдегидом перикардиальных материалов, используемых для изготовления био-
протезов клапанов сердца, а также определена зависимость интенсивности кальцификации от сте-
пени повреждения структуры и микроархитектоники их внеклеточного матрикса. Методом скани-
рующей электронной микроскопии исследован микрорельеф поверхности внутреннего серозного
слоя перикарда экспериментальных и контрольных материалов с определением степени деламина-
ции и интенсивности микроповреждений в зависимости от типа предимплантационной обработки.
Для определения склонности к асептическому кальцинозу фиксированных биоматериалов с ин-
тактным и поврежденным внеклеточным матриксом проведено исследование степени кальцифи-
лаксии образцов при их инкубации в модельных условиях нормокальциемии in vitro. Показана пря-
мая зависимость интенсивности кальцификации фиксированных биоматериалов от степени повре-
ждения их внеклеточного матрикса.
Ключевые слова: биоматериалы, ксеногенный перикард, сердечно-сосудистая хирургия, асептический
кальциноз, деламинация, внеклеточный матрикс.
DOI: 10.31857/S0006302922010173
(преимущественно ксеноперикарда), которые
Дисфункция клапанов сердца является тре-
применяются как для изготовления биопротезов
тьим по частоте сердечно-сосудистым заболева-
клапанов сердца, так и для различных рекон-
нием после ишемической болезни сердца и си-
стемной артериальной гипертензии [1-3]. При
структивно-восстановительных и клапан-сбере-
гающих операций [2, 4-6]. Несмотря на несо-
этом в большинстве случаев фармакотерапия по-
мненные преимущества биологических замени-
роков клапанов сердца совершенно неэффектив-
на и хирургическая замена поврежденного клапа-
телей клапанов сердца перед механическими,
на соответствующим функциональным замени-
склонность используемых биоматериалов к пато-
телем (трансплантатом или протезом клапана
логической асептической кальцификации (каль-
цинозу) в организме реципиента приводит к вы-
сердца) или реконструктивная операция по кор-
рекции клапанного порока сердца является един-
сокому проценту вторичных дисфункций био-
ственным способом лечения данной группы за-
протезов клапанов сердца и, следовательно,
болеваний [4]. В свою очередь, развитие антит-
необходимости высокотравматичных реопера-
ромбогенной хирургии клапанов сердца
[5]
ций, что связано с дополнительным риском ле-
привлекло особое внимание ученых к разработке
тального исхода для пациента [4, 6-8]. Таким об-
способов получения неиммуногенных биологи-
разом, разработка технологий получения биоло-
ческих материалов на основе донорских тканей
гических материалов, не подверженных
кальцинозу, по-прежнему является острой и вос-
Сокращениe: ГА - глутаровый альдегид.
требованной задачей.
160
ПАССИВНЫЙ АСЕПТИЧЕСКИЙ КАЛЬЦИНОЗ
161
В свою очередь, разработка эффективных тех-
кальциноза трансплантатов клапанов сердца,
нологий подавления способности биоматериалов
опосредованный повреждениями ультраструкту-
к развитию кальциноза должна базироваться на
ры их внеклеточного матрикса также применим
ясном понимании механизмов инициации дан-
по отношению к биопротезам клапанов сердца на
ного патологического процесса в организме ре-
основе ксеноперикарда.
ципиента. Однако на сегодняшний день патофи-
Таким образом, цель настоящей работы состо-
зиология дегенерации биопротезных клапанов
яла в том, чтобы оценить, насколько кальцифи-
изучена недостаточно, а триггеры асептического
кация тканей ксеноперикарда, используемого
кальциноза неизвестны [9]. При этом накоплено
для изготовления биопротезов клапанов сердца,
достаточно много экспериментальных данных,
определяется повреждениями его внеклеточного
указывающих на потенциальные механизмы
матрикса. Для достижения поставленной цели
кальциноза биологических протезов клапанов
исследовали степень повреждения поверхности
сердца. В частности, рассматриваются предполо-
внутреннего серозного слоя (p. serosum) фрагмен-
жения о связи инициации кальциноза фиксиро-
тов ксеноперикарда после стандартных и мат-
ванной ткани с компонентами погибших клеток
рикс-сберегающих протоколов децеллюляриза-
донора и апоптотическими тельцами [2, 10-13],
ции и сравнили полученные результаты со степе-
компонентами тканевого матрикса (коллагеном I
нью пассивной, независимой от клеток
типа, фибронектином, эластином) [14-17], каль-
реципиента кальцификации ткани (кальцифи-
цийсвязывающими белками (Gla-протеины,
лаксии) при инкубации образцов в модельных
остеокальцин, остеопонтин, остеонектин, фету-
средах, имитирующих внутреннюю среду орга-
ин-А) и фосфопротеинами [18, 19], щелочной
низма с нормальным содержанием кальция в сре-
фосфатазой [20, 21], липидами [22-24] митохон-
де (модельная нормокальциемия) in vitro.
дриями погибших клеток донора или погибаю-
щих на биопротезе клеток реципиента [25, 26] и
т.д. На основании клинических наблюдений так-
МАТЕРИАЛЫ И МЕТОДЫ
же установлено, что кальциноз интенсифициру-
Все исследуемые материалы изготавливали в
ется при молодом возрасте реципиента и повы-
лабораторных условиях с учетом требований,
шенных механических нагрузках на биопротез
предъявляемых к производству искусственных
[10].
клапанов сердца [30]. В качестве основного мате-
Одновременно с вышесказанным известно,
риала использовали бычий перикард, получен-
что фиксация биологических тканей таким
ный от половозрелых животных, имеющих соот-
кросс-сшивающим агентом как глутаровый аль-
ветствующие ветеринарные свидетельства. Пери-
дегид (ГА) также может способствовать кальци-
карды извлекали не позднее чем через 1 ч после
нозу имплантированной ткани [4, 10, 11, 13], од-
забоя животных и помещали в стерильный фи-
нако вариативность полученных клинических
зиологический раствор (0.9% NaCl) c добавлени-
данных от пациентов одной возрастной группы,
ем гентамицина (400 мкг/мл) и флуконазола
получивших биопротезы клапанов сердца,
(20 мкг/мл). После доставки в лабораторию при
фиксированные стандартным раствором ГА без
2-8°С (не позднее чем через 8 ч после забоя и из-
кэппирования, но подвергшиеся различным про-
влечения) нативный материал очищали физиче-
токолам децеллюляризации/девитализации, ука-
ски и отмывали от крови в физиологическом рас-
зывают на то, что непосредственно сам техноло-
творе с гепарином (5000 ЕД/100 мл, Московский
гический процесс предимплантационной обра-
эндокринный завод, Москва). После очищения и
ботки вносит существенный вклад в инициацию
отмывки от гепарина часть материалов хранили в
асептического кальциноза имплантированной
стерильном физиологическом растворе в каче-
ткани. Помимо вышесказанного известно, что
стве нативного нулевого контроля при 4°С (груп-
непосредственно стабилизированная ГА ткань
па К.0). Часть материалов подвергали стандарт-
бипротезов обладает контактным токсическим
ной химической стабилизации 0.625%-м раство-
эффектом, вследствие чего наблюдаемый на ран-
ром глутарового альдегида (Applichem GmbH,
них стадиях кальциноз является преимуществен-
Германия) с последующей процедурой децеллю-
но пассивным физико-химическим процессом и
ляризации в 1.0%-м растворе додецилсульфата
осуществляется без участия клеток реципиента
натрия (группа ЭК.1) (по ТУ 9444-003-01897446-
[4, 27]. Ранее мы установили, что повреждения
2011, данный способ обработки является самым
внеклеточного матрикса трансплантатов клапа-
распространенным и активно используется в
нов сердца, вызванные различными протоколами
клинической практике). Часть материалов под-
децеллюляризации, напрямую способствуют раз-
вергали щадящей децеллюляризации в растворе
витию кальцификации имплантированной ткани
липофильных детергентов низкой концентрации
вне зависимости от участия в данном процессе
по методике, описанной в работе [31], с последу-
клеток реципиента [25, 28, 29], и полагаем, что
ющей химической стабилизацией раствором мо-
предложенный ранее механизм асептического
номерного глутарового альдегида при комнатной
БИОФИЗИКА том 67
№ 1
2022
162
ЗВЯГИНА и др.
температуре (группа Э1.0). Часть материалов под-
Э2.1 - образцы, обработанные по протоколу
вергали также щадящей децеллюляризации в рас-
матрикс-сберегающей децеллюляризации с фик-
творе липофильных детергентов низкой концен-
сацией в полимеризованном ГА при температуре
трации (по аналогии с группой Э1.0), но химиче-
38°С, хранение в 4%-м растворе пропиленоксида.
скую стабилизацию проводили в растворе
Сканирующая электронная микроскопия. Для
полимеризованного ГА при 38°С с целью улучше-
оценки степени повреждения внеклеточного мат-
ния степени химической стабилизации ткани и
рикса образцов после каждого типа предимплан-
снижения количества реакционно способных
тационной обработки оценивали микрорельеф
групп ГА (группа Э1.1). Группы ЭК.1, Э1.0 и Э1.1
поверхности p. serosum перикардиальных матери-
после процесса химической стабилизации храни-
алов с помощью сканирующей электронной мик-
ли в стандартном общепринятом консервирую-
роскопии. Для анализа фрагменты образцов всех
щем растворе, представляющем собой 0.1% ГА в
исследуемых групп разрезали на квадратные пла-
20%-м растворе этилового спирта.
стинки площадью 1 см2 (для каждой группы n = 6)
Также часть образцов была обработана анало-
и предварительно замораживали в течение 12 ч
гично группе Э1.0, но после процесса химической
при -80°С с помощью низкотемпературного мо-
стабилизации в мономерном ГА дополнительно
розильника Premium U410 (New Brunsweek,
хранилась в 4%-м растворе пропиленоксида по
США). Затем замороженные образцы, закреп-
методике, описанной в работе [32] (группа Э2.0).
ленные в подвешенном состоянии на специаль-
Соответственно часть образцов была обработана
ных держателях карусельного типа, помещали в
по аналогии с группой Э1.1, но после процесса хи-
колбы лиофильной сушилки FreeZone
2.5 L
мической стабилизации в полимеризованном ГА
Benchtop Freeze Dry System (Labconco, США) и
при температуре 38°С дополнительно хранилась в
лиофилизировали в течение 24 ч. Непосредствен-
4%-м растворе пропиленоксида по вышеуказан-
но перед микроскопией высушенные образцы
ной методике (группа Э2.1). Данные группы (Э2.0
приклеивали на предметные столики специаль-
и Э2.1) были включены в эксперимент, поскольку
ным скотчем, столики закрепляли в держателе и
консервация в пропиленоксиде является доста-
напыляли пластинки частицами золота в вакуум-
точно распространенным методом хранения би-
ном распылителе Q150R ES (Quorum Technolo-
протезов клапанов сердца, но данные о влиянии
gies, Англия), после чего вентилировали для из-
такого способа хранения материалов на сохран-
бавления от излишка золотых частиц. После про-
ность матрикса и степень их кальцифилаксии в
боподготовки образцы быстро переносили в
литературе не представлены. Все манипуляции с
камеру электронного микроскопа VEGA3 (Tes-
материалами проводили в стерильных условиях
can, Чехия) и проводили съемку при давлении
ламинарного бокса класса IIа (Lamsystems, Рос-
7.3⋅10-2 Па в колонне и 1.5⋅10-1 Па в камере.
сия) с использованием стерильных растворов.
По завершении были получены следующие
Моделирование условий нормокальциемии
группы материалов сравнения:
in vitro. Для определения степени пассивной фи-
зико-химической минерализации биоматериалов
К.0 - нативный перикард, контроль срав-
после воздействия стандартных и матрикс-сбере-
нения;
гающих протоколов предимплантационной обра-
ЭК.1 - образцы, обработанные по стандартно-
ботки, образцы групп сравнения инкубировали в
му протоколу предимплантационной обработки,
модельных средах, имитирующих условия сыво-
включающему децеллюляризацию с фиксацией в
ротки крови и тканевой жидкости с нормальным
мономерном ГА и хранение в стандартном кон-
содержанием кальция и фосфатов. Известно, что
сервирующем растворе;
в условиях гиперкальциемии наблюдается уско-
Э1.0 - образцы, обработанные по протоколу
ренное и в том числе пассивное (независимое от
матрикс-сберегающей децеллюляризации с фик-
клеток реципиента) осаждение кальциевых депо-
сацией в мономерном ГА при комнатной темпе-
зитов на тканях бипротезов клапанов сердца [11,
ратуре, хранение в стандартном консервирующем
33]. При этом данные о влиянии нормальных
растворе;
концентраций кальция на степень кальцифилак-
Э1.1 - образцы, обработанные по протоколу
сии фиксированных перикардиальных материа-
матрикс-сберегающей децеллюляризации с фик-
лов в литературе практически не представлены.
сацией в полимеризованном ГА при температуре
В качестве модельной среды инкубации, имити-
38°С, хранение в стандартном консервирующем
рующей сыворотку крови, был выбран 5%-й
растворе;
раствор бычьего сывороточного альбумина фрак-
Э2.0 - образцы, обработанные по протоколу
ции V (стандартные референсные значения [34]
матрикс-сберегающей децеллюляризации с фик-
(Amresco, США)) в фосфатно-солевом буфере по
сацией в мономерном ГА при комнатной темпе-
рекомендациям Kiesendahl и др. [33] без ионов
магния с добавлением 2.5 мМ CaCl2 [33, 35, 36]
ратуре, хранение в 4%-м растворе пропиленок-
сида;
(Panreac Quimica, Испания)
БИОФИЗИКА том 67
№ 1
2022
ПАССИВНЫЙ АСЕПТИЧЕСКИЙ КАЛЬЦИНОЗ
163
Оценка степени повреждения/деламинации образцов
Группа
Степень повреждения после обработки в % от общей площади
поверхности p. serosum
К.0
0.8 ± 0.1%
ЭК.1
80.9 ± 8.9%*
Э1.0
12.1 ± 3.5%*
Э2.0
10.9 ± 2.1%*
Э1.1
26.1 ± 8.2%*, **
Э2.1
79.1 ± 5.5%*, ***
Примечание. * - р < 0.05 относительно контроля, ** - р < 0.05 относительно группы Э1.0, *** - р < 0.05 относительно группы
Э2.0.
Исследуемые материалы нарезали в ламинар-
AS FS (10 мг/дл) добавляли аликвоту соляной
ном боксе на фрагменты размером 6 × 4 × 1 мм
кислоты, равную аликвоте опытных образцов.
(n = 6 для каждой группы) и помещали в инкуба-
Статистический анализ. Результаты усредняли
ционный раствор в соотношении 1 : 30 (v/v).
по шести образцам и определяли среднеквадра-
Инкубацию проводили в шейкере-инкубаторе
тическую ошибку. Результаты исследований
ЕS-20/60 (BioSan, Латвия) в течение 6 недель при
представлены в виде среднего ± стандартная
30 об/мин и температуре 37°С. Замену среды на
ошибка среднего. Все эксперименты проводили
свежую осуществляли также в стерильных усло-
не менее чем в трех повторах (n ≥ 3). Статистиче-
виях каждые 48 ч.
скую значимость отличий определяли с помощью
Измерение минерализованного кальция методом
ANOVA с последующим множественным сравне-
абсорбционной спектроскопии. Содержание каль-
нием Холм-Cидака или критерия Манна-Уитни
ция во фрагментах тканей исследуемых групп
для двух групп сравнения, p ≥ 0.05.
определяли методом абсорбционной спектроско-
пии. Из различных областей нативных и обрабо-
танных материалов до и после инкубации в мо-
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
дельных средах получали фрагменты размером
2 × 2 мм (n = 6), которые затем высушивали в те-
Результаты, полученные с помощью сканирую-
чение 2 ч при 100°С в сухожаровом шкафу (Binder,
щей электронной микроскопии. Для всех групп был
Германия) и измеряли сухой вес образцов. Затем
детализированно изучен микрорельеф поверхно-
каждый высушенный фрагмент помещали в
сти p. serosum с оценкой степени повреждения/де-
0.5 мл 1 н HCl (для растворения минерализован-
ламинации образцов, выраженной в % от общей
ного кальция) на 24 ч при 20-25°С. В дальнейшем
площади анализа. Поверхность p. serosum пери-
проводили измерение количества минерализо-
кардиальных материалов является наиболее важ-
ванного кальция в растворе с помощью стандарт-
ной для оценки, поскольку подвергается основ-
ного набора для определения кальция Calcium AS
ным гидравлическим ударам тока крови и
FS Arsenazo III (DiaSys, Германия), используя
наибольшему механическому воздействию. Про-
планшетный спектрофлуориметр Infinity F200
центное содержание микроповреждений поверх-
(Tecan, Австрия). Расчет значений минерализо-
ности перикардиальных материалов оценивали
ванного кальция в образцах (в мкг кальция на мг
по оцифрованным изображениям поверхности
сухого веса ткани) проводили согласно инструк-
p. serosum (не менее десяти областей анализа с
ции производителя. Для расчета количества каль-
каждого образца), полученных при одинаковом
ция по показателям оптической плотности в
увеличении. Анализ проводили методом прямого
лунках с экспериментальными образцами ис-
подсчета участков перфорации, разволокнения и
пользовали уравнение для аппроксимации ка-
продольных микроразрывов поверхности и изме-
либровочной кривой. С целью исключения по-
рения площади оголения подлежащего под
грешности измерений оптической плотности
p. serosum коллагенового слоя. Оценку степени
комплексов кальция и Arsenazo III в лунках опыт-
повреждения проводили в сравнении с нативным
ных образцов как следствие использования соля-
контролем - фрагментами перикарда без какой-
ной кислоты (изменение рН раствора) при прове-
либо обработки (группы К.0). Результаты пред-
дении калибровки в лунки со стандартом Calcium
ставлены в таблице и на рис. 1 и 2.
БИОФИЗИКА том 67
№ 1
2022
164
ЗВЯГИНА и др.
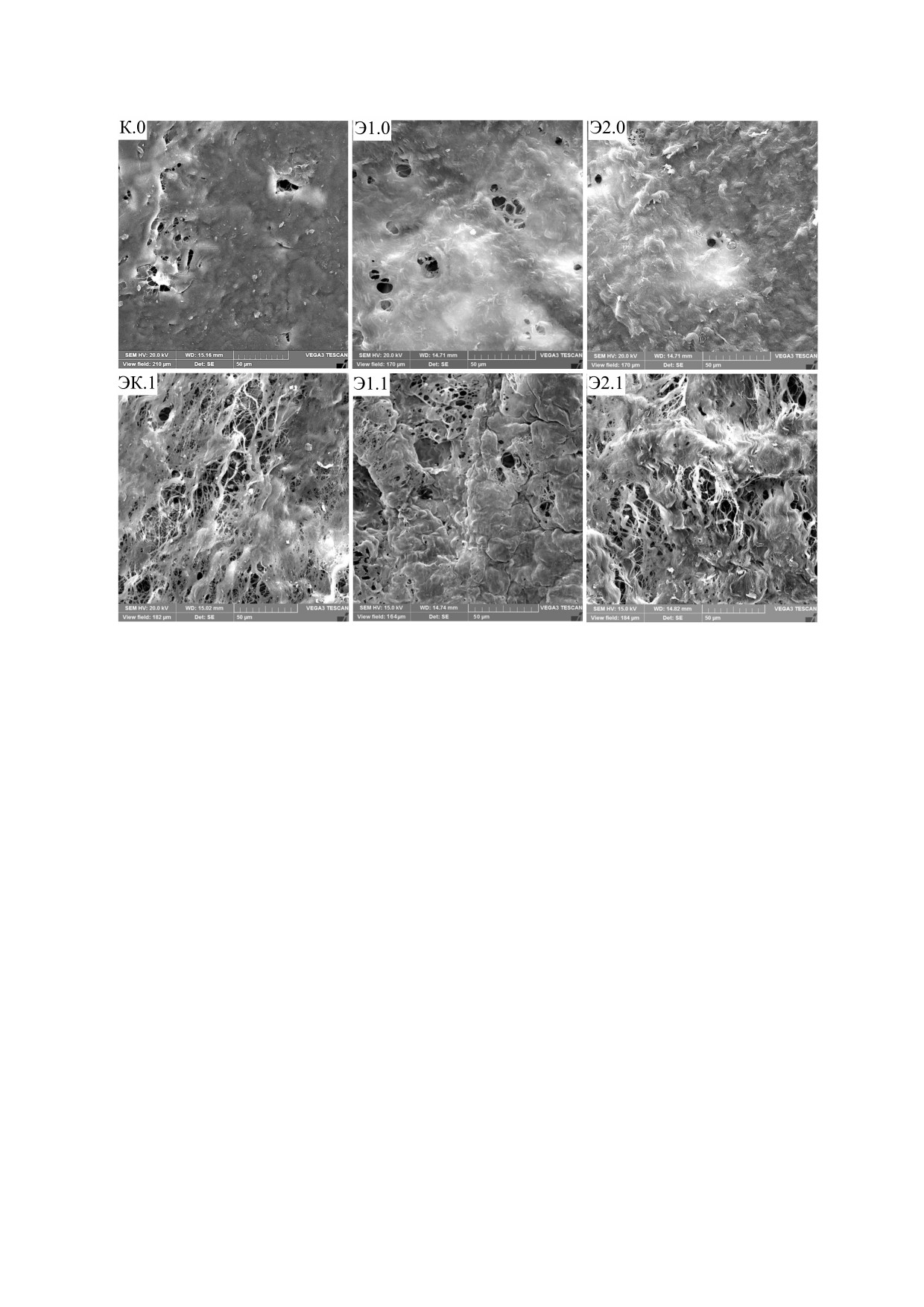
Рис. 1. Сканирующая электронная микроскопия поверхности p. serosum образцов контрольной и экспериментальных групп
фиксированных перикардиальных материалов после полного цикла предимплантационной обработки, общий план
(пояснения в тексте).
Было выявлено, что наименее поврежденной
повреждения наблюдается для образцов групп
по отношению к контролю является поверхность
Э1.0 и Э2.0, а наибольшая степень повреждения -
материалов групп Э1.0 и Э2.0, т. е. групп, обрабо-
для образцов ЭК.1 и Э2.1.
танных по протоколу матрикс-сберегающей де-
При большем увеличении в образцах группы
целлюляризации с последующей фиксацией в
нативного контроля выявлен надлежащий над
мономерном ГА при комнатной температуре;
поверхностью гладкий сиропообразный слой, по-
степень повреждения p. serosum образцов данных
крывающий сверху коллагеновый матрикс, пред-
групп составила 12.1 ± 3.5% и 10.9 ± 2.1% соот-
ставляющий собой гликозоаминогликаны ба-
ветственно. Более выраженная степень повре-
зальной ламины поверхности p. serosum. При
ждения - 26.1 ± 8.2% от всей площади образца -
сравнительном анализе обнаружено, что данный
наблюдалась для поверхности материалов группы
слой сохранен в образцах групп Э1.0, Э2.0 и ча-
Э1.1, обработанных в аналогии с группами Э1.0,
стично группы Э1.1, но практически полностью
но с последующей фиксацией в полимеризован-
отсутствует в образцах групп ЭК.1 и Э2.1 (рис. 2).
ном ГА при температуре 38°С. Наибольшая сте-
В группах ЭК.1 и Э2.1 повреждения гликоза-
пень повреждения наблюдалась для образцов
миногликанового слоя и деламинация достигали
групп ЭК.1 и Э2.1 и составила 80.9 ± 8.9% и
80% от площади всей исследованной поверхно-
79.1 ± 5.5% соответственно.
сти, при этом в подлежащем слое коллагенового
матрикса дополнительно наблюдались признаки
На рис. 1 представлены сводные микрофото-
частичного продольного разволокнения и микро-
графии типичных поверхностей p.serosum образ-
разрывы коллагеновых волокон.
цов ксеноперикарда после различных вариантов
предимплантационной обработки и хранения,
Полученные данные свидетельствуют о том,
полученные методом сканирующей электронной
что стандартная децеллюляризация 1%-м раство-
микроскопии. Видно, что наименьшая степень
ром додецилсульфата натрия обладает выражен-
БИОФИЗИКА том 67
№ 1
2022
ПАССИВНЫЙ АСЕПТИЧЕСКИЙ КАЛЬЦИНОЗ
165
Рис. 2. Сканирующая электронная микроскопия поверхности образцов p. serosum и подлежащего коллагенового слоя
контрольной и экспериментальных групп фиксированных перикардиальных материалов после полного цикла
предимплантационной обработки, крупный план (пояснения в тексте).
ным повреждающим воздействием на внеклеточ-
минерализации матрикса была свойственна для
ный матрикс p. serosum образцов, при этом выяв-
образцов, имевших наибольшую же степень по-
лено, что даже при использовании матрикс-
вреждения внеклеточного матрикса. Сводные ре-
сберегающей децеллюляризации дальнейшая
зультаты измерения минерализованного кальция
фиксация в полимеризованном ГА при темпера-
и оценки степени повреждения ВКМ групп срав-
туре 38°С оказывает выраженное повреждающее
нения представлены на рис. 3.
воздействие на внеклеточный матрикс перикар-
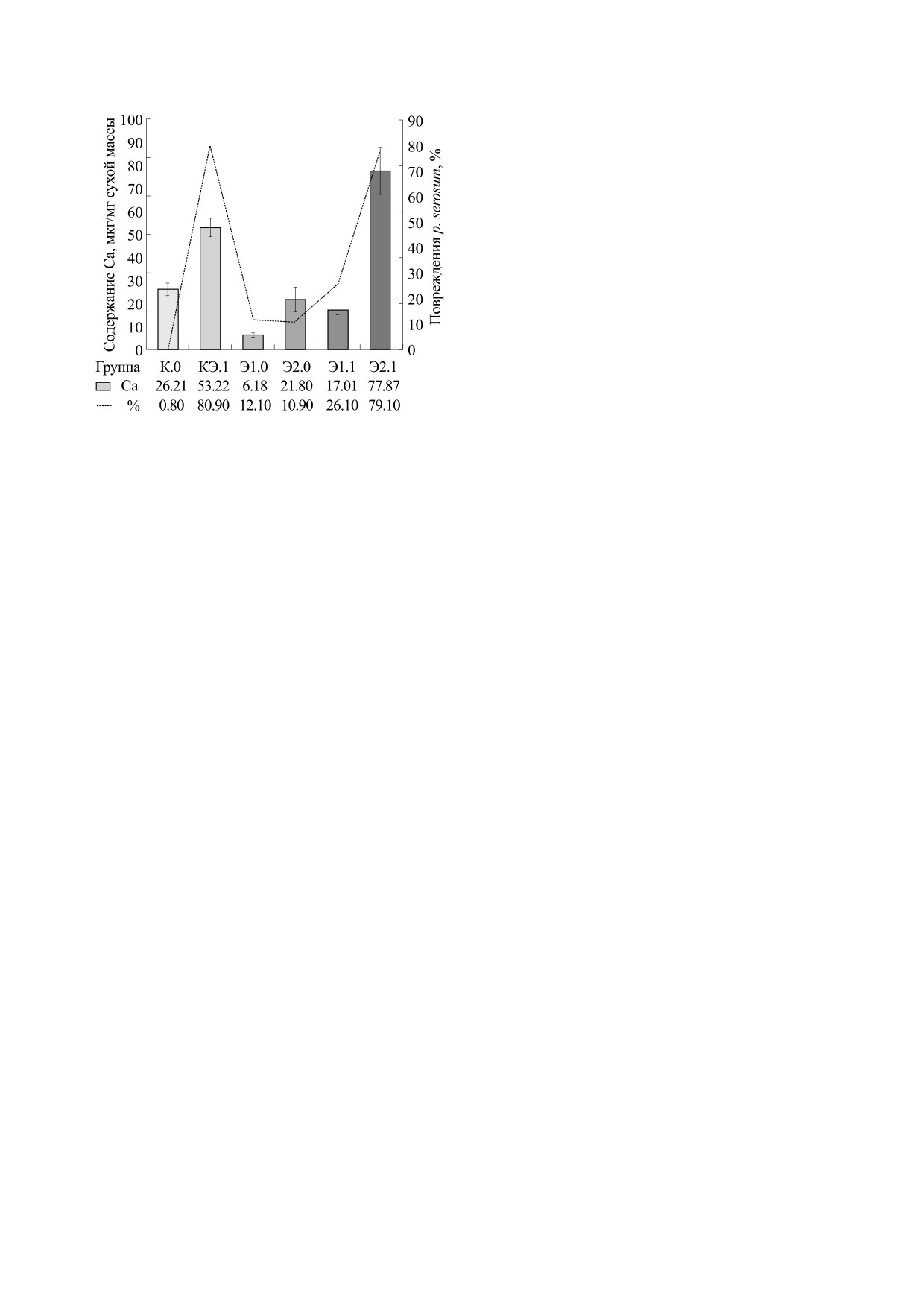
Из рисунка видно, что нативный контроль ми-
диальных материалов. При этом значимая и до-
нерализовался достаточно активно, что объясня-
стоверная разница в степени повреждения для
ется наличием в матриксе перикарда клеток до-
групп Э1.1 и Э2.1 свидетельствует о том, что кон-
нора и клеточного дебриса, которые, как извест-
сервация в 4%-м растворе пропиленоксида после
но, могут выступать центрами инициации
процедуры химической стабилизации в ГА при
пассивного кальциноза [2, 10-13]. В случае мате-
температуре
38°С дополнительно повреждает
риалов, подвергшихся децеллюляризации (удале-
внеклеточный матрикс материалов.
нию клеток донора) выявлена прямая корреля-
ция между степенью повреждения внеклеточного
Результаты измерения кальция. Способность
матрикса и интенсивностью пассивного осажде-
материалов пассивно осаждать на себе фосфаты
ния минерализованного кальция на компонентах
кальция (степень кальцифилаксии) исследовали
внеклеточного матрикса.
в модельных условиях in vitro при инкубации в
растворах, имитирующих сыворотку крови с нор-
Выявленная достоверная разница (p < 0.001)
мальным содержанием кальция. Через шесть не-
между нативным контролем (К.0) и группой Э1.0
дель инкубации количество адсорбированного
свидетельствует о том, что матрикс-сберегающая
кальция на материалах измеряли спектрофото-
децеллюляризация с последующей фиксацией в
метрически. Выявлено, что наибольшая степень
ГА при комнатной температуре в значительной
БИОФИЗИКА том 67
№ 1
2022
166
ЗВЯГИНА и др.
фиксации ткани (предположительно, использо-
вание нефизиологической температуры в 38°С)
способствуют повреждению ультраструктуры
внеклеточного матрикса и абсорбции фосфатов
кальция на его компонентах.
ЗАКЛЮЧЕНИЕ
Таким образом, полученные нами результаты
свидетельствуют, что пассивная физико-химиче-
ская минерализация химически стабилизирован-
ных глутеральдегидом ксеноперикардиальных
материалов, используемых для изготовления
биопротезов клапанов сердца, напрямую зависит
от степени повреждения их внеклеточного мат-
рикса вследствие процесса предимплантацион-
ной обработки. Дополнительно выявлено, что
консервация и хранение фиксированного ГА
Рис. 3. Сводный график степени кальцифилаксии кон-
биоматериала в 4%-м растворе пропиленоксида
трольной и экспериментальных групп фиксированных
может дополнительно способствовать осажде-
перикардиальных материалов после 45 суток инкуба-
нию фосфатов кальция на компонентах внекле-
ции в модельной среде, имитирующей сыворотку крови
точного матрикса материалов и что данное явле-
в условиях нормокальциемии, в сравнении со степенью
ние требует дополнительных детализированных
повреждения p. serosum данных групп, выраженной в
исследований, поскольку влияние консервирую-
процентах.
щих растворов на степень кальцифилаксии пери-
кардиальных материалов является практически
не изученным.
степени подавляет способность химически-ста-
билизированного материала абсорбировать на се-
бе фосфаты кальция. При этом выявленная до-
БЛАГОДАРНОСТИ
стоверная разница в степени кальцификации
между группами К.0 и КЭ.1 (p < 0.001), а также
При выполнении работы была использована
группами К.0, КЭ.1 и Э1.0 (p < 0.001) отчетливо
приборная база Центра коллективного пользова-
свидетельствует о том, что процесс матрикс-сбе-
ния ИТЭБ РАН.
регающей децеллюляризации является определя-
ющим этапом предимплантационной обработки
перикардиальных материалов для придания им
ИCТОЧНИКИ ФИНАНCИPОВАНИЯ
свойства кальциноз-резистентности.
Работа выполнена при финансовой поддержке
Российского фонда фундаментальных исследова-
При этом статистически достоверная разница
ний в рамках научного проекта № 20-315-90101.
между группами Э1.0 и Э2.0 (p < 0.05) и группами
Э1.1 и Э2.1 (p < 0.05), обработанных с той лишь
разницей, что группы Э2.0 и Э2.1 хранились в
КОНФЛИКТ ИНТЕРЕСОВ
консервирующем 4%-м растворе пропиленокси-
да, свидетельствует о том, что либо непосред-
Авторы заявляют об отсутствии конфликта
ственно технологический процесс консервации,
интересов.
либо процесс перехода пропиленоксида в пропи-
ленгликоль могут способствовать дополнитель-
ному повреждению внеклеточного матрикса либо
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
образованию дополнительных реакционных
Настоящая работа не содержит описания ка-
групп, способствующих осаждению фосфатов
ких-либо исследований с использованием людей
кальция на компонентах внеклеточного матрик-
и животных в качестве объектов.
са. Это требует отдельных детализированных ис-
следований. В свою очередь, выявленная досто-
верная разница в степени кальцификации
СПИСОК ЛИТЕРАТУРЫ
(p < 0.01) между группами Э1.0 и Э1.1, отличаю-
1. B. R. Lindman, M.-A. Clavel, P. Mathieu, et al., Nat.
щихся способом химической стабилизации в мо-
Rev. Dis. Primers 3 (2), 16006 (2016).
номерном (Э1.0) и полимеризованном (Э1.1) глу-
теральдегиде также свидетельствует о том, что не-
2. О.Б. Аникеева, О.В. Павленко, С.Н. Титов и др.,
посредственно
технологический
процесс
Аналитич. вестн. 44, 597 (2015).
БИОФИЗИКА том 67
№ 1
2022
ПАССИВНЫЙ АСЕПТИЧЕСКИЙ КАЛЬЦИНОЗ
167
3.
А. Карпантье, Реконструктивная хирургия клапа-
19. H. A. Baba, M. Deiwick, D. Breukelmann, et al.
нов сердца по Карпантье: от анализа клапана к его
Pathologe 19 (6), 420 (1998).
реконструкции (Логосфера, М., 2019).
20. E. Jorge-Herrero, P. Fernández, N. de la Torre, et al.,
4.
D. Dvir, T. Bourguignon, C. M. Otto, et al., Circula-
Biomaterials 15 (10), 815 (1994).
tion 137 (4), 388 (2018).
21. R. Shetty, P. Pibarot, A. Audet, et al., Eur. J. Clin. In-
5.
B. Zhang, E. Salaun, N. Côté, et al., J. Am. Coll. Car-
vest. 39 (6), 471 (2009).
diol. 76 (15), 1737 (2020).
22. В. С. Акатов, И. С. Фадеева, А. В. Чеканов и др.,
6.
P. R. Vogt, H. Brunner-LaRocca, P. Sidler et al., Eur.
Биофизика 55 (5), 937 (2010).
J. Cardiothorac. Surg. 17 (2), 134 (2000).
23. В. С. Акатов, Н. И. Рындина, Р. М. Муратов и др.
7.
T. R. G. Cartlidge, M. K. Doris, S. L. Sellers, et al., J.
Докл. РАН 406 (6), 832 (2006).
Am. Coll. Cardiol. 73 (10), 1107 (2019).
24. E. Gendler, S. Gendler, and M. E. Nimni, J. Biomed.
8.
F. J. Schoen and R. J. Levy, Ann. Thorac. Surg. 79 (3),
Mater. Res. 18 (7), 727 (1984).
1072 (2005).
25. В. С. Акатов, Кальцификация трансплантатов
9.
E. Aikawa and M. C. Blaser, Arterioscler. Thromb.
клапанов сердца и сосудов: механизмы кальцифика-
Vasc. Biol. 41 (1), 117 (2021).
ции и ее предотвращение (Akademikerverlag Publ.,
10.
F. Ghadially, Ultrastruct. Pathol. 25, 243 (2001).
Saarbrucken, 2012).
11.
K. E. Watson, F. Parhami, V. Shin, et al., Arterioscler.
26. И. С. Фадеева, Дис
канд. биол. наук (ИТЭБ
Thromb. Vasc. Biol. 18, 1964 (1998).
РАН, Пущино, 2013).
12.
J. S. Lee, D. M. Basalyga, A. Simionescu, et al., Am.
27. ГОСТ 26997-2002 Клапаны сердца искусствен-
J. Pathol. 168 (2), 490 (2006).
ные. Общие технические условия (с попр. ИУС N
6-2004) (2004).
13.
M. A. Bowler and W. D. Merryman, Cardiovasc.
Pathol. 24 (1), 1 (2015).
28. И. С. Фадеева, Патент РФ №2678966, № 4 (2019).
14.
M. T. Bailey, S. Pillarisetti, H. Xiao, et al., J. Biomed.
29. W. M. L. Neethling, Patent WO 2013/067598 Al
Mater. Res A 66 (1), 93 (2003).
(2013).
15.
W. Jahnen-Dechent, A. Heiss, C. Schäfer, et al., Circ.
30. N. Kiesendahl, C. Schmitz, A. von Berg, et al., Ann.
Res. 108 (12), 1494 (2011).
Biomed. Eng. 48, 282 (2020).
16.
M. Santin, W. Rhys-Williams, J. O’Reilly, et al., J. R.
31. В. М. Лифшиц, Лабораторные тесты у здоровых
Soc. Interface 3 (7), 277 (2006).
людей (Триада-Х, М., 2004).
17.
M. Hui and H. C. Tenenbaum, Anat. Rec. (New
32. J. J. Grzesiak and M. D. Pierschbacher, J. Clin. Invest.
Anat.). 253, 91 (1998).
95 (1), 227 (1995).
18.
P. A. Price, D. Toroian, and W. S. Chan, J. Biol.
33. P. A. Price, W. S. Chan, and D. M. Jolson, Arterio-
Chem. 284 (7), 4594 (2009).
scler. Thromb. Vasc. Biol. 26 (5), 1079 (2006).
Passive Aseptic Calcification of Fixed Pericardial Biomaterials Is Mediated by Damage
to the Structure and Microarchitectonics of Its Extracellular Matrix
A.I. Zvyagina*, A.I. Dal*, V.V. Minaychev*, O.A. Krasnova*, **, V.S. Akatov*, and I.S. Fadeeva*, **
*Institute of Theoretical and Experimental Biophysics, Russian Academy of Sciences,
Institutskaya ul. 3, Pushchino, Moscow Region, 142290 Russia
**Pushchino State Natural Science Institute, prosp. Nauki 3, Pushchino, Moscow Region, 142290 Russia
Our research focused on understanding the mechanism of passive (independent of recipient cells) aseptic cal-
cification of pericardial materials fixed with gluteraldehyde used to produce bioprosthetic heart valves. Also,
the dependence of the intensity of calcification on the degree of damage to the structure and microarchitec-
tonics of their extracellular matrix was determined. The microrelief of the surface of p. serosum of experimen-
tal and control materials was studied by scanning electron microscopy. The degree of delamination was esti-
mated and the intensity of micro-injuries was evaluated depending on the type of preimplantation treatment.
In order to assess the propensity for aseptic calcinosis of fixed biomaterials with intact and damaged extracel-
lular matrix, the degree of calciphylaxis of samples during their incubation under model conditions of nor-
mocalcemia in vitro was investigated. It was shown that the intensity of calcification of fixed biomaterials was
in direct dependence on the degree of damage to their extracellular matrix.
Keywords: biomaterials, xenogenic pericardium, cardiovascular surgery, aseptic calcification, delamination, ex-
tracellular matrix
БИОФИЗИКА том 67
№ 1
2022