Коллоидный журнал, 2022, T. 84, № 6, стр. 768-779
Фазовые превращения в системе ПАН–N-метилморфолин-N-оксид–вода
Е. Э. Пальчикова 1, *, И. С. Макаров 1, М. В. Миронова 1, М. И. Виноградов 1, Л. К. Голова 1, В. Г. Куличихин 1
1 Институт нефтехимического синтеза им. А.В. Топчиева РАН
119991 Москва,
Ленинский пр., 29, Россия
* E-mail: shatokhina@ips.ac.ru
Поступила в редакцию 24.04.2022
После доработки 06.06.2022
Принята к публикации 29.06.2022
- EDN: NWTZPH
- DOI: 10.31857/S0023291222600055
Аннотация
Методом оптической интерферометрии исследованы массообменные процессы, протекающие при растворении тройного сополимера ПАН, и установлены предельные концентрации растворов сополимера в различных кристаллогидратных формах N-метилморфолин-N-оксида (NMMO). С помощью методов спектра мутности, интерферометрии и оптической микроскопии изучено влияние природы осадителя на фазовые превращения системы в процессе коагуляции раствора и определены осадительные числа при введении в разбавленные растворы ПАН воды и водных растворов NММО (20–50 мас. %). Для водного коагулянта осадительное число для раствора ПАН в NMMO почти в 4 раза ниже соответствующего значения для традиционных растворов ПАН в ДМСО и ДМФА, что обусловлено высоким сродством NMMO к воде. Анализ диффузионных процессов при контакте раствора ПАН с коагулянтами позволила выявить условия получения практически бездефектной пленки ПАН, которые могут быть перенесены на реальные процессы формования. С этой точки зрения, оптимальными осадителями растворов ПАН являются водные растворы, содержащие порядка 20% NMMO, в то время как 50%-ные растворы осадителями не являются.
ВВЕДЕНИЕ
Волокнообразующие сополимеры на основе акрилонитрила (ПАН) пользуются высоким спросом в различных областях народного хозяйства и техники. Прежде всего, это текстильная промышленность, где нет ни одного шерстеподобного материала, не содержащего ПАН. В связи с этим, проблеме получения волокон ПАН уделяется большое внимание в технической литературе. Особенностью ПАН является его неплавкость, что делает необходимым его растворение в удобных для производства волокон растворителях, изучение свойств прядильных растворов, выбор оптимального состава осадительной ванны, анализ фазовых процессов, происходящих при коагуляции струй растворов в ходе трансформации в готовые волокна, температурно-деформационные режимы формования и т.д. Таким образом, в ряду проблем, связанных с переработкой ПАН в формованные изделия, одно из важнейших мест занимает природа используемого растворителя. Наибольшее применение получили водно-солевые [1] и такие апротонные растворители, как ДМСО, ДМФА, ДМАА и др. [2].
Поиски более эффективных растворителей продолжаются и по настоящее время. К числу новых растворителей ПАН можно отнести ионные жидкости [3, 4], а также, как впервые показано в наших исследованиях [5, 6], высокодонорный растворитель – N-метилморфолин-N-оксид (NMMO). Главным преимуществом последнего является возможность получения высококонцентрированных формовочных растворов ПАН. Эффективность взаимодействия NММО с ПАН обеспечивает наличие в молекуле NММО семиполярной N → О связи с двумя неподеленными электронными парами на атоме кислорода, способными взаимодействовать с двумя протон-содержащими или полярными группами. Однако, благодаря высокой электронодонорной активности N → О группы, NMMO легко образует и кристаллогидраты: моногидрат с Tпл = 76°С, бигидрат с Tпл = 28°С, а также серию сесквигидратов с промежуточными точками плавления, характеризующиеся различной растворяющей способностью. Казалось бы, наличие воды в растворителе благоприятно для растворения только гидрофильных полимеров, но оказалось, что NMMO растворяет и гидрофобные полиэфиры, и полиамиды, и сополимеры на основе акрилонитрила [7]. По-видимому, основным в механизме растворения является не только разрушение имеющихся в полимерах Н-связей, но и влияние N-оксидной группы на процесс перераспределения электронной плотности взаимодействующих полярных групп разных макромолекул в пользу формирования соответствующих связей с молекулами растворителя.
Основными способами формования ПАН волокон из растворов в традиционных растворителях являются мокрый, в котором фильера погружена в осадитель [8, 9], сухой (без использования осадителя), когда струи прядильного раствора попадают в нагретую шахту, где растворитель испаряется и формируются волокна [10], сухо-мокрый (сформировавшиеся на выходе из фильеры струи раствора проходят через воздушный зазор и далее попадают в ванну с осадителем) [11] и, недавно разработанный в ИНХС РАН, механотропный [12], в котором распад раствора на фазы происходит за счет интенсивного растяжения свободных струй прядильного раствора.
В промышленной практике наибольшее распространение получили мокрый и сухо-мокрый способы формования ПАН волокон [13]. Формование волокон этими способами подразумевает коагуляцию раствора при его контакте с нерастворителем (осадителем) и формирование гель-волокна, способного к фильерной и ориентационной вытяжкам, в ходе которых удаляется растворитель и формируется твердое волокно. Массообменные процессы в осадительной ванне являются одной из основных стадий, где формируется структура и морфология будущих волокон или пленок [14].
К числу факторов, позволяющих регулировать скорость и глубину взаимодействия осадителя с раствором, относятся: химическая природа полимера, состав раствора и его реологические свойства, природа осадителя, температура, концентрация раствора и др. [15–18]. Как показано многочисленными исследованиями, ключевую роль в поведении полимерных растворов при формовании играет эволюция фазового равновесия полимерных систем [19]. Так, в работах [20–22] предложено использование топологического анализа фазовых равновесий полимерных систем и рассмотрен принцип взаимной независимости различных типов равновесия. В простейшем случае, эволюцию фазовых превращений при контакте раствора с коагулянтом оценивали с позиций фазового равновесия бинарной системы полимер-растворитель, описываемого бинодалью. Переход системы из состояния истинного раствора в двухфазную область, сопровождаемый гелеобразованием, происходит за счет изменения параметра взаимодействия Флори−Хаггинса, вызываемого присутствием нерастворителя (осадителя) или изменением температуры [23, 24].
В этих условиях происходит распад раствора на разбавленную и концентрированную по полимеру фазы. Формально, при более медленном росте концентрированной фазы формируется гель, который представляет собой совокупность двух равновесных фаз с незавершенным фазовым разделением. При более быстром росте концентрированной фазы происходит полный распад системы на фазы с их макроразделением, что может приводить к потере сплошности материала. Таким образом, в процессе коагуляции струй раствора существенное влияние на процессы распада на фазы, форму и размеры фрагментов образующихся фаз оказывают термодинамика и кинетика фазовых превращений, создающая предпосылки для формирования различных промежуточных физических форм, как то: незавершенный фазовый распад (образование гелей-студней), жидкофазное расслоение, кристаллизация либо полимера, либо растворителя, и т.д. [21].
Эти основополагающие представления об эволюции фазового состояния растворов были перенесены на формование волокон из растворов полимеров и легли в основу интерпретации многочисленных экспериментальных данных. Так, в работах по изучению фазовых превращений в тройных системах ПАН–растворитель (ДМСО, ДМФА)–осадитель [25, 26] достаточно подробно изучены массообменные процессы при взаимодействии раствора с коагулянтом, приводящие к изменению фазового состояния трехкомпонентной композиции и формирование первичной структуры пленки/волокна.
Так как NMMO является и наиболее популярным в настоящее время растворителем целлюлозы и широко используется в технологической практике, то некоторые аспекты формования целлюлозных и ПАН волокон оказываются общими и поэтому могут быть сопоставимыми. Анализ процесса коагуляции растворов целлюлозы в NMMO разными коагулянтами была проведена в работах [27–29], в которых на основании двойных фазовых диаграмм была показана разница в кинетике осаждения в гомогенном и гетерогенном режимах, регулируемых температурой коагулянта. Оценка “жесткости” и “мягкости” процесса осаждения позволила построить гипотетическую диаграмму состояния с суперпозицией аморфного и кристаллического равновесий.
В этой связи чрезвычайно важным является изучение и анализ фазовых превращений в системе ПАН−NMMO−осадитель, начиная от получения растворов в различных кристаллогидратах NММО до осаждения при контакте с осадителями различной термодинамической афинности (сродства) по отношению к растворителю, что позволит в дальнейшем направленно выбирать состав осадительных ванн, обеспечивающих формирование однородной и способной эффективно деформироваться и ориентироваться первичной морфологии. Именно этим вопросам и посвящена данная работа.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали тройной сополимер состава: 93.0% акрилонитрила, 5.7% метилакрилата и 1.3% итаконовой кислоты (базовый сополимер волокна Нитрон, ООО “Саратоворгсинтез”). В качестве прямого растворителя ПАН использовали N-метилморфолин-N-оксид (Demochem, Китай), с содержанием воды 13.3% – моногидратная форма (МГ NММО) и 10% – высокоплавкая сесквигидратная форма (ВП NММО), с температурами плавления ~76 и ~120°C соответственно.
Содержание воды в NММО определяли с помощью методов титрования по Фишеру (ЭК-СПЕРТ-007М, Россия), а также по точке плавления растворителя с помощью поляризационной микроскопии (Boetius, VEB Kombinat Nadema, бывшая ГДР) и метода дифференциальной сканирующей калориметрии (DSC 2920 (TA Instruments, США)).
Для определения т.н. осадительных чисел проводили измерения коэффициентов пропускания растворов с добавками осадителя в диапазоне длин волн 315–980 нм использовали фотоэлектрический колориметр КФК-2 (ПО “Загорский оптико-механический завод”, Россия). Основная абсолютная погрешность колориметра при измерении коэффициентов пропускания не более ±1%. Для задания и поддержания температуры в рабочей камере колориметра использовали электрическую нагревательную поверхность, температуру которой контролировали с помощью термопары. Исследования проводили при Т = 100°С.
Контроль за содержанием растворителя в осадительных составах осуществляли по величине показателя преломления раствора NMMO в воде, определяемой с помощью рефрактометра [30].
Растворимость ПАН в NММО и изменение фазового состояния бинарной системы полимер-растворитель изучали методом оптической интерферометрии в интервале температур от 70 до 120°C. Данный метод позволяет регистрировать процесс взаимодиффузии растворителя и полимера. Пленку ПАН и NММО приводили в контакт в клиновидном зазоре с двухгранным углом 2°, образованном двумя полупрозрачными стеклами с высокой отражательной способностью. Момент соприкосновения расплавленного NMMO с пленкой толщиной 93 мкм, наблюдаемый в микроскопе, считали началом процесса взаимодействия компонентов.
Монохроматический лазерный луч при прохождении через ячейку генерирует две интерференционные картины, присущие ПАН и NММО, разделенные фазовой границей. При знании показателей преломления композиций анализ профилей концентрации в диффузионной зоне позволяет рассчитать параметры диффузионного процесса и по определенным граничным концентрациям построить фазовые диаграммы. Аналогичную процедуру проводили и для моделирования процесса формования волокон и пленок, наблюдая за диффузионным массообменом между раствором ПАН и осадителем. Методика проведения эксперимента и обработка интерферограмм не отличались от традиционных [31, 32]. Эксперименты проводили в режиме ступенчатого нагрева и охлаждения.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Особенности процесса растворения тройного сополимера ПАН в различных кристаллогидратах NММО были изучены с помощью метода интерферометрии при 120°С в температурной области, лежащей выше температуры плавления используемых растворителей – МГ NММО и ВП NММО (сесквигидрата), т.е. выше кривой ликвидуса, согласно фазовой диаграмме системы NММО–вода, представленной на рис. 1.
Подробный анализ фазового равновесия в системе NMMO−вода был выполнен методами поляризационной микроскопии и ДСК в [33]. Точки, соответствующие полному исчезновению кристаллической фазы, образуют линию ликвидуса. Кроме однофазной области L, где происходит полная взаимная растворимость NMMO и воды, на фазовой диаграмме наблюдаются несколько двухфазных областей: (L + BH) – равновесие между насыщенным раствором и бигидратом NMMO, (L + MH) – равновесие между насыщенным раствором и моногидратом NMMO, (L + AS) – равновесие между насыщенным раствором и безводным растворителем, (BH + MH) – смесь кристаллов бигидрата и моногидрата NMMO и (MH + AS) – смесь кристаллов моногидрата и безводного растворителя. Ход линии ликвидуса и положение линии солидуса, соответствующей композиции (MH – BH), позволяет ожидать инконгруентное плавление с разложением кристаллогидратов NMMO.
На рис. 2 представлены интерферограммы, иллюстрирующие формирование зон взаимодиффузии в системе ПАН–МГ NММО и ПАН–ВП NММО. В зоне контакта компонентов – жидкого МГ ММО и оптически прозрачной твердой пленки ПАН формируется фазовая граница (Ф). Зоны I и IV соответствуют областям 100%-ных компонентов, зоны II и III – областям диффузии ПАН в МГ NММО и МГ NММО в ПАН, соответственно. Обращает на себя внимание большая ширина диффузионной области со стороны растворителя, которая, наряду с большими загибами интерференционных полос, свидетельствуют о высокой скорости проникновения полимера в растворитель, т.е. процесс взаимодиффузии является несимметричным. С увеличением времени контакта угол наклона полос уменьшается.
Рис. 2.
Интерферограммы систем ПАН–МГ NММО (а, б) и ПАН–ВП NММО (в, г) через 1 (а, в) и 40 (б, г) мин после контакта компонентов, Т = 120°С.

Количественная интерпретация интерферограмм с учетом частичной совместимости компонентов и температурных зависимостей показателей преломления позволила построить профили распределения концентрации в диффузионной зоне для систем ПАН–МГ NММО и ПАН–ВП NММО при температуре 120°С (рис. 3).
Рис. 3.
Профили распределений концентраций в системах ПАН–МГ NММО (а) и ПАН–ВП NММО (б) при температуре 120°С. Ф – фазовая граница, II – область диффузии ПАН в NММО, III – области диффузии NММО в ПАН.

Согласно полученным данным, предельная концентрация ПАН в МГ NММО равна 15%, а в высокоплавком NММО – 56%. Полученные значения находятся в хорошем соответствии с величинами предельной растворимости ПАН в используемых гидратах NММО [34].
По температурно-временным зависимостям составов сосуществующих фаз, определенным, в качестве примера, на расстоянии 0.2 мм от фазовой границы, были построены кривые растворимости ПАН при 120°С в гидратах NММО, представленные на рис. 4. Отдельно расположенные точки соответствуют предельной концентрации полимера в растворах используемых гидратов.
При ступенчатом охлаждении систем до комнатной температуры на интерферограммах наблюдается появление кристаллов NММО (рис. 5).
Рис. 5.
Интерферограммы системы ПАН−МГ NММО (а–в) и ПАН−ВП NММО (г−е) при охлаждении: а, г – 120°С; б, д – 90°С; в, е – 70°С.

Следует отметить, что если кристаллизация МГ NММО в растворе ПАН проявляется в районе 80°С, т.е. температуре, соответствующей точке плавления МГ NММО, то в ВП NММО кристаллогидрат начинает образовываться только при 70°С. Отсюда следует, что высококонцентрированные растворы ПАН в маловодном NMMO, в котором свободных валентностей существенно больше, чем в МГ NMMO, склонны к переохлаждению фактически на ~50°С, что, по-видимому, обусловлено высокой энергией взаимодействия свободных N–O групп с функциональными группами полимера.
Имея представление о кинетике растворения ПАН в различных кристаллогидратах NMMO, на следующем этапе работы перешли на получение концентрированных растворов по методу твердофазного растворения целлюлозы, описанному в [34, 35]. Согласно этому подходу, в условиях всестороннего сжатия и сдвига между твердыми частицами целлюлозы и кристаллического NММО при комнатной температуре протекают механохимические процессы взаимодействия N-оксидных групп растворителя с гидроксильными группами целлюлозы, приводя к разрушению сетки Н-связей полимера и, фактически, образование твердых пред-растворов. При нагреве выше точки плавления NMMO они плавятся и переходят в высококонцентрированные, текучие растворы, характеризующиеся достаточно высокой степенью гомогенности.
Как оказалось, несмотря на гидрофобную природу ПАН, наличие в нем высокополярных функциональных групп сомономеров обеспечивает эффективное взаимодействие с NММО в процессах твердофазной активации/растворения [36–38]. Отличительной особенностью этих процессов является постоянство фазового состава системы в процессе растворения полимера от стадии приготовления “твердых растворов” до их плавления и перехода в текучее состояние. Другими словами, никаких фазовых изменений компонентов ни в процессе механического воздействия на смесь твердых порошков, ни их плавления не происходит.
Поскольку мы работаем с трехкомпонентной системой ПАН–NMMO–вода, то для описания фазовых равновесий в ней целесообразно работать с тройной фазовой диаграммой (рис. 6), которая была построена с использованием двух методов перевода ПАН в раствор. Метод твердофазной активации-растворения был описан выше. Но наряду с этом методом, существует и иной, суть которого состоит в предварительной обработке полимера водным раствором NММО, содержащим не менее 40% воды. Данный подход широко используется в промышленных процессах получения прядильных растворов целлюлозы в NMMO [39]. Несмотря на то, что при столь высоком содержании воды такой раствор не является растворителем, он облегчает проникновение жидкой фазы в микроволокна целлюлозы. Далее следует многоступенчатое удаление воды до ее содержания в растворителе менее 13.3%, получение жидких прядильных растворов и их формование. Процесс получил название ММО-процесс. Аналогичный подход был использован и для растворения ПАН.
Затемненная область на диаграмме отвечает формированию гомогенных растворов ПАН. Представленные в этой области светлые точки соответствуют растворам с содержанием ПАН от 10 до 56%, полученным по твердофазному процессу.
Фактически, с точки зрения расположения зоны истинных растворов в данном растворителе, форма этой диаграммы аналогична диаграмме системы целлюлоза−NMMO−вода [36, 37]. В частности, растворение начинается при содержании воды в NMMO равным или менее 13.3%, отвечающем моногидрату (рис. 1). Данное обстоятельство свидетельствует о том, что это критическое содержание воды для растворения обоих полимеров, хотя механизм растворения является существенно различным. В случае ПАН речь идет не о разрушении плотной сетки Н-связей, характерной для целлюлозы, а скорее о “точечном” взаимодействии –N–O групп с карбоксильными или акрилатными группами, содержание которых в сополимере ПАН не превышает 2–3%, но те нарушения в структуре полимера, которые создаются при таком локальном взаимодействии, распространяются на соседние участки макромолекулы, ослабляя взаимодействия нитрильных групп и приводя к сольватации и растворению полимера.
Схематическое изображение стадий ММО-процесса получения растворов ПАН в NММО, т.е. поэтапного удаления избытка воды, представленное темными точками на диаграмме, позволяет проследить изменение состава трехкомпонентной системы ПАН−NММО−Н2О. На рис. 7 показан внешний вид композиций на каждом этапе. При обработке 0.1 г ПАН 1.6 мл 50%-ного водного раствора NММО формируется дисперсия частиц полимера с распределением близким к однородному (рис. 7а и крайняя правая точка на рис. 6). Второй этап – частичное удаление избытка воды и образование суспензии состава: 7% ПАН, 28% Н2О и 65% NММО (рис. 7б и средняя точка на диаграмме). При дальнейшем удалении избытка воды происходит собственно растворение при составе компонентов: ~10% ПАН, ~13.3% Н2О и 76.7% NММО (черная точка в заштрихованной области диаграммы и микрофотография раствора на рис. 7в).
Рис. 7.
Фотографии системы ПАН−NMMO−вода с различным содержанием воды: а – 50, б – 28, в – 13.3% (микрофотография раствора).

Учитывая то, что ПАН – гидрофобный полимер, водная активация для него, в отличие от системы с целлюлозой, малоэффективна. Более того, в отличие от твердофазного способа, где среднее время приготовления раствора не превышает 10–15 мин, растворение по ММО-способу (с удалением избыточной воды) занимает значительно больший промежуток времени и сопряжено с достаточно сложными процессами вакуумной отгонки или выпарки воды из вязкой системы, подвергаемой воздействию температуры.
Линия, соединяющая темные точки на диаграмме, демонстрирует эволюцию состава и фазовых превращений системы ПАН–ММО–вода от двухфазной дисперсии до однофазного раствора, происходящее при уменьшении содержания в системе только одного компонента – воды. Эта особенность позволяет проанализировать характер поведения системы и в обратном направлении т.е. при увеличении содержания воды, в какой-то степени моделирующей формование волокон в водный осадитель. Гипотетически, двигаясь по диаграмме слева направо и пересекая кривую растворимости в направлении повышения содержания нерастворителя – воды, трехкомпонентная композиция попадает в область распада на фазы. В переводе на язык формования волокон это означает появление высококонцентрированной фазы, придающей струе раствора в осадителе консистенцию гель-волокна, и разбавленной по полимеру фазы, играющей роль дисперсионной среды.
Анализ таких трансформаций фазового состава системы в процессе коагуляции позволяет выбрать наиболее оптимальные условия выделения полимера из раствора. В качестве параметра, характеризующего глубину коагуляции полимерных растворов, часто используют осадительное число – требуемое количество осадителя, вызывающего распад раствора на фазы. Как правило, этот процесс вызывает изменение оптических свойств раствора, т.е. появление мутности. Традиционно, этот параметр определяют на основании фазовых превращений разбавленных растворов, происходящих под действием коагулянтов.
Методика определения осадительных чисел состоит в постепенном введении нерастворителя в 1%-ный раствор полимера и определению его мутности в момент начала коагуляции. Для растворов ПАН в ДМСО, ДМФА и этиленкарбонате – наиболее популярных на практике растворителей ПАН, осадительные числа при использовании в качестве осадителя воды составляют 13.5, 13.5 и 18 мл, соответственно [38]. Осадительное число можно использовать в качестве оценки термодинамической активности осадителей, а также оценивать их “мягкость/жесткость” по отношению к интенсивности процесса коагуляции. Так, малые значения осадительного числа говорят о большом сродстве осадителя к растворителю [40] и указывают на высокую скорость фазового распада, т.е. на “жесткий” режим формования. Высокая растворяющая способность NMMO и его высокая термодинамическая активность к воде дает основание предположить, что процесс коагуляции растворов ПАН в NMMO будет отличаться от присущего традиционным растворам при использовании одного и того же коагулянта – воды. Для определения осадительного числа использовали раствор ПАН в моногидрате NMMO, который готовили и осаждали при Т = 100°С. Оптические свойства композиции определяли по изменению коэффициента пропускания (величина, обратная коэффициенту экстинкции) при различных длинах волн для образцов с различным содержанием введенной воды (рис. 8).
Рис. 8.
Зависимость коэффициента пропускания при длинах волн 540 и 750 нм для 1%-ного раствора ПАН в МГ NMMO от содержания введенной воды.

При добавлении в раствор до 2.5 мл воды, что соответствует концентрации 15.8%, коэффициент пропускания светового потока практически не изменяется. Дальнейшее увеличение содержания воды в системе до 16% приводит к незначительному снижению коэффициента пропускания. Наконец, при достижении содержания воды в системе 16.8% наблюдается резкое падение значений коэффициентов пропускания, т.е. раствор “мутнеет”.
Таким образом, проведенное контролируемое осаждение 1%-ных растворов ПАН в NMMO водой выявило, что распад 1%-ного раствора объемом 100 мл на фазы по изменением оптических свойств системы наблюдается при добавлении 3.5 мл (16.8%) воды. Это означает, что в случае NMMO в качестве растворителя значения осадительного числа при коагуляции раствора водой почти в 4 раза ниже, чем для ДМСО и ДМФА, и в 5 раз ниже по сравнению с системами на основе этиленкарбоната, что подтверждает высказанное ранее предположение об особенностях процесса осаждения растворов ПАН в NMMO водой по сравнению с растворами в традиционных апротонных растворителях.
В промышленных процессах 100%-ный осадитель, например, вода, используется крайне редко. Такой осадитель приводит к высоким скоростям выделения полимерной фазы и образованию дефектной морфологии волокон, приводящей к их невысоким механическим характеристикам. Более того, регенерация таких ванн экономически не выгодна. Для снижения скоростей коагуляции используют более “мягкие” осадители – для растворов ПАН, как правило, водные растворы растворителя [27, 39, 41, 42]. В случае MMO-процесса, при формовании целлюлозных волокон используют осадительные ванны с содержанием растворителя порядка 20% или, в поисковом плане – спирты [29].
В связи с этим, представляло реальный интерес проанализировать процесс коагуляции раствора ПАН 20%-ным водным раствором NMMO. Соответствующие данные представлены на рис. 9.
Рис. 9.
Зависимость коэффициента пропускания для 1%-ного раствора ПАН в МГ NMMO от содержаниявведенного 20%-ного водного раствора NMMO.

Из приведенных зависимостей видно, что с увеличением содержания осадителя в системе до 6.3 мл (18.3%) значения коэффициента пропускания снижаются плавно. Дальнейшее увеличение доли введенного в раствор осадителя до 8.2 мл (19.8%) приводит к резкому повышению коэффициента экстинкции и раствор становится мутным.
Как обсуждалось ранее, оптимальным содержанием NMMO в осадительной ванне является 20%. Использование осадительных ванн с более высоким содержанием растворителя хотя и нетехнологично, но может быть востребовано в процессах получения мембран и полых волокон, где требуется тонкое регулирование морфологии полимерного материала.
Как видно из рис. 10, наибольшее изменение коэффициента пропускания светового потока 1%-ного раствора ПАН в МГ NMMO с различным содержанием 40%-ного водного раствора NMMO наблюдается при длине волны 750 нм, соответствующей минимальным размерам частиц выделяющейся при осаждении фазы. С увеличением содержания осадителя в системе значения коэффициента пропускания плавно снижаются, а при добавлении 12.8 мл (21%) осадителя раствор мутнеет, и значения коэффициента пропускания резко падают.
Рис. 10.
Зависимость коэффициента пропускания для 1%-ного раствора ПАН в МГ NMMO с различным содержанием введенного 40%-ного водного раствора NMMO.
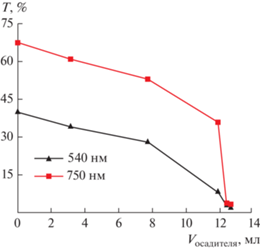
При осаждении исследуемых растворов 50%-ным водным раствором NMMO постоянства коэффициента пропускания в начальной стадии накопления в системе такого нерастворителя практически не происходит, но наблюдается более резкое его падение по сравнению с водой, 20 и 40%-ными водными растворами NMMO (рис. 11).
Рис. 11.
Зависимость коэффициента пропускания для 1%-ного раствора ПАН в МГ NMMO с различным содержанием 50%-ного водного раствора NMMO.

При добавлении более 15–20 мл такого псевдо-осадителя коэффициент пропускания достигает минимума и практически не изменяется при введении дальнейших порций 50%-ного водного раствора NMMO, т.е. такой осадитель не вызывает фазового распада и является скорее разбавителем раствора. Финальная композиция находится в термодинамически неравновесном состоянии незавершенного микрофазового разделения и кинетически устойчива.
Состояние этой системы наглядно демонстрируют приведенные на рис. 12 фотографии исходного раствора ПАН и смесевых растворов с различным количеством введенного 50%-ного водного раствора NMMO.
Рис. 12.
Фотографии исходного 1%-ного раствора ПАН (а) и композиций после добавления к 100 мл раствора 5.8 (б) и 19.8 (в) мл 50%-ного водного раствора NMMО.

Как видно из представленных фотографий, добавление 19.8 мл 50%-ного водного раствора NMMО к раствору ПАН приводит к легкому помутнению, свидетельствующему о двухфазности смесевой системы при отсутствии ожидаемого гелеобразования. По-видимому, это связано с высоким содержанием растворителя в таком “осадителе”, которое приводит к общему содержанию воды в композиции ~23%, что примерно соответствует бигидрату NMMO с точкой плавления ниже 35°С, который способен локально кристаллизоваться при комнатной температуре.
Как следует из полученных данных, приведенных в табл. 1, для растворов ПАН в NMMO наиболее активным – жестким осадителем является вода. Увеличение содержания NMMO в водной осадительной ванне до 20 и 40% сдвигает порог осаждения вправо, тем самым увеличивается время распада на фазы, т.е. происходит смягчение водного осадителя, что способствует формированию более выгодной морфологии и улучшает технологичность процесса. При этом 50%-ный водный раствор NMMO практически не приводит к коагуляции раствора.
Таблица 1.
Осадительные числа для 1%-ного раствора ПАН в МГ NММО с разными коагулянтами
| Коагулянт | Вода, мл | 20% NММО, мл | 40% NММО, мл | 50% NММО, мл | Вода (для 1%-ного раствора в ДМСО), мл |
|---|---|---|---|---|---|
| Осадительное число | 3.5 | 8.2 | 12.8 | – | 13.5 |
Осадительное число характеризует термодинамическую способность осадителя снижать активность растворителя и, тем самым, перераспределять взаимодействия полимер-растворитель в пользу полимер-полимерных контактов, но не учитывает кинетику коагуляции, представляло интерес рассмотреть кинетические особенности этого процесса. В качестве кинетического критерия взаимодействия раствор-осадитель целесообразно использовать диффузионные характеристики.
С помощью интерференционного метода были исследованы массообменные процессы, протекающие при контакте растворов ПАН в МГ NMMO с водой и водными растворами NMMО (40 и 50 мас. %). На рис. 13 представлены интерферограммы, иллюстрирующие процесс взаимодиффузии в начальный момент контакта раствора ПАН в МГ NMMO (5 мас. %) с осадителем и спустя 10 минут после начала процесса.
Рис. 13.
Интерферограммы диффузионной зоны в ходе взаимодействия 5%-ного раствора ПАН с водой (а, г) и водными растворами NММО – 40 (б, д) и 50 мас. % (в, е) через 10 c (а, б, в) и 10 мин (г, д, е) после контакта компонентов.

Эти исследования проводили при температуре 95°С, превышающей температуру плавления МГ NММО. Как видно из рис. 13а, 13г, при контакте раствора с водой в диффузионной зоне происходит формирование полимерной пленки, при этом интенсивное проникновение осадителя приводит к появлению в ней анизометричных дефектов (вакуолей). При замене воды на более мягкий осадитель (40%-ный раствор NММО в воде) можно наблюдать формирование плeнки с меньшим количеством вакуолей (рис. 13б, 13д).
В случае использования в качестве жидкой фазы, контактирующей с раствором ПАН, 50%-ного водного раствора NMMO оптическая картина зоны взаимодиффузии принципиально изменяется (рис. 13в, 13е). В первые секунды контакта в диффузионной зоне формируется не полимерная пленка, а гелеобразный слой. С увеличением времени контакта он рассасывается, а интерференционные полосы непрерывно переходят из одной фазы в другую, как в случае систем с полной совместимостью. Эти данные подтверждают вывод, сделанный при анализе данных по порогу осаждения, что 50%-ный раствор NMMO не вызывает коагуляцию раствора ПАН.
ЗАКЛЮЧЕНИЕ
Путем использования двух подходов: твердофазной активации смесей твердых полимера и растворителя с последующим нагреванием (1) и предварительной обработки порошка ПАН водным раствором NMMO и удалением избытка воды (2) впервые построена тройная фазовая диаграмма системы ПАН−NMMO−вода. Использование двух гидратов NMMO показало, что процесс растворения ПАН начинается с моногидрата, в котором достигается максимальная концентрация полимера 15%, в то время как в NMMO, содержащем 10% воды, возможно получить даже 56%-ный раствор. Исследование диффузионных процессов, протекающих при растворении пленки ПАН в различных гидратах NMMO показало, что определяющей является диффузия полимера в растворитель, а не наоборот. Моделирование процесса формования волокон/пленок позволило выявить переход от жестких коагулянтов к более мягким при добавлении растворителя в жесткий осадитель (воду). Оптимальные осадительные составы (в зависимости от области применения волокон/пленок) содержат от 20 до 40% NMMO в воде.
Список литературы
Iovleva M.M., Smirnova V.N., Budnitskii G.A. The solubility of polyacryonitrile // Fibre Chem. 2001. V. 33. № 4. P. 262–264. https://doi.org/10.1023/A:1012934313303
Некрасов И.К., Кузовлева Р.В. Свойства полиакрилонитрила в водных растворах роданистого натрия // Высокомолек. соед. Сер. А. 1971. Т. 13. № 11. С. 2607–2611.
Zhang J., Yamagishi N., Gotoh Y. Facilitated fibrillation of regenerated cellulose fibers by immiscible polymer blending using an ionic liquid // Cellulose. 2019. V. 26. P. 889–902. https://doi.org/10.1007/s10570-018-2120-9
Byrne N., Leblaisa A., Fox B. Preparation of polyacrylonitrile–natural polymer composite precursors for carbon fiber using ionic liquid co solvent solutions // J. Mater. Chem. A. 2014. V. 2. P. 3424–3429. https://doi.org/10.1039/C3TA15227H
Makarov I.S., Golova L.K., Kuznetsova L.K., Rebrov A.V., Berkovich A.K., Skvortsov I.Yu., Kulichikhin V.G. Composite fibers based on cellulose and polyacrylonitrile copolymers // Russ. J. Gen. Chem. 2017. V. 87. № 6. P. 1351–1356.
Golova L.K., Makarov I.S., Vinogradov M.I., Kuznetsova L.K., Kulichikhin V.G. Morphological features and rheological properties of combined cellulose and polyacrylonitrile solutions in N-methylmorpholine-N-oxide // Polym. Sci. Ser. A. 2018. V. 60. P. 796–804. https://doi.org/10.1134/S0965545X18060056
Голова Л.К., Макаров И.С., Матухина Е.В., Купцов С.А., Шамбилова Г.К., Куличихин В.Г. Кристаллосольваты термотропных алкиленароматических сополиэфиров и поли-м-фениленизофталамида с N-метилморфолин-N-оксидом // Высокомолек. соед. Сер. А. 2008. Т. 50. № 6. С. 1020–1036.
Pakshver E.A. Advances in the production of polyacrylonitrile fibres (review) // Fibre Chem. 1977. V. 8. № 5. P. 463–474. https://doi.org/10.1007/BF00546830
Mezhirov M.S. The gelation time in wet spinning // Fibre Chem. 1973. V. 4. № 4. P. 367–369. https://doi.org/10.1007/BF00545782
Knoop M.T., Lieske A. Pat. 11180869B2 USA. 2016.
Kruchinin N.P., Spirova T.A., Medvedev V.A., Serkov A.T., Radishevskii M.B., Volodin V.I., Prokhorov V.A., Krutova I.N., Egorova R.V., Grekhova E.V. Morphological and structural features of polyacrylonitrile fibres spun by the dry-wet method // Fibre Chem. 1992. V. 23. № 3. P. 169–174. https://doi.org/10.1007/BF00545854
Kotomin S.V., Kulichikhin V.G., Skvortsov I.Yu. Mechanotropic mechanism of electrospinning // AIP Conference Proceedings. 2018. V. 1981. P. 020183. https://doi.org/10.1063/1.5046045
Mezhirov M.S. A new method of studying the gelation rate in wet spinning // Fibre Chem. 1972. V. 3. № 3. P. 247–250. https://doi.org/10.1007/BF00543240
Skvortsov I.Y., Kulichikhin V.G., Ponomarev I.I., Varfolomeeva L.A., Kuzin M.S., Skupov K.M., Volkova Y.A., Razorenov D.Y., Serenko O.A. Solubility, rheology, and coagulation kinetics of poly-(o-aminophenylene)naphthoylenimide solutions // Polymers. 2020. V. 12. № 11. P. 2454. https://doi.org/10.3390/polym12112454
Kulichikhin V.G., Skvortsov I.Yu., Mironova M.I., Ozerin A.N., Kurkin T.S., Berkovich A.K., Frenkin E.I., Malkin A.Ya. From polyacrylonitrile, its solutions, and filaments to carbon fibers II. Spinning PAN-precursors and their thermal treatment // Adv. Polym. Technol. 2018. V. 37. № 4. P. 1099–1113. https://doi.org/10.1002/adv.21761
Peng G.-Q., Zhang X.-H., Wen Y.-F., Yang Y.-G., Liu L. Effect of coagulation bath DMSO concentration on the structure and properties of polyacrylonitrile (PAN) nascent fibers during wet-spinning // J. Macromol. Sci. Part B. 2008. V. 47. № 6. P. 1130–1141. https://doi.org/10.1080/00222340802403214
Hao J., An F., Yu Y., Zhou P., Liu Y., Lu Ch. Effect of coagulation conditions on solvent diffusions and the structures and tensile properties of solution spun polyacrylonitrile fibers // J. Appl. Polym. Sci. 2017. V. 134. № 5. P. 44390. https://doi.org/10.1002/app.44390
Wang Y.-X., Wang C.-G., Yu M.-J. Effects of different coagulation conditions on polyacrylonitrile fibers wet spun in a system of dimethylsulphoxide and water // J. Appl. Polym. Sci. 2007. V. 104. № 6. P. 3723–3729. https://doi.org/10.1002/app.25723
Koningsveld R., Stockmayer W.H., Nies E. Polymer Phase Diagrams: A Textbook. Oxford: Oxford University Press, 2001.
Папков С.П., Ефимова С.Г. О классификации систем полимер−растворитель // Высокомолек. соед. 1966. Т. 8. № 11. С. 1984–1989.
Иовлева М.М., Бандурян С.И. Фазовые равновесия в системах полимер-растворитель: развитие в области волокон // Высокомолекулярные соединения. 2010. Т. 52. № 11. С. 2033–2037 (Iovleva M.M., Banduryan S.I. // Polym. Sci. Ser. A. 2010. V. 52. P. 1228.)
Папков С.П. Физико-химические основы переработки растворов полимеров. М.: Химия, 1971.
Flory P.J. The configuration of real polymer chains // J. Chem. Phys. 1949. V. 17. P. 303. https://doi.org/10.1007/978-1-4684-2853-7_5
Huggins M.L.In: Ulrich R.D. (eds) Macromolecular science. Contemporary topics in polymer science, vol. 1. Springer, Boston, MA. https://doi.org/10.1007/978-1-4684-2853-7_6
Dong R., Zhao J., Zhang Y., Pan D. Morphology control of polyacrylonitrile (PAN) fibers by phase separation technique // J. Polym. Sci. Part B. Polym. Phys. 2009. V. 47. № 3. P. 261–275.
Pakshver E.A., Kalabin A.L. Gelation in spinning chemical fibres from solutions of polymers // Fiber Chem. 2005. V. 37. № 5. P. 315–318.
Biganska O., Navard P. Morphology of cellulose objects regenerated from cellulose–N-methylmorpholine N-oxide–water solutions // Cellulose. 2009. V. 16. P. 179–188.
Romanov V.V., Kruchinin N.P., Lunina O.B., Trifonova N.P., Kulichikhin V.G. Effect of precipitation conditions on the properties of yarns obtained from solutions of cellulose in methylmorpholine oxide // Fibre Chem. 1986. V. 17. P. 417–419. https://doi.org/10.1007/BF00543772
Makarov I.S., Golova L.K., Vinogradov M.I., Mironova M.V., Arkharova N.A., Klechkovskaya V.V., Kulichikhin V.G. Morphological transformations in the process of coagulation of cellulose solution in N-methylmorpholine N-oxide with isobutanol // Polym. Sci. Ser. C. 2021. V. 63. P. 161–169. https://doi.org/10.1134/S181123822102003X
Biganska O. PhD Thesis. Paris: École Nationale Supérieure des Mines de Paris, 2012.
Bairamov D.F., Chalykh A.E., Feldstein M.M., Siegel R.A., Platé N.A. Dissolution and mutual diffusion of poly(N-vinyl pyrrolidone) in short-chain poly(ethylene glycol) as observed by optical wedge microinterferometry // J. Appl. Polym. Sci. 2002. V. 85. P. 1128–1136. https://doi.org/10.1002/app.10635
Чалых А.Е. Диффузия – метод исследования полимерных систем // Высокомолек. соед. 2001. Т. 43. № 12. С. 2304–2328.
Платонов В.А., Куличихин В.Г., Белоусов Ю.Я. // Сб. тез. докл. Всесоюз. семинара “Структура и реакционная способность целлюлозы и ее производных”. Минск, 1982.
Golova L.K., Bondarenko G.N., Makarov I.S., Kuznetsova L.K., Vinogradov M.I., Kulichikhin V.G. Peculiarities of dissolving polyacrylonitrile copolymer containing methylsulfo groups in N-methylmorpholine-N-oxide // Polym. Sci. Ser. A. 2020. V. 62. P. 597–606. https://doi.org/10.1134/S0965545X20060036
Makarov I.S., Golova L.K., Kuznetsova L.K., Shljakhtin A.V., Nifant’ev I.E., Kulichikhin V.G. Пaт. 2541473C2 PФ. 2013.
Golova L.K. New cellulose fiber lyocell // Rus. J. Gen. Chem. 2002. V. XLVI. P. 49–57.
Куличихин В.Г., Голова Л.К. Растворы целлюлозы в оксидах третичных аминов: межмолекулярные взаимодействия, структура, реология. Научные основы химической технологии углеводов. М.: ЛКИ, 2008.
Пакшвер А.Б. Карбоцепные волокна. М.: Химия, 1966.
Fink H.P., Weigel P., Purz H.J. Formation of lyocell-type fibres with skin-core structure // Lenzing. Ber. 1998. V. 78. P. 41.
Основы физики и химии полимеров / Под ред. В.Н. Кулезнева. Учебное пособие для вузов. М.: Высш. школа, 1977.
Romanov V.V., Sokira A.N., Lunina O.B., Iovleva M.M. Morphological features of the structure of fibres prepared from solutions of cellulose in methylmorpholine oxide // Fibre Chem. 1988. V. 20. № 1. P. 38.
Голова Л.К., Бородина О.Е., Кузнецова Л.К., Любова Т.А., Крылова Т.Б. Твердофазный ММО-процесс // Хим. волокна. 2000. № 4. С. 14–20 (Golova L.K., Borodina O.E., Kuznetsova L.K., Lyubova T.A., Krylova T.B. // Fibre Chem. 2000. V. 32. № 4. P. 243.)
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал





